
19£Æ(8∑÷)A°¢B°¢C°¢D «Àƒ÷÷ø…»Ð”⁄ÀƵƒŒÔ÷ £¨À¸√«∑÷±”…œ¬¡–“ı¿Î◊””ΗٿÎ◊”¡Ω¡Ω◊È∫œ∂¯≥…£¨√ø÷÷¿Î◊”÷ªƒÐ π”√“ª¥Œ°£
|
—Ù¿Î◊” |
Na+ |
NH4+ |
A13+ |
Ba2+ |
|
“ı¿Î◊” |
SO42- |
OH- |
CO32- |
NO3- |
Ω´A°¢B°¢C°¢DÀƒ÷÷ŒÔ÷ »Ð“∫¡Ω¡ΩªÏ∫œ(±ÿ“™ ±£¨”–µƒ µ—ÈΩ¯––º”»»)∆‰ µ—Èœ÷œÛ»Áœ¬£∫
¢ŸΩ´B»Ð“∫∫ÕC»Ð“∫ªÏ∫œ≤˙…˙∞◊…´≥¡µÌ£¨∞◊…´≥¡µÌ≤ª»Ð”⁄À·°£
¢⁄Ω´A»Ð“∫∫ÕD»Ð“∫ªÏ∫œ≤˙…˙∞◊…´≥¡µÌ£¨Õ¨ ±”–∆¯ÃÂ…˙≥…°£
¢€Ω´A»Ð“∫∫ÕB»Ð“∫ªÏ∫œ≤˙…˙∞◊…´≥¡µÌ£¨Õ¨ ±”–∆¯ÃÂ…˙≥…°£
ƒ«√¥A°¢B°¢C°¢D∑÷±Œ™°°°°°°°°°°°°°° °¢°°°°°°°°°°°°°° °¢°°°°°°°°°°°°°° °¢
°°°°°°°°°° °°°£
18£Æ(10∑÷) µ—È “–Ë”√480mL°° 1.0mol/LµƒNaOH»Ð“∫°£œ¬Õº «∏√—ß…˙‘⁄ µ—È “≈‰÷∆∏√NaOh»Ð“∫µƒπ˝≥à 擂պ£¨«Îæð¥Àªÿ¥”–πÿŒ °£
°°°° 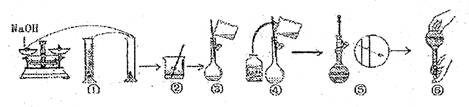
°° (1)‘⁄…œ ˆ µ—Èπ˝≥Ã÷–£¨”√µΩµƒ»ð¡øµƒπÊ∏Ò «°°°°°°°°°°°°°°°°°° °£
°° (2)”√“—÷™÷ ¡øŒ™y gµƒ±Ì√Ê√Û£¨◊º»∑≥∆»°°°°°°°°°°°°°°°°°°° g NaOHπÃð£
°° (3)π€≤Ï≈‰÷∆NaOH»Ð“∫µƒπ˝≥à 擂պ£¨÷∏≥ˆ∆‰÷–”–¥ÌŒÛµƒ «(ÃÓ≤Ÿ◊˜–Ú∫≈)°£‘⁄¢Ÿ-¢Þ÷–£¨√ª”–ÃÂœ÷≥ˆ¿¥µƒ“ª∏ˆ÷ÿ“™≤Ω÷Ë «£∫°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° °£
17£Æ(8∑÷)≥£Œ¬œ¬‘⁄20mL 0.1mol/L Na2CO3»Ð“∫÷–÷µŒº”»Î0.1mol/ L HC1»Ð“∫40mL£¨»Ð“∫µƒPH÷µ÷Ω•ΩµµÕ£¨¥À ±»Ð“∫÷–∫¨Ãº‘™ÀÿµƒŒ¢¡£ŒÔ÷ µƒ¡ø≈®∂»µƒ∞Ÿ∑÷∫¨¡ø(◊ð÷·)“≤∑¢…˙±‰ªØ(CO2“Ú“ð≥ˆŒ¥ª≠≥ˆ)£¨»Áœ¬ÕºÀ˘ æ
ªÿ¥œ¬¡–Œ £∫
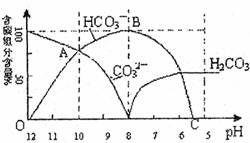
°° (1)‘⁄0.1mol/L Na2CO3»Ð“∫À˘”–—Ù¿Î◊”∫Õ“ı¿Î◊”µƒ≈®∂»”–∫Œπÿœµ£ø(”√µ» Ω±Ì æ)°°°°°°°°°°°° °£
°° (2)µ±º”»Î—ŒÀ· π»Ð“∫PH÷µŒ™10 ±£¨ªÏ∫œ“∫÷–∫¨Ãº‘™Àÿµƒ¿Î◊”ŒÔ÷ µƒ¡ø÷Ʊ»Œ™°°°°°°°°°° °£
°° (3)ÀÊ◊≈—ŒÀ·µƒº”»Î£¨«Î–¥≥ˆBC∂Œµƒ¿Î◊”∑Ω≥Ã Ω°°°°°°°°°°°°°°°°°° °£
°° (4)µ±ªÏ∫œ“∫µƒPH=°°°°°°°°°° ±£¨ø™ º∑≈≥ˆCO2∆¯Ã°£
16£Æ“—÷™”–ª˙ŒÔA÷–∫¨Ãº°¢—ı°¢µ™‘™Àÿ£¨«“A∑÷◊”Œ™÷–µ™‘≠◊”◊Ó…Ÿ£¨«“Aµƒœý∂‘∑÷◊”÷ ¡øŒ™128£¨‘ÚA÷–«‚‘≠◊” ˝◊Ó∂ýŒ™°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°°°° A£Æ16°°°°°°°°°°°°°°°°°°°°°° B£Æ14°°°°°°°°°°°°°°°°°°°°°° C£Æ18°°°°°°°°°°°°°°°°°°°°°° D£ÆŒÞ∑®»∑∂®
|
15£Æ”–“ª÷÷¿∂…´æßÃÂ[ø…±Ì 挙£∫MxFey(CN)6]£¨æ≠X…‰œþ—–æø∑¢œ÷£¨À¸µƒΩ·ππÃÿ’˜ «Fe3+∫ÕFe2+ª•œý’ºæð¡¢∑Ωê•≤ªœý¡⁄µƒ∂•µ„£¨∂¯CN-Œª”⁄¡¢∑Ωõƒ¿‚≥§°£∆‰æßÃÂ÷–“ı¿Î◊”µƒ◊Ó–°Ω·π𵕑™»Á”“ÕºÀ˘ æ°£œ¬¡–Àµ∑®’˝»∑µƒ «°°°°°°°° (°°°° )
°°°° 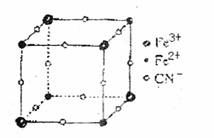
°°°°°° A£Æ∏√æßàٔ⁄¿Î◊”æßã¨M≥ +2º€°°°°°° B£Æ∏√æßàٔ⁄¿Î◊”æßã¨M≥ +1º€
°°°°°° C£Æ∏√æßõƒªØ—ß ΩŒ™MFe2(CN)6°°°°°°°° D£ÆæßÃÂ÷–”Î√ø∏ˆFe3+æý¿Î◊ÓΩ¸«“µ»æý¿Îµƒ
°°°°°° CN-Œ™3∏ˆ
14£ÆªÏ∫œœ¬¡–∏˜◊ÈŒÔ÷ π÷Æ≥‰∑÷∑¥”¶£¨º”»»’Ù∏…≤˙ŒÔ≤¢‘⁄300°Ê◊∆…’÷¡÷ ¡ø≤ª±‰£¨◊Ó÷’≤–¡ÙπÃÃÂŒ™¥ø檌Եƒ «°°°°°°°°°°°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°°°° A£ÆœÚCuSO4»Ð“∫÷–º”»Î“ª–°øÈΩ Ùƒ∆
°°°°°° B£Æµ»ŒÔ÷ µƒ¡ø≈®∂»°¢µ»Ãª˝µƒ(NH4)2SO4”ÎBaC12»Ð“∫
°°°°°° C£Æµ»ŒÔ÷ µƒ¡øNaHCO3”ÎNa2O2πÃÃÂ
°°°°°° D£Æ‘⁄NaBr»Ð“∫÷–Õ®»Î…Ÿ¡ø¬»∆¯
13£ÆŒ™¡À«¯±ŒÂ∆øŒÞ…´»Ð“∫£∫HC1°¢A1C13°¢Ba(NO3)2°¢NaC1°¢Na2CO3£¨ÀƒŒª—ß…˙∂º√ª”–”√æ∆æ´µ∆£¨»˝Œª—ß…˙¡Ì”√¡À ‘º¡(º◊¡Ì”√¡À∑”Ù ‘º¡°° ““¡Ì”√¡ÀNaOH»Ð“∫°° ±˚¡Ì”√¡À◊œ…´ Ø»Ô ‘“∫)£¨∂°√ª”–¡Ì”√»Œ∫Œ ‘º¡£¨∆‰÷–≤Ÿ◊˜≤Ω÷Ë“ª∂®◊Ó…Ÿµƒ «°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°°°° A£Æº◊∫Õ±˚°°°°°°°°°°°°°° B£Æ““°°°°°°°°°°°°°°°°°°°°°° C£Æ““∫Õ±˚°°°°°°°°°°°°°° D£Æ∂°
12£Æœ¬Õº « µ—È “÷∆»°““À·““ı•µƒ◊∞÷√°£‘Úœ¬¡–Àµ∑®’˝»∑µƒ «°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°° 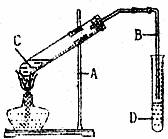
°°°°°° A£Æ”“±þµºπÐ≤»α•∫ÕúÀ·ƒ∆»Ð“∫°°°°°°°°°°°° B£Æ∑¥”¶Ω· ¯∫ÛπÐC“∫ÃÂø…ƒÐª·±‰∫⁄…´
°°°°°° C£Æ ‘πÐC÷–º”»Î ‘º¡µƒÀ≥–Ú «£∫2mL≈®¡ÚÀ·°˙3ml““¥º°˙2mL““À·
°°°°°° D£Æ ‘πÐD÷–”Õ◊¥ŒÔ‘⁄œ¬≤„£¨±•∫ÕúÀ·ƒ∆»Ð“∫÷˜“™Œ™¡À÷–∫Õª”∑¢≥ˆµƒ““À·
11£Æ∂‘ Â∂°ª˘±Ω∑””κ◊»©Àı∫œ–Œ≥…ª∑◊¥£¨‘Ï≥…±≠◊¥ππ‘Ï£¨“Ú∆‰∑÷◊”–Œ◊¥”Îœ£¿∞ •±≠(callix crater)œýÀ∆£¨«“ «”…∂ý∏ˆ±Ωª∑ππ≥…µƒ∑ºœ„◊Â∑÷◊”(arene)£¨”…¥Àµ√√˚Œ™±≠∑º(calizarene)£¨“≤≥∆÷ÆŒ™ªØ—ߺ“µƒ •±≠£¨”–πÿ±≠∑ºµƒ¿ÌΩ‚øœ∂®≤ª’˝»∑µƒ «°°°° °°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° (°°°° )
°°°° 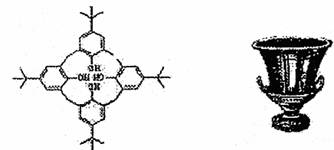
°°°°°° A£Æ±≠∑º≤ª Ù”⁄Ã˛∂¯ Ù”⁄∑”
°°°°°° B£Æ±≠µ◊Àƒ∏ˆ∑”Ù«ª˘œýª•◊˜”√£¨Ù«ª˘º‰µƒ◊˜”√¡¶ Ù”⁄π≤º€º¸
°°°°°° C£Æ±≠∑ºƒÐ”Ϋ‚—ıªØƒ∆»Ð“∫°¢≈®‰ÂÀƺ∞À·–‘∏þ√ÃÀ·ºÿ»Ð“∫∑¥”¶
°°°°°° D£Æ±≠∑ºµƒ∑÷◊” ΩŒ™£∫C44H56O4
9£Æ‘⁄◊ˆ÷–∫Õ»»µƒ≤‚∂® µ—È÷–£¨ π”√œ¬¡–ŒÔ∆∑≤ª «Œ™¡Àºı…Ÿ µ—ÈŒÛ≤Óµƒ «°°°°°°°°°°°°°°°° (°°°° )
°°°°°° A£ÆÀÈ≈ðƒ≠ÀСœ°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° B£Æª∑–Œ≤£¡ßΩ¡∞Ë∞Ù
°°°°°° C£Æµ◊≤øµÊ÷ΩÃı°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°°° D£Æ¡Ω∏ˆ¡øÕ≤
|
°°°°°° A£ÆµÁΩ‚∑®÷∆¬¡ ±“ª∞„ «”√»€»⁄赃—ıªØ¬¡Ω¯––µÁΩ‚µ´“≤ø…”√∆‰œý”¶µƒ—Œ£¨»Á»€»⁄赃
°°°°°° A1C13
°°°°°° B£ÆµÁΩ‚∑®…˙≤˙¬¡ ±£¨–Ë∂‘¬¡Õ¡øÛΩ¯––÷¥ø£¨‘⁄÷¥øπ˝≥Ã÷–”¶”√¡À—ıªØ¬¡ªÚ«‚—ıªØ¬¡µƒ
°°°°°° ¡Ω–‘
°°°°°° C£Æ‘⁄¬»ºÓ𧓵÷–£¨µÁΩ‚≥ÿ÷–µƒ“ıº´≤˙…˙µƒ «H2£¨NaOH‘⁄—Ùº´∏ΩΩ¸≤˙…˙
°°°°°° D£Æ¬»ºÓ𧓵∫ÕΩ Ùƒ∆µƒ“±¡∂∂º”√µΩ¡ÀNaC1£¨‘⁄µÁΩ‚ ±À¸√«µƒ“ıº´∂º «C1- ßµÁ◊”
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com