
15.某同学研究铝及其化合物的性质设计了如下两个实验方案
方案①:2.7gAl X溶液
X溶液 氢氧化铝沉淀
氢氧化铝沉淀
方案②:2.7gAl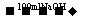 Y溶液
Y溶液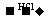 氢氧化铝沉淀
氢氧化铝沉淀
NaOH和HCl的浓度均是3mol/L,下图是向X溶液和Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是
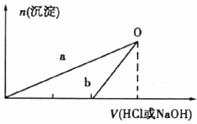
A.b曲线表示的是向X溶液中加入NaOH溶液
B.在O点时两方案中所得溶液浓度相等
C.a、b曲线表示的反应都是非氧化还原反应
D.X溶液显酸性,Y溶液显碱性
第Ⅱ卷(必做120分+选做32分,共152分)
选做部分,考生必须从中选择2个物理题,1个化学题和1个生物题作答。
[必做部分]
14.MOH和ROH两种一元碱的溶液分别加水稀释时,pH变化如下图所示,下列叙述中正确的是
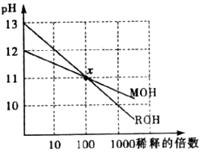
A.MOH和ROH都是强碱
B.在 点,
点,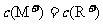
C.稀释前,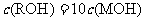
D.常温下,pH之和为14的醋酸和ROH溶液等体积混合,所得溶液可能呈中性
13.对下列发生的化学反应的描述不正确的是
A.过量的SO2通入NaOH溶液中: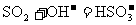
B.等物质的量的氯气与溴化亚铁反应: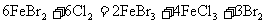
C.Na2CO3溶液显碱性的原因:

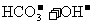
D.NaHCO3溶液中加入过量的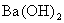 溶液:
溶液:
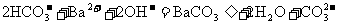
12.向一定量的稀碳酸钠溶液中逐滴加入等体积等浓度的盐酸,所得溶液中下列等式成立的是
①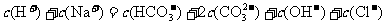
②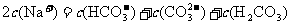
③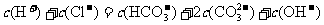
④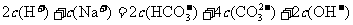
A.①③④ B.②③④ C.①②③ D.全部正确
11.下列说法正确的是
A.10mL质量分数为98%的H2SO4,用水稀释至100mL,H2SO4的质量分数为9.8%
B.正戊烷、异戊烷和新戊烷中的共价键数相同
C.质量均为6g的金刚石和石墨中都含有6.02×1023个碳原子
D.标准状况下,11.2LHCl中含有的离子总数是6.02×1023
10.下列说法正确的是
A.将足量的二氧化硫通入到紫色石蕊试液中,先变红后褪色
B.检验某溶液中是否含有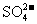 ,BaCl2溶液不能用HNO3酸化
,BaCl2溶液不能用HNO3酸化
C.用湿润的pH试纸测定溶液的pH
D.合金的熔点一般比成分金属的熔点高
9.下列叙述不正确的是
A.淀粉、纤维素、蛋白质都属于天然高分子化合物
B.蒸馏法是历史最悠久的海水淡化方法
C.熔融状态下能导电的物质一定是离子晶体
D.不同的原子质子数可能相同
24.(14分)有机物A(C11H12O2)可调配果味香精。用含碳、氢、氧三种元素的有机物B和C为原料合成A。
(1)有机物B的蒸汽密度是同温同压下氢气密度的23倍,0.1molB在氧气中完全燃烧生成标况下体积为4.48L的CO2和5.4g水,则有机物B的分子式为
(2)有机物C的分子式为C7H8O,C能与钠反应,不与碱反应,也不能使溴的四氯化碳溶液褪色。C的结构简式为 。
(3)已知两个醛分子间能发生如下反应:
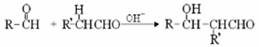 (﹣R、﹣R’表示氢原子或烃基)
(﹣R、﹣R’表示氢原子或烃基)
用B和C为原料按如下路线合成A:
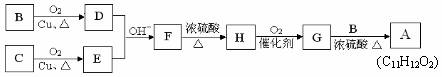
① 上述合成过程中涉及的反应类型有: (填写序号)
a取代反应;b 加成反应;c 消去反应;d 氧化反应;
② B转化D的化方程式:
。
③ F的结构简式为: 。
④ G和B反应生成A的化方程式: 。
(4)F的同分异构体有多种,写出既能发生银镜反应又能发生水解反应,且苯环上只有一个取代基的所有同分异构体的结构简式
23.(16分)某化研究小组为证明CO具有还原性,首先查阅相关的资料,获取下列信息 :①C+H2O(g)
:①C+H2O(g) CO+H2 CO+H2O(g)
CO+H2 CO+H2O(g)
 CO2+H2 CO2+C
CO2+H2 CO2+C 2CO ②CO和H2都可在加热条件下与CuO反应 ③CO有剧毒,在空气中可以燃烧。根据以上信息和有关知识,他们设计如下图所示的实验装置。
2CO ②CO和H2都可在加热条件下与CuO反应 ③CO有剧毒,在空气中可以燃烧。根据以上信息和有关知识,他们设计如下图所示的实验装置。
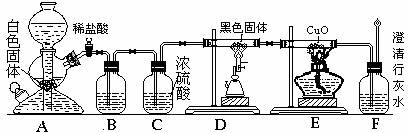
请回答下列问题:
(1)装置A中反应的离子方程式是 。
(2)装置B最适宜的试剂是 ;必须用装置C吸收气体中水蒸气的理由是
(3)按照如图装置进行实验时,首先进行的操作是 ,并要排净整套装置中的空气,则排净装置中空气的必要性是 ________。
(4)根据该实验中的 现象,可证明CO具有还原性。
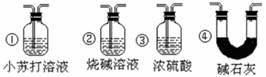
(5)若要根据装置F中石灰水变浑浊的现象确认CO具有还原性,应在上图装置 之间连接下图中的 装置(填序号)。
22.(共16分)物质A有如下图所示转化关系,其中乙为金属单质,F的溶液中只含有一种溶质;甲由两种单质直接化合得到;B 为红棕色固体; D 的水溶液加入用硝酸酸化的AgNO3溶液有白色沉淀生成。(有的反应可能在水溶液中进行,有的反应的生成物未全部给出,反应条件也未注明)。
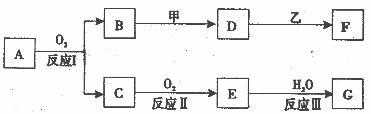
则:
①请写出反应I的化方程式____________________________________。
②已知1gC与氧气反应生成气态E,放出QkJ热量,请写出该反应的热化方程式:
__________________________________________。
③甲的化式为______________。
④ D和乙反应的离子方程式为__________________________________________。
⑤请简述检验G溶液中阴离子的方法 。
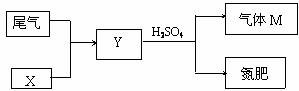
⑥工业上生产G物质过程中,G物质在________设备中产生,生产过程中产生的尾气M可如下图所示回收利用,请根据图示判断X是(填名称) ,写出Y与硫酸反应生成M的化方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com