
13£®·š¹ú»¯Ñ§ŒÒÒÁ·ò¡€Ð€Íò»ñ2005Äêŵ±Ž¶û»¯Ñ§œ±¡£Ëû·¢ÏÖÁËÏ©ÌþÀïµÄÌŒ-̌˫Œü»á±»²ðÉ¢¡¢ÖØ×飬ÐγÉзÖ×Ó£¬ÕâÖÖ¹ý³Ì±»ÃüÃûΪϩÌþžŽ·Öœâ·ŽÓŠ¡£Ï©ÌþžŽ·Öœâ·ŽÓŠ¿ÉÐÎÏóµØÃèÊöΪœ»»»Îè°é¡£(ÈçÍŒËùÊŸ)¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )

¡¡¡¡ Ï©ÌþžŽ·Öœâ·ŽÓŠÖеĎ߻¯ŒÁÊÇœðÊô¿š±ö(ÈçCH2==M)£¬œðÊô¿š±öÓëÏ©Ìþ·Ö×ÓÏàÓöºó£¬Áœ¶ÔÎè°é»áÔÝʱ×éºÏÆðÀŽ£¬ÊÖÀÊÖÌøÆðËÄÈËÎ赞¡£ËæºóËüÃÇ¡°œ»»»Îè°é¡±£¬×éºÏ³ÉÁœžöзÖ×Ó£¬ÆäÖÐÒ»žöÊÇеÄÏ©Ìþ·Ö×Ó£¬ÁíÒ»žöÊÇœðÊôÔ×ÓºÍËüµÄÐÂÎè°é¡£ºóÕß»áŒÌÐøÑ°ÕÒÏÂÒ»žöÏ©Ìþ·Ö×Ó£¬ÔَΡ°œ»»»Îè°é¡±¡£°ÑC6H5CH2CH==CH2ÓëCH2==MÔÚÒ»¶šÌõŒþÏ»ìºÏ·ŽÓŠ£¬ÏÂÁвúÎï²»¿ÉÄÜŽæÔÚµÄÊÇ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
A£®C6H5CH2CH==M ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®CH2= CH2
C£®C6H5CH2 ==CH2 C6H5 ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®C6H5CH2CH==CH CH2 C6H5
12£®ÄÜÕýÈ·±íÊŸÏÂÁзŽÓŠµÄÀë×Ó·œ³ÌÊœÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®ÂÈÆøžúË®·ŽÓŠ£ºCl2+H2O¡ú2H++Cl-+ClO-
¡¡¡¡¡¡ B£®ÁòËáÍÈÜÒºžúÇâÑõ»¯±µÈÜÒº·ŽÓŠ£ºBa2++SO2-4¡úBaSO4¡ý
¡¡¡¡¡¡ C£®±œ·ÓÄÆÈÜÒºÖÐÍšÈëÉÙÁ¿¶þÑõ»¯ÌŒ£º
¡¡¡¡¡¡¡¡¡¡¡¡ 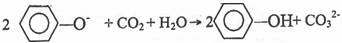
¡¡¡¡¡¡ D£®Áò»¯ÑÇÌúžúÑÎËá·ŽÓŠ£ºFeS+2H+¡úFe2++H2S¡ü
11£®ÈçÏÂÍŒ£¬a¡¢bÊÇÁœžùÌŒ°ô¡£ÒÔÏÂÐðÊö²»ÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
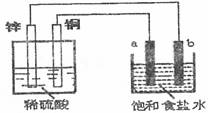
¡¡¡¡¡¡ A£®aÊÇÑôŒ«£¬µçŒ«·ŽÓŠÊœÎª2Cl--2e¡úCl2¡ü
¡¡¡¡¡¡ B£®ÍÉϲúÉúÎÞÉ«ÆøÌ壬aÉϲúÉúÓÐŽÌŒ€ÐÔÆøζµÄÆøÌå
C£®±¥ºÍʳÑÎË®ÖеΌӷÓ̪ÊÔÒºµÄÏÖÏó£ºbŒ«žœœüÈÜÒºÑÕÉ«±äºì£»ÉÕ±ÈÜÒºÖÐÀë×ÓµÄÅš¶È±ä»¯ÊÇ£ºC(Zn2+)±äŽó£¬C(H+)±äС
¡¡ ¡¡¡¡ D£®ÍƬÉϵĵ猫·ŽÓŠÊœÊÇ£ºCu2++2e¡úCu
10£®ÏÂÁО÷×éÀë×Ó£¬ÔÚÖž¶šµÄ»·Ÿ³ÖÐÒ»¶šÄÜŽóÁ¿¹²ŽæµÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡ ¡¡¡¡ A£®ÓÉË®µçÀë³öµÄC(H+)=1¡Á10-12mol£¯LµÄÈÜÒºÖУºI-¡¢Cl-¡¢HCO-3¡¢Na+
¡¡ ¡¡¡¡ B£®ÔÚÇ¿ËáÐÔÈÜÒºÖУºNa+¡¢S2-¡¢NO-3¡¢CO2-3
¡¡ ¡¡¡¡ C£®º¬ŽóÁ¿Fe3+ÈÜÒºÖУºK+¡¢Cl-¡¢NO-3¡¢Na+
¡¡ ¡¡¡¡ D£®ÔÚŒÓÈëÂÁ·ÛÄܲúÉúŽóÁ¿H2µÄÈÜÒºÖУºNH+4¡¢Fe2+¡¢SO2-4¡¢Cl-
9£®ÏÂÁÐÅÅÁÐ˳ÐòÕýÈ·µÄÊÇ¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ ¢Ù·Ðµã£ºH2S>H2O¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¢ÚÑõ»¯ÐÔ£ºCu2+>Fe3+>H+>Fe2+
¡¡ ¡¡¡¡ ¢ÛÔ×Ӱ럶£ºNa>Mg>O¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ ¢Ü»¹ÔÐÔ£ºF>Cl->S2-
¡¡ ¡¡¡¡ ¢ÝœáºÏH+µÄÄÜÁŠ£ºOH->CH3COO->Cl-
¡¡ ¡¡¡¡ A£®¢Ù¢Û¢Ü¡¡¡¡ ¡¡¡¡¡¡¡¡ B£®¢Ú¢Û¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ C£®¢Û¢Ý¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®¢Ú¢Û¢Ý
8£®Ò»¶šÌõŒþÏ£¬¿ÉÄæ·ŽÓŠC(s)+CO2(g) 2CO(g)-Q£¬ŽïµœÆœºâ׎̬£¬ÏÖœøÐÐÈçϲÙ×÷£º¢ÙÉýžß·ŽÓŠÌåϵµÄζȣ»¢ÚÔöŒÓ·ŽÓŠÎïcµÄÓÃÁ¿£»¢ÛËõС·ŽÓŠÌåϵµÄÌå»ý£º¢ÜŒõÉÙÌåϵÖÐCOµÄÁ¿¡£ÉÏÊöŽëÊ©ÖÐÒ»¶šÄÜʹ·ŽÓŠµÄÕý·ŽÓŠËÙÂÊÏÔÖøŒÓ¿ìµÄÊÇ(¡¡¡¡ )
2CO(g)-Q£¬ŽïµœÆœºâ׎̬£¬ÏÖœøÐÐÈçϲÙ×÷£º¢ÙÉýžß·ŽÓŠÌåϵµÄζȣ»¢ÚÔöŒÓ·ŽÓŠÎïcµÄÓÃÁ¿£»¢ÛËõС·ŽÓŠÌåϵµÄÌå»ý£º¢ÜŒõÉÙÌåϵÖÐCOµÄÁ¿¡£ÉÏÊöŽëÊ©ÖÐÒ»¶šÄÜʹ·ŽÓŠµÄÕý·ŽÓŠËÙÂÊÏÔÖøŒÓ¿ìµÄÊÇ(¡¡¡¡ )
¡¡ ¡¡¡¡ A£®¢Ù¢Ú¢Û¢Ü¡¡¡¡ ¡¡¡¡ B£®¢Ù¢Û¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ C£®¢Ü¢Ú¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®¢Ù¢Û¢Ü
7£®ÓÃNA±íÊŸ°¢·üŒÓµÂÂÞ³£ÊýµÄÖµ£¬ÏÂÁÐ˵·šÖÐÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®4gÖØË®(D2O)ÖÐËùº¬ÖÊ×ÓÊýΪ0.2NA
¡¡¡¡¡¡ B£®4.48L£¬N2ÓëCOµÄ»ìºÏÎïËùº¬·Ö×ÓÊýΪ0.2NA
¡¡¡¡¡¡ C£®º¬10.6gÈÜÖÊNa2CO3µÄÈÜÒºÖУ¬Ëùº¬ÑôÀë×Ó×ÜÊýΪŽóÓÚ0.2NA
¡¡¡¡¡¡ D£®12.5mL 16mol£¯l¡£ÅšÁòËáÓë×ãÁ¿Í·ŽÓŠ£¬×ªÒƵç×ÓÊýΪ0.2NA¡£
6£®ÏÂÁзŽÓŠÖÐÉú³ÉÎïµÄ×ÜÄÜÁ¿žßÓÚ·ŽÓŠÎï×ÜÄÜÁ¿µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®ÌŒËáÇâÄÆÊÜÈȷ֜⡡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ B£®ÇâÆøÈŒÉÕ
¡¡¡¡¡¡ C£®ÂÁÓëÑõ»¯Ìú·ÛÄ©·ŽÓŠ¡¡¡¡ ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ D£®Ñõ»¯žÆÈÜÓÚË®
5£®ÏÂÁÐÐðÊöÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡ ¡¡¡¡ A£®ÎÞÂÛÄÄÒ»ÖÖŸ§ÌåÖУ¬Ö»ÒªŽæÔÚÑôÀë×ÓŸÍÒ»¶šŽæÔÚÒõÀë×Ó
¡¡ ¡¡¡¡ B£®¶þÑõ»¯¹èÊÇÔ×ÓŒäÍš¹ý·ÇŒ«ÐÔ¹²ŒÛŒüÐγɵÄÔ×ÓŸ§Ìå
¡¡ ¡¡¡¡ C£®±ùÊÇË®·Ö×ÓŒäÍš¹ý·Ö×ÓŒä×÷ÓÃÁŠ¶øÓйæÔòÅÅÁгɵķÖ×ÓŸ§Ìå
¡¡ ¡¡¡¡ D£®ÈÛÈÚµÄÂÈ»¯ÄÆÄܵŒµçÊÇÒòΪÆäÁ£×ÓŒäŽæÔÚÀë×ÓŒü
4£®ÏÂÁÐÓйØ˵·šÖÐÕýÈ·µÄÊÇ¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡¡ (¡¡¡¡ )
¡¡¡¡¡¡ A£®¹¹³ÉH2O¡¢CCl4¡¢PCl5¡¢N2·Ö×ÓµÄÔ×Ó¶ŒÂú×ã×îÍâ²ã8µç×Ӝṹ
¡¡¡¡¡¡ B£®ÒÒ¶þŽŒ¡¢±ûÈýŽŒ¡¢±œŒ×ŽŒÊôÓÚͬϵÎï
¡¡¡¡¡¡ C£®HF¡¢SO2¡¢NH3¡¢H2O¶ŒÊÇÈõµçœâÖÊ
¡¡¡¡¡¡ D£®16O¡¢17O¡¢18OÊôÓÚͬλËØ
¹úŒÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·šºÍ²»ÁŒÐÅÏ¢ŸÙ±šÆœÌš | ÍøÉÏÓкŠÐÅÏ¢ŸÙ±š×šÇø | µçÐÅÕ©ÆŸÙ±š×šÇø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓкŠÐÅÏ¢ŸÙ±š×šÇø | ÉæÆóÇÖÈšŸÙ±š×šÇø
Î¥·šºÍ²»ÁŒÐÅÏ¢ŸÙ±šµç»°£º027-86699610 ŸÙ±šÓÊÏ䣺58377363@163.com