
17.(09Ē¶«ÄĻ)ijĶ¬Ń§ĪŖĮĖ²ā¶Ø»ĘĶŠ¼(ÓÉŠæŗĶĶŠĪ³ÉµÄŗĻ½š)ѳʷ×é³É£¬Č”ĖÄ·ŻŃłĘ··Ö±š¼ÓĻ”ĮņĖį·“Ó¦£¬Ę䏵Ń鏿¾Ż¼ĒĀ¼ČēĻĀ±ķ”£
|
ѳʷ |
µŚ1·Ż |
µŚ2·Ż |
µŚ3·Ż |
µŚ4·Ż |
|
Ȕѳʷ֏Įæ(g) |
50.0 |
50.0 |
50.0 |
50.0 |
|
Č”Ļ”ĮņĖįÖŹĮæ(g) |
40.0 |
80.0 |
120.0 |
160.0 |
|
²śÉśĘųĢåÖŹĮæ(g) |
0.4 |
0.8 |
1.0 |
1.0 |
ŹŌ¼ĘĖć£ŗ
¢Å¾·ÖĪö£¬ŌŚµŚ1·ŻŃłĘ·²āµĆµÄŹż¾ŻÖŠ£¬”””””””” (ĢīĪļÖŹ)ĶźČ«·“Ó¦ĮĖ”£(1·Ö)

¢ĘĮŠŹ½¼ĘĖć»ĘĶŠ¼ŃłĘ·ÖŠµÄŠæµÄÖŹĮæ·ÖŹżŗĶĖłÓĆĻ”ĮņĖįÖŠČÜÖŹµÄÖŹĮæ·ÖŹż”£(6·Ö)

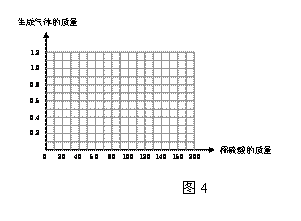 ¢ĒĒėŌŚĶ¼4ÖŠ»³öŌŚ50.0gѳʷ֊¼ÓĻ””” ĖįµÄÖŹĮæÓė²śÉśĘųĢåÖŹĮæ±ä»Æ¹ŲĻµµÄŹ¾ŅāĶ¼”£(1·Ö)””
¢ĒĒėŌŚĶ¼4ÖŠ»³öŌŚ50.0gѳʷ֊¼ÓĻ””” ĖįµÄÖŹĮæÓė²śÉśĘųĢåÖŹĮæ±ä»Æ¹ŲĻµµÄŹ¾ŅāĶ¼”£(1·Ö)”” 
””
19”¢(09ĮŁŅŹ)ĪŅ¹śŌ¼ŌŚÄĻ±±³ÆŹ±¾ĶæŖŹ¼Ņ±Į¶»ĘĶ”£»ĘĶŹĒĶŗĶŠæµÄŗĻ½š(Cu-Zn)£¬ĖüæÉÓĆĄ“ÖĘŌģ¼°Ę䔢µēĘ÷Įć¼ž¼°ČÕÓĆĘ·”£ĪŖĮĖ²ā¶Øij»ĘĶѳʷ֊ŠæµÄÖŹĮæ·ÖŹż(²»æ¼ĀĒ»ĘĶÖŠµÄĘäĖūŌÓÖŹ)£¬ĻÖ½«15mLĻ”ŃĪĖį·ÖČż“Ī¼ÓČėµ½5g»ĘĶѳʷ·ŪÄ©ÖŠ£¬Ćæ“Ī³ä·Ö·“Ó¦ŗ󣬲ā¶ØÉś³ÉĒāĘųµÄÖŹĮ棬ŹµŃ鏿¾Ż¼ūĻĀ±ķ£ŗ
|
”” |
µŚŅ»“Ī |
µŚ¶ž“Ī |
µŚČż“Ī |
|
¼ÓČėĻ”ŃĪĖįµÄĢå»ż(mL) |
5 |
5 |
5 |
|
Éś³ÉĒāĘųµÄÖŹĮæ(g) |
0.04 |
m |
0.02 |
ŹŌĒó£ŗ
(1)”””””” m=”””””””” ”””””£
(2)“Ė»ĘĶѳʷ֊ŠæµÄÖŹĮæ·ÖŹżŹĒ¶ąÉŁ£æ
34£®(09¼ĪŠĖ)ijĶ¬Ń§·¢ĻÖ½šŹōŃŪ¾µ¼Ü±ķĆę¾³£»įÓŠĀĢÉ«ĪļÖŹ²śÉś£¬ÕāŹĒŹ²Ć“ĪļÖŹÄŲ?ĖūŗĶĶ¬Ń§ĆĒŹÕ¼Æ»żĄŪĮĖŅ»¶ØĮæµÄÕāÖÖĀĢÉ«ĪļÖŹ£¬·ÅŌŚŹŌ¹ÜĄļøō¾ųæÕĘų¼ÓČČ”£¹Ū²ģµ½ŹŌ¹ÜÄŚ±ŚÓŠĖ®Ö飬ĀĢÉ«ĪļÖŹ±ä³ÉŗŚÉ«·ŪÄ©£¬²śÉśµÄĘųĢåÄܹ»Ź¹³ĪĒåŹÆ»ŅĖ®±ä»ė×Ē”£
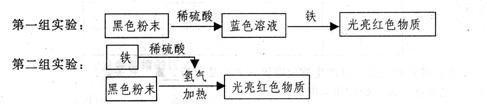 (1)ŹµŃé±ķĆ÷£ŗ¾µ¼ÜÉĻµÄĀĢÉ«ĪļÖŹÖŠŅ»¶Øŗ¬ÓŠ ”””ų”” ŌŖĖŲ”£¾µ¼ÜÉĻ»į²śÉśĀĢÉ«µÄŠā£¬ÕāĀĢÉ«ĪļÖŹÖŠŹĒ·ńŗ¬ÓŠĶÄŲ?Ķ¬Ń§ĆĒÓĆÉĻŹöŹŌ¹ÜÖŠµÄŗŚÉ«·ŪÄ©·ÖĮ½×é·Ö±š½ųŠŠĮĖŹµŃé£ŗ
(1)ŹµŃé±ķĆ÷£ŗ¾µ¼ÜÉĻµÄĀĢÉ«ĪļÖŹÖŠŅ»¶Øŗ¬ÓŠ ”””ų”” ŌŖĖŲ”£¾µ¼ÜÉĻ»į²śÉśĀĢÉ«µÄŠā£¬ÕāĀĢÉ«ĪļÖŹÖŠŹĒ·ńŗ¬ÓŠĶÄŲ?Ķ¬Ń§ĆĒÓĆÉĻŹöŹŌ¹ÜÖŠµÄŗŚÉ«·ŪÄ©·ÖĮ½×é·Ö±š½ųŠŠĮĖŹµŃé£ŗ
(2)“ó²æ·ÖĶ¬Ń§ČĻĪŖµŚŅ»×鏵Ńé·½·Ø±Č½ĻĄķĻė£¬ŹŌ¼ņŅŖĖµĆ÷ĄķÓÉ”£ ”””ų””
26.(10·Ö)
(1) 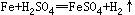 (2)2.8g
(2)2.8g
(3)ÓɱķÖŠŹż¾Ż·ÖĪö£¬ŹµŃé¢óÖŠ100gĻ”ĮņĖįĶźČ«·“Ó¦”£
É菵Ńé¢óÉś³ÉĮņĖįŃĒĢśµÄÖŹĮæĪŖx£¬ĻūŗÄĢśµÄÖŹĮæĪŖy”£
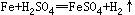
56”””””””” 152”” 2
y”””””””””” x”””” 0.2g
=£¬x=15.2g”””” =,y=5.6g
ĖłµĆČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżĪŖ”Į100%=14.4%”£
“š£ŗĀŌ”£
.
26£®(09Ī«·»)(10·Ö)ij»Æѧµ÷²éŠ”×éµÄĶ¬Ń§µ½øÖĢś³§×öÉē»įµ÷²é”£ĖūĆĒ³éČ”×é³ÉĶźČ«ĻąĶ¬µÄÖŹĮæĪŖ2.84g”¢4.26g”¢6.23gµÄČż·ŻøÖŃł(¼ŁÉčøÖŃłÖŠÖ»ŗ¬ĢśŗĶĢ¼)£¬·Ö±š¼ÓČė100gĻ”ĮņĖįÖŠ½ųŠŠŹµŃé(ŹµŃéI”¢¢ņ”¢¢ó)£¬³ä·Ö·“Ó¦ŗ󣬽«µĆµ½µÄŹµŃ鏿¾Ż»ęÖĘ³öČēĻĀĶ¼Ļń£ŗ
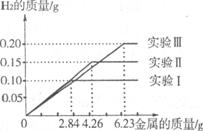 ŹŌ»Ų“š(¼ĘĖć½į¹ū¾«Č·µ½0. 1%)£ŗ
ŹŌ»Ų“š(¼ĘĖć½į¹ū¾«Č·µ½0. 1%)£ŗ
(1)Š“³öŹµŃéÖŠÓŠ¹ŲµÄ»Æѧ·½³ĢŹ½£ŗ
(2)ŹµŃéIÖŠĢś²Ī¼Ó·“Ó¦µÄÖŹĮæĪŖ”””””””””” ”£
(3)Ļ”ĮņĖįĶźČ«²Ī¼Ó·“Ó¦µÄŹµŃéÖŠ£¬·“Ó¦ŗóČÜŅŗÖŠČÜÖŹµÄÖŹĮæ·ÖŹżŹĒ¶ąÉŁ”£
30£®(1) Mg+H2SO4£½MgSO4+H2”ü””(2) Cu”” 5”” 2.5”” (3) 80%”””” (4) 20.4%
30£®(09Ģ©ÖŻ)(8·Ö)ij»ÆѧŠĖȤŠ”×éĪŖĮĖ²ā¶ØĆ¾ĶŗĻ½šÖŠĆ¾µÄÖŹĮæ·ÖŹż£¬Č”³ö3gŗĻ½šŃłĘ·£¬½«60gĻ”ĮņĖį·Ö6“Ī¼ÓČėѳʷ֊£¬³ä·Ö·“Ó¦ŗó¹żĀĖ”¢Ļ“µÓ”¢øÉŌļ”¢³ĘÖŲ£¬µĆµ½µÄŹµŃ鏿¾ŻČēĻĀ£ŗ
|
Ļ”ĮņĖįÓĆĮæ |
Ź£Óą¹ĢĢåÖŹĮæ |
|
µŚŅ»“Ī¼ÓČė10g |
mg |
|
µŚ¶ž“Ī¼ÓČė10g |
2.0g |
|
µŚČż“Ī¼ÓČė10g |
1.5g |
|
µŚĖÄ“Ī¼ÓČė10g |
1.0g |
|
µŚĪå“Ī¼ÓČė10g |
0.6g |
|
µŚĮł“Ī¼ÓČė10g |
0.6g |
(1)²ā¶Ø¹ż³ĢÖŠ·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ”” ”””””ų”””””” £»
(2)“ÓŅŌÉĻŹż¾ŻæÉÖŖ£¬×īŗóŹ£ÓąµÄ0.6g¹ĢĢåµÄ³É·ÖŹĒ”” ”””ų ””””£»ÕāĮł“ĪŹµŃéÖŠ£¬µŚ ”””ų”” “Ī¼ÓČėĻ”ĮņĖįŹ±ŃłĘ·ÖŠµÄĆ¾ŅŃ¾ĶźČ«·“Ó¦£»±ķøńÖŠ£¬m=”” ”””ų”” ”””£
(3)¼ĘĖćŗĻ½šŃłĘ·ÖŠĆ¾µÄÖŹĮæ·ÖŹż”£
(4)¼ĘĖćĖłÓĆĻ”ĮņĖįÖŠH2SO4µÄÖŹĮæ·ÖŹż”£
29£®(1) B”” O2»ņŃõĘų”” H2O»ņĖ®””(2) 2Cu+O2+H2O+CO2 ===Cu2(OH)2CO3
(3) [²éŌÄ׏ĮĻ]CO32-”” Cu2+”” ŗŚ””ÓŠĖ®Öé
[·“Ė¼ÓėĶŲÕ¹]
¢Ł½«²śÉśµÄĘųĢåĶØČė×ćĮæµÄ³ĪĒåŹÆ»ŅĖ®ÖŠ
¢ŚĖ®»ņ¶žŃõ»ÆĢ¼
¢ŪĶæÓĶ”¢ĘįµČ
24£®(09Ģ©ÖŻ)(6·Ö)AŹĒ³£¼ū½šŹōµ„ÖŹ£¬B”¢CŹĒ·Ē½šŹōµ„ÖŹ£¬ĒŅCŹĒĆܶČ×īŠ”µÄĘųĢ壬¼×ŹĒ“ÅĢśæóµÄÖ÷ŅŖ³É·Ö£¬ŅŅŹĒĪŽÉ«ŅŗĢ壬ĖüĆĒÖ®¼äÓŠČēĻĀµÄ×Ŗ»Æ¹ŲĻµ(²æ·Ö²śĪļŗĶ·“Ó¦Ģõ¼žĪ“±źĆ÷)”£
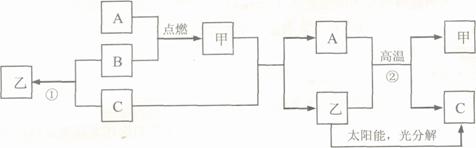
”” (1)ĶʶĻC”¢¼×”¢ŅŅµÄ»ÆѧŹ½ĪŖ£ŗC”” ”ų ””””£¬¼×”” ”ų ””””£¬ŅŅ”” ”ų ””””£»
”” (2)Š“³ö·“Ó¦¢ŚµÄ»Æѧ·½³ĢŹ½”””””””””””””” ”ų ””””””””””””””£»
”” (3)Š“³ö·“Ó¦¢ŁµÄ»Æѧ·½³ĢŹ½”””””””””””””” ”ų ””””””””””””””£¬øĆ·“Ó¦³żĮĖ¾ßÓŠ·Å³öČČĮæ¶ą£¬ŌĮĻ²»ŹÜĻŽÖʵÄÓŵćĶā£¬»¹ÓŠ”””” ”ų ””””µÄÓÅµć”£
|
(3) 2H2+O2 === 2H2O”” ²śĪļĪŽĪŪČ¾
(09Ģ©ÖŻ)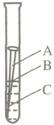 29£®(11·Ö)øÖĢś”¢ĀĮŗĻ½š”¢ĶÖĘĘ·µČŹĒÓ¦ÓĆ¹ć·ŗµÄ½šŹō²ÄĮĻ”£¾Ż¹Ą¼Ę£¬ĆæğȫŹĄ½ē±»øÆŹ“ĖšŗĵÄøÖĢś²ÄĮĻ£¬Ō¼Õ¼Č«ÄźøÖ²śĮæµÄŹ®·ÖÖ®Ņ»”£Ä³Š£»ÆѧŠĖȤŠ”×éµÄĶ¬Ń§Ģ½¾æ½šŹōøÆŹ“µÄŌŅņ£¬Éč¼ĘČēĻĀŹµŃé£ŗ
29£®(11·Ö)øÖĢś”¢ĀĮŗĻ½š”¢ĶÖĘĘ·µČŹĒÓ¦ÓĆ¹ć·ŗµÄ½šŹō²ÄĮĻ”£¾Ż¹Ą¼Ę£¬ĆæğȫŹĄ½ē±»øÆŹ“ĖšŗĵÄøÖĢś²ÄĮĻ£¬Ō¼Õ¼Č«ÄźøÖ²śĮæµÄŹ®·ÖÖ®Ņ»”£Ä³Š£»ÆѧŠĖȤŠ”×éµÄĶ¬Ń§Ģ½¾æ½šŹōøÆŹ“µÄŌŅņ£¬Éč¼ĘČēĻĀŹµŃé£ŗ
(1)ČēĶ¼£¬Č”Ņ»øłŌ¼10cmµÄ¹āĮĮĢś¶¤·ÅŌŚ×ŌĄ“Ė®ÖŠ£¬¹Ū²ģA”¢B”¢CČż“¦µÄ±ä»Æ”£
¼øĢģŗó£¬ĖūĆĒ»į·¢ĻÖ”””ų””“¦×īĻČ³öĻÖĢśŠā£¬“ó¼Ņ½įŗĻŹé±¾ÖŖŹ¶ÖŖµĄ£¬ĢśŌŚæÕ
ĘųÖŠÉśŠāŹµ¼ŹŹĒĢśŗĶ”””ų”” ”””¢”” ”””ų””µČĪļÖŹĻą»„×÷ÓĆ·¢ÉśŅ»ĻµĮŠø“ŌÓµÄ
»Æѧ·“Ó¦µÄ¹ż³Ģ”£
””(2)Ņ»Ķ¬Ń§ĮŖĻėµ½¼ŅĄļĶÖĘ²Ķ¾ßÉĻÓŠŅ»²ćĀĢÉ«ĪļÖŹ£¬ČĻĪŖĶŌŚæÕĘųÖŠŅ²»įÉśŠā”£ĖūĆĒÉĻĶų²éŌÄ׏ĮĻ£¬ÖŖµĄÕāÖÖĀĢÉ«ĪļÖŹµÄ»Æѧ³É·ÖĪŖCu2(OH)2CO3(ĶĀĢ)”£ĖūĆĒ“ÓĶĀĢ×é³ÉŗĶæÕĘųµÄ³É·Ö“óµØ²Ā²ā£¬ĶÉśŠā³żĮĖÓėĢśÉśŠāĢõ¼žĻąĶ¬Ķā£¬»¹Ó¦øĆÓŠCO2²Ī¼Ó·“Ó¦”£
”” ĒėŠ“³öĶŌŚæÕĘųÖŠÉś³ÉĶĀĢµÄ»Æѧ·½³ĢŹ½”””””””ų ”””””” ”£
(3)[²éŌÄ׏ĮĻ]æ×ČøŹÆµÄÖ÷ŅŖ³É·ÖŹĒCu2(OH)2CO3£¬Ņ²æÉŅŌ±ķŹ¾³ÉCuCO3”¤Cu(OH)2”£
”” Óėæ×ČøŹÆĻąĖĘ£¬»¹ÓŠŠķ¶ąæóĪļæÉÓĆxCuCO3”¤yCu(OH)2(x”¢y¶¼ŹĒÕżÕūŹż)±ķŹ¾£¬ŹÆĒą
”” ¾ĶŹĒĘäÖŠµÄŅ»ÖÖ”£
”” [ŹµŃéĢ½¾æ]ĪŖĮĖŃéÖ¤ŹÆĒąµÄ×é³É³É·Ö£¬ĖūĆĒÉč¼ĘĮĖČēĻĀŹµŃ飬ĒėÄć¹²Ķ¬²ĪÓėĢ½¾æ”£
|
”” |
ŹµŃé²Ł×÷ |
ŹµŃéĻÖĻó |
½įĀŪ |
|
”” ²½Öčl ”” |
ȔɣĮæŹÆĒąŃłĘ·ÖĆÓŚ“óŹŌ¹ÜÖŠ¼ÓČė×ćĮæĻ”ĮņĖį |
(1)²śÉś“óĮæĘųĢå (2)ČÜŅŗ³ŹĄ¶É« |
(1)ŹÆĒąÖŠŗ¬ÓŠ””
”ų””
Ąė×Ó (2)ŹÆĒąÖŠŗ¬ÓŠ”” ”ų”” Ąė×Ó |
|
”” ²½Öč2 ”” |
ȔɣĮæŹÆĒąŃłĘ·ÖĆÓŚ“óŹŌ¹ÜÖŠ¼ÓČČ |
(1)²ŠĮō¹ĢĢå³Ź”” ”ų”” É« (2)“óŹŌ¹ÜÄŚ±Ś”” ”ų”” |
”” ŹÆĒą¼ÓČČŅ×·Ö½ā ”” |
[·“Ė¼ÓėĶŲÕ¹]
¢ŁČ·¶Ø²½Öč1ÖŠ²śÉśĘųĢå³É·ÖµÄŹµŃé·½·ØŹĒ”””””””””””” ”ų”””””””””””” ”£
¢Śøł¾ŻŅŌÉĻĢ½¾æ£¬Ö»ŅŖ²ā¶Ø³ö²Ī¼Ó·“Ó¦µÄŹÆĒąµÄÖŹĮæ”¢Éś³ÉµÄŃõ»ÆĶµÄÖŹĮæŗĶ”” ”ų”” µÄÖŹĮ棬¾ĶæÉČ·¶ØŹÆĒąµÄ»ÆѧŹ½(¼“Č·¶Øx”¢yµÄÖµ)”£
¢Ū·ĄÖ¹½šŹōŠāŹ“µÄ·½·Øŗܶą£¬ČēÖĘ³É²»ŠāøÖ”¢ŌŚ½šŹō±ķĆę”””””” ”ų”””””” (ČĪŠ“Ņ»ÖÖ·½·Ø)”£
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com