
|
|
A |
||
|
G |
E |
D |
B |
|
|
F |
|
C |
23.“椅子形状”的图包含了元素周期表前四周期的部分元素,其中A、B、C、D四种元素原子序数之和为77。
(1)写出A、B、C的价电子构型的电子排布式 。
(2)G原子的最外层电子占有 种能量不同的轨道。
(3)F形成的气态氢化物的电子式 。E和F简
单气态氢化物的稳定性较强的是 (写化学式)。
(4)A、B两元素都可以与氧元素形成化合物OA2、B2O,其分子的空间构型为折线型分子,对它们分子极性的判断正确的是( )。
a.都为非极性分子 b.都为极性分子 c.无法确定
在两种化合物中元素A、B的化合价分别为A ,B 。
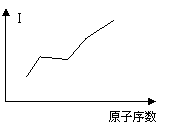 (5)气态原子失去一个电子所需要吸收的
(5)气态原子失去一个电子所需要吸收的
能量叫做第一电离能(I)。G、E、D、B四种
原子的第一电离能大小变化如右图所示:
同一周期元素的气态原子的第一电离能
与原子半径的关系 。
22.将2.4g Fe、Mg合金投入到一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体VL(硝酸被还原成NO),若向反应后的溶液中加入足量的NaOH溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为3.6g。则收集到的气体体积V的值可能为( )。
A.0.896 B.1.10 C. 1.69 D. 2.24
第Ⅱ卷(共84分)
21.氯酸钾和亚硫酸氢钾能发生氧化还原反应:ClO3-+HSO3--SO42-+Cl-+H+(未配平)。已知该反应的速率随c(H+)的增大而加快。下图为用ClO3-在单位时间内物质的量浓度变化表示的该反应v-t图。下列说法中不正确的是( )。
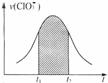 A.反应开始时速率增大可能是c(H+)所致
A.反应开始时速率增大可能是c(H+)所致
B.后期反应速率下降的主要原因是反应物浓度减小
C.纵坐标为v (H+)的V-t曲线与图中曲线完全重合
D.图中阴影部分“面积”可以表示t1-t2时间为n(Cl-)增加
20.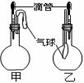 如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响)。则所用试剂分别可能依
如图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都有明显地胀大(忽略液体体积对气球的影响)。则所用试剂分别可能依 次是( )。
次是( )。
A.甲:铝粉和浓NaOH溶液 乙:饱和NaCl溶液和Cl2
B.甲:双氧水和MnO2 乙:NaOH溶液和CO2
C.甲:浓氨水和碱石灰 乙:浓氨水和SO2
D.甲:水和CO2 乙:水和氯化氢
19.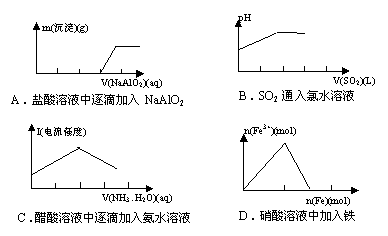 下列实验过程中产生的现象与对应的图形相符的是( )。
下列实验过程中产生的现象与对应的图形相符的是( )。
18.下列反应中离子方程式书写正确的是( )。
A.在稀氨水中通入过量CO2:NH3·H2O+CO2→NH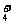 +HCO
+HCO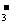
B.Na2CO3溶液中滴加盐酸至刚好出现气泡时:CO32-+2H+→ CO2↑+H2O
C.Ba(OH)2溶液滴加入到NaHSO4溶液中至溶液呈中性:
Ba2+ + OH- + H+ +SO42-→BaSO4↓+ H2O
D.向碳酸氢钙溶液中加入过量氢氧化钠:Ca2++2HCO3-+2OH-→ CaCO3↓+2H2O+CO32-
17.把一定量的铁和硫化亚铁的混合物与100 mL 2 mol/L的硫酸充分反应后,固体完全溶解,同时生成气体Y 3.36L(在标准状况下)。将反应后的溶液稀释到1 L,测得溶液的pH=1,则下列叙述一定正确的是( )。
A.气体Y是H2 B.气体Y中H2和H2S的体积比为1:2
C.反应中共消耗混合物10g D.反应中转移电子小于0.3 mol
16.下列说法中,错误的是( )。
A.在0.1 mol·L-1的氢氟酸中加入适量的蒸馏水,溶液中c(OH-)减小
B.室温下,CH3COOH分子可以存在于酸性、碱性、中性溶液中
C.在由水电离出的c(OH-)=1×10-12 mol·L-1的溶液中,NH4+可能大量存在
D.在NaAlO2溶液中 ,NaHCO3不可能大量存在
,NaHCO3不可能大量存在
15.铁在下列四种情况中腐蚀速率判断正确的是( )。
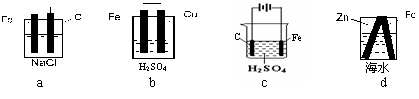
A.a>b>c>d B.b>a>d>c C.d>c>b>a D.b>d>a>c
14.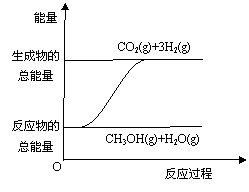 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气
的两种反应原理是:
①CH3OH(g)+H2O(g)→CO2(g)+3H2(g)-49.0 kJ
②CH3OH(g)+1/2O2(g)→CO2(g)+2H2(g)+192.9 kJ
下列说法不正确的是( )。
A.反应①中的能量变化如右图所示
B.从①和②中看出:物质的量相同的H2O(g)所具有的能量低于O2(g)
C.1molCH3OH与H2O(g)完全反应要吸收49.0kJ能量
D.根据②推知反应:CH3OH(l)+1/2O2(g)→CO2(g)+2H2(g)+Q , Q<192.9kJ
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com