
5.仅根据下列哪组数据,可以计算月球与地球间距离 ( )
A.月球的质量和地球的质量
B.月球绕地球公转周期、地球同步卫星的轨道半径和周期
C.月球绕地球公转周期和地球的半径
 D.地球的半径、地球表面的重力加速度
D.地球的半径、地球表面的重力加速度
4.氢原子的核外电子从第3能级跃迁到2能级时,辐射出的光照到某金属上时恰能产生光电效应现象。那么,很多处于第4能级的氢原子向低能级跃迁时,辐射出各种频率的光。其中有几种频率的光可能使这种金属发生光电效应 ( )
A.3种 B.4种 C.5种 D.6种
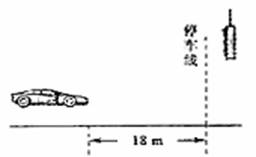 1.如图所示,以8m/s匀速行驶的汽车即将通过路口,绿灯还有2s将熄灭,此时汽车距离停车线18m。该车加速时加速度大小为2m/s2,减速时加速度大小为5m/s2。此路段允许行驶的最大速度为12.5m/s,下列说法中正确的是 ( )
1.如图所示,以8m/s匀速行驶的汽车即将通过路口,绿灯还有2s将熄灭,此时汽车距离停车线18m。该车加速时加速度大小为2m/s2,减速时加速度大小为5m/s2。此路段允许行驶的最大速度为12.5m/s,下列说法中正确的是 ( )
A.如果立即做匀加速运动,在绿灯熄灭前汽车可能通过停车线
B.如果立即做匀加速运动,在绿灯熄灭前通过停车线汽车一定超速
C.如果距停车线5m处减速,汽车能停在停车线处
D.如果立即做匀减速运动,在绿灯熄灭前汽车一定不能通过停车线
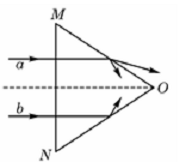 2.如图为玻璃等腰三棱镜的横截面。a、b两束可见单色光从空气垂直射入棱镜底面MN,在棱镜侧面OM、ON上反射和折射的情况如图所示。由此可知 ( )
2.如图为玻璃等腰三棱镜的横截面。a、b两束可见单色光从空气垂直射入棱镜底面MN,在棱镜侧面OM、ON上反射和折射的情况如图所示。由此可知 ( )
A.棱镜内a光的传播速度比b光的小 B.a光的频率比b光的高
C.棱镜内a光的传播速度比b光的大 D.a光的波长比b光的长
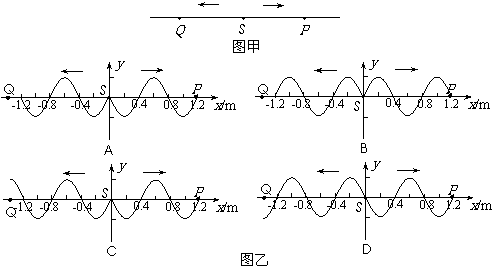
3.如图甲所示,波源S的起振方向向 上,振动频率f=100Hz,产生的简谐波分别沿水平方向左右传播,波速v=80m/s,在波的传播方向上有P、Q两点。已知SP=1.2m,SQ=1.4m。如图乙所示,波刚好传播到p点时波形图正确的是 ( )
12.(13分)有机物 是合成高分子化合物HPMA的中间体,HPMA
可用于锅炉阻垢剂。
(1)有机物A能够发生的反应有: (填写字母)
a.取代反应 b.加成反应 c.消去反应 d.酯化反应
(2)有面物A在Cu做催化剂和加热条件下,与氧气反应生成有机物B。B中含有的官能团除-Cl以外,还含有的官能团是: (写名称和结构简式)
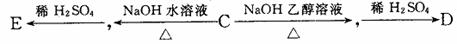 (3)有机物B经氧化后生成有机物C,C可有如下图所示的转化关系:
(3)有机物B经氧化后生成有机物C,C可有如下图所示的转化关系:
写出E的结构简式: ;
(4)D在高温、高压和催化剂作用下反应生成HPMA写出反应的化学方程式:
;
(5)F是E的一种同分异构体。0.1molE与足量NaHCO3反应放出2.24LCO2(标准状况下);0.1molF与足量金属Na反应放出3.36LH2(标准状况下);F能发生银镜反应。F的结构简式可能是: 。
11.(16分)中学化学常见的物质A、B、C、D之间存在如下转化关系:A+B→C+D+H2O(没
有配平)。请按要求填空:
(1)若A为短周期元素组成的黑色固体单质,与B的浓溶液共热时,产生C、D两种气体。C、D两种气体均能使澄清石灰水变浑浊,则该反应的化学方程式是
,鉴别这两种气体不能选用的试剂是 。
a.BaCl2溶液 b.KMnO4溶液
c.品红溶液 d.酸化的Ba(NO3)2溶液
向500mL2mol/L的NaOH溶液中通入0.8mol无色无味的C气体,恰好完全反应,该反应的化学方程式是 。此时溶液中的离子按照浓度由大到小排列的顺序是 。
(2)若A为红色金属单质,与适量B的溶液在常温下恰好完全反应,生成的无色气体C遇空气迅速变成经棕色。若被还原的B物质的量为2mol时,间生C气体的体积是
L(标况)。将生成的红棕色气体通入一个烧瓶里,塞紧瓶塞后,将烧瓶浸入冰水中,烧瓶中气体的颜色变浅,请用化学方程式和必要的文字解释颜色变化的原因 。
(3)若A在水中的溶解度随温度的升高而降低;B为短周期非金属单质;D是漂白粉的成分之一。C发生水解反应的离子方程式是
。
(4)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,受热易分解,分解后生成两种极易溶于水的气体。检验A中阴离子的方法是
 (简述操作过程及结论)。
(简述操作过程及结论)。
9.(14分)现有A、B、C、D四种元素,其原子序数依次递增。已知,A、C短周期非金属元素,其单质在常温下均为气体。两单质混合见光瀑炸生成AC,AC溶液显强酸性。B、D为金属元素,B的原子序数为D的一半。D与C2和AC溶液反应分别得DC3和DC2,烧碱溶液不能与D单质反应,而能与B单质反应。请回答下列问题:
(1)C的原子结构示意图为 ;B在周期表中的位置是 。
(2)用电子式表示AC的形成过程 。
(3)写出B单质与NaOH溶液反应的离子方程式 。
(4)电浮选凝聚法是工业上采用的一种污水处理方法。右图
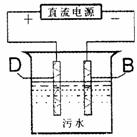 是该方法处理污水的实验装置示意图(B、D金属单质作
是该方法处理污水的实验装置示意图(B、D金属单质作
电极)。实验过程中,污水的pH始终保持在5.0~6.0之间。
接通电源后,阴极产生的气体将污物带到水面形成浮渣而
刮去,起到浮选净化作用;阳极产生的沉淀具有吸附性,
吸附污物而沉积,起到凝聚净化作用。阳极的电极
反应有两个,分别是2H2O-4e-=4H++O2↑,和
。阳极区生成沉淀的离子方程式是
。
(5)一定条件下,2molB与3molD的氧化物W恰好反应,则W的化学式为 。
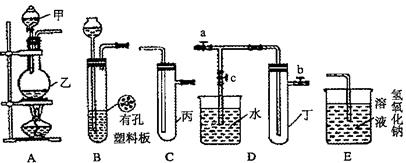 10.(17分)某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
10.(17分)某化学兴趣小组的同学利用下图所示实验装置进行实验(图中a、b、c表示止水夹)。
请按要求填空:
(1)A装置中仪器的名称为:甲是 ,乙是 。
(2)A、C、E相连后的装置可用于制取Cl2并进行相关的性质实验。
①写出实验室制取Cl2的反应方程式。
。
②若在丙中加入适量水,即可制得氯水。将所得氯水分成两份,进行I、II两个实验,实验操作、现象、结论如下:
|
实验序号 |
实验操作 |
现象 |
结论 |
|
I |
将氯水滴入品红溶液 |
溶液褪色 |
氯水与水反应的产物有漂白性 |
|
II |
氯水中加入NaHCO3粉末 |
有无色气泡产生 |
氯气与水反应的产物具有较强的酸性 |
请你评价实验I、II的结论是否合理?若不合理,请说明理由:
。
③请利用上述装置设计一个简单的实验,用来验证Cl-和Br-的还原性强弱。(分别指出甲、乙、丙中盛装的试剂、实验现象及结论)
。
(3)B、D、E装置相连后,在B中盛装浓硝酸和铜片(放在有孔塑料板上),可制得NO2并进行有关实验。
①B中发生反应的离子方程式为 。
②欲用D装置验证NO2与水的反应,其操作步骤为:先关闭止水夹 ,(填字母,下同)再打开止水夹 ,使烧杯中的水进入试管丁的操作是 。
③利用B装置还可制取的气体有 (写出两种即可)。
8.某氯化镁溶液的密度为dg/cm3,其中镁离子的质量分数为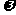 ,amL该溶液的Cl-的物质的量为 ( )
,amL该溶液的Cl-的物质的量为 ( )
A.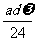 mol B.
mol B.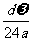 mol C.
mol C.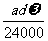 mol D.
mol D.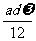 mol
mol
5.常温下,浓度为0.1mol/L的一元酸HA溶液的pH=2.0,浓度为0.1mol/L的一元碱BOH溶液中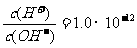 。将此两种溶液等体积混合后,所得溶液中离子浓度大小关系正确的是 ( )
。将此两种溶液等体积混合后,所得溶液中离子浓度大小关系正确的是 ( )
A.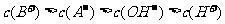
B.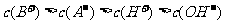
C.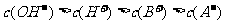
D.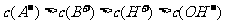
 6.T°C时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(I)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(II)所示,则下列结论正确的是 ( )
6.T°C时,A气体与B气体反应生成C气体。反应过程中A、B、C浓度变化如图(I)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(II)所示,则下列结论正确的是 ( )
A.在(t1+10)min时,保持其他条件不变,增大压强,平衡向逆反应方向移动
B.其他条件不变,升高温度,正、逆反应速率增大,且A的转化率增大
C.T°C时,在相同容器中,若由0.4mol/LA 、0.4mol/LB、0.2mol/LC反应,达到平衡后,C的浓度也为0.4mol/L
D.(t1+10)min时,保持压强不变,通入稀有气体,平衡不移动
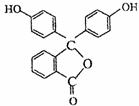 7.酚酞的结构简式如左图,下列关于酚酞的说法一定正确的
7.酚酞的结构简式如左图,下列关于酚酞的说法一定正确的
是 ( )
A.酚酞的分子式是C20H12O4
B.分子中的所有碳原子不在同一平面
C.1mol酚酞最多可能消耗2molNaOH
D.1mol酚酞可与10molH2加成
4.一种科学、简便的检测司机是否酒后驾车的方法是:使驾车人呼出的气体接触载有硫酸酸化处理的三氧化铬(CrO3)的硅胶,如果呼出的气体中有乙醇蒸气,乙醇就会被氧化成乙醛,同时三氧化名铬被还原为硫酸铬Cr2(SO4)3。下列说法不正确的是 ( )
A.CrO3和Cr2(SO4)3的颜色不同
B.CrO3中铬元素的化合价为+6
C.生成1mol的Cr2(SO4)3时,发生转移的电子为6mol
D.CrO3与稀盐酸反应只生成Cr2(SO4)3和水
3.下列各组离子在溶液中能大量共存,且加入过量NaOH溶液或过量稀盐酸均能得到澄清溶液的是 ( )
A.Al3+、Na+、SO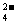 、NO
、NO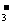 B.Ca2+、Mg2+、HCO
B.Ca2+、Mg2+、HCO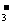 、NO
、NO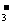
C.Fe2+、K+、SO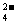 、Cl- D.K+、Na+、SiO
、Cl- D.K+、Na+、SiO 、ClO-
、ClO-
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com