
|
|
酸性氧化物 |
碱性氧化物 |
|
定 义 |
凡能与碱反应生成盐和水的氧化物 大多数非金属氧化物是酸性氧化物 大多数酸性氧化物是非金属氧化物 |
凡能与酸反应生成盐和水的氧化物 大多数金属氧化物是碱性氧化物 所有碱性氧化物是金属氧化物 |
|
化 学 性 质 |
(1)大多数可与水反应生成酸 CO2+H2O== H2CO3 SO2+H2O== H2SO3 SO3+H2O== H2SO4 |
(1)少数可与水反应生成碱 Na2O +H2O== 2NaOH K2O +H2O== 2KOH BaO +H2O== Ba(OH)2 CaO +H2O== Ca(OH)2 |
|
(2) 酸性氧化物+碱 → 盐+水 CO2 +Ca(OH)2== CaCO3↓+H2O (不是复分解反应) |
(2) 碱性氧化物+酸 → 盐+水 Fe2O3+6HCl== 2FeCl3+3H2O |
2、碱的通性(具有通性的原因:__________________________________________________)
(1)碱溶液与酸碱指示剂的反应: 使紫色石蕊试液变_______色,使无色酚酞试液变__________色
(2)酸性氧化物+碱 → 盐+水 如:______________________________________________
(3)酸+碱 → 盐+水 如:________________________________________________
注:①难溶性碱受热易分解(不属于碱的通性) 如Cu(OH)2 ΔCuO +H2O 2Fe(OH)3 ΔFe2O3+3H2O
②常见沉淀:AgCl↓ BaSO4↓ Cu(OH)2↓ F e(OH)3↓ Mg(OH)2↓ BaCO3↓ CaCO3↓
1、氢氧化钠、氢氧化钙的物理性质、用途
|
|
氢氧化钠 |
氢氧化钙 |
|
颜色、状态 |
________色体,______溶于水(溶解放热) |
________色粉末,_________溶于水 |
|
俗名 |
________________________(具有强腐蚀性) |
____________________________ |
|
制法 |
Ca(OH)2+Na2CO3==
CaCO3↓+2NaOH |
CaO +H2O== Ca(OH)2 |
|
用途 |
①氢氧化钠固体作_________剂 ②化工原料:制肥皂、造纸 ③去除油污:炉具清洁剂中含氢氧化钠 |
①工业:制漂白粉 ②农业:改良____性土壤、配波尔多液 ③建筑: |
2、酸的通性(具有通性的原因:____________________________________________________________)
(1)与酸碱指示剂的反应: 使紫色石蕊试液变______色,不能使无色酚酞试液变色
(2)金属 + 酸 → 盐 + 氢气 如:___________________________________________
(3)碱性氧化物 + 酸 → 盐 + 水 如:____________________________________________
(4)碱 + 酸 → 盐 + 水 如:___________________________________________________
(5)盐 + 酸 → 另一种盐 + 另一种酸(产物符合复分解条件) 如:_______________________________
1、浓盐酸、浓硫酸的物理性质、特性、用途
|
|
浓盐酸 |
浓硫酸 |
|
颜色、状态 |
“纯净”: ______色液体 工业用盐酸:黄色(含Fe3+) |
_______色粘稠、_______状液体 |
|
气味 |
有_______________气味 |
无 |
|
特性 |
__________________性 (敞口置于空气中,瓶口有白雾) |
__________性__________ 性__________性 |
|
用途 |
①金属________ ②制造_____________ ③人体中含有少量盐酸,助_____________ |
①金属_____________ ②浓硫酸作___________剂 ③生产化肥、精炼石油 |
 酸是由___元素和_____根组成的化合物 如:硫酸(________)、盐酸(________)、硝酸(_________)
酸是由___元素和_____根组成的化合物 如:硫酸(________)、盐酸(________)、硝酸(_________)
碱是由_________和_________组成的化合物 如:氢氧化钠(________)、氢氧化钙(________)、氨水(________)
酸、碱、盐的水溶液可以导电(原因:溶于水时离解形成自由移动的阴、阳离子)
67.某工厂化验室用溶质的质量分数为20%的氢氧化钠溶液,洗涤一定量石油产品中的残余硫酸,共消耗氢氧化钠溶液40g,洗涤后溶液呈中性,求在这一定量的石油产品里含H2SO4多少克?
66.某化工厂技术人员欲用稀盐酸处理含80g氢氧化钠的污水(污水中的其他成分不与盐酸反应),共消耗稀盐酸500g。计算所用稀盐酸中溶质的质量分数。
65.学校课外活动小组为了测定某钢铁厂生铁样品中铁的质量分数,在实验室中称取生铁样品5.8g放入烧杯中(烧杯的质量为30g),然后再加入50g稀硫酸,使之充分反应后,称量,烧杯及烧杯中物质的总质量为85.6g(已知该反应中稀硫酸足量,杂质不参与反应)。请计算:
(1)产生氢气的质量是多少?
(2)该生铁样品中铁的质量分数?(结果保留一位小数)
64.在学校的元旦联欢会上,某同学表演了“水能生火”的魔术。他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来。小蔡很感兴趣,于是,他和同学们进行探究。
[提出问题]过氧化钠与水反应生成了什么物质?为什么脱脂棉会燃烧?
[猜想]①可能有一种气体和另一种物质生成
②反应过程中可能有热量放出
[设计装置]如下图所示
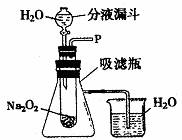
[实验探究]
实验一:探究反应后生成的气体是什么?
(1)打开上图装置中分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃。说明生成的气体是____________________。
(2)实验中,还观察到伸入烧杯中的导管口有气泡冒出,请解释产生该现象的原因:____________________________________________________________
实验二:继续探究反应后生成的另一种物质是什么?
(1)小张猜想另一种物质是Na2CO,小蔡认为不可能。小蔡的依据是:__________________________________________________________________
(2)小蔡取反应后所得的溶液于试管中,滴入无色酚酞试液,发现酚酞试液变红色,说明反应后所得的溶液呈__________性。
[表达]由实验探究的结果,写出过氧化钠和水反应的化学方程式
_____________________________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com