
63.请根据下表回答有关问题。(除第(2)小题外,其余均用序号填写)
|
序号 |
① |
② |
③ |
④ |
|
物质 |
醋酸 |
高锰酸钾 |
熟石灰 |
纯碱 |
|
化学式 |
CH3COOH |
KMnO4 |
Ca(OH)2 |
NaCO3 |
(1)上表中的物质属于碱的是___________。
(2)用表中的物质作为反应物,写出符合下列要求的化学方程式。
①实验室制取氧气________________________________________________________
②制取氢氧化钠__________________________________________________________
(3)若要测定纯碱溶液的酸碱度,可选用下列选项中___________。
①无色酚酞试液 ②紫色石蕊试液 ③pH试纸
(4)槟榔芋皮上含有一种碱性的物质--皂角素,皮肤沾上它会奇痒难忍。可选用下列___________来涂抹止痒。①食醋(含醋酸) ②熟石灰 ③纯碱
62.往氢氧化钾溶液滴入几滴紫色石蕊试液,溶液显蓝色。在氢氧化钾溶液中大量存在的粒子有H2、O、K+和OH-,哪一种粒子能使紫色石蕊试液变蓝色呢?我们进行如下探究:
(1)提出假设:是________粒子使紫色石蕊试液变蓝色。
(2)实验探究:①在第一支试管中加入2mL水,再滴入几滴紫色石蕊试液,试液不变色,说明水分子不会使紫色石蕊试液变蓝色。②在第二支试管中加入2mLK2SO4溶液,再滴入几滴紫色石蕊试液,试液不变色,说明________________________________________。
(3)结论:原假设________。(填“成立”或“不成立”)
61.如下图是某桶装矿泉水标签的一部分。据此回答:
|
水中含有的主要 成分及含量mg/L 钾 0.86 钠 33.00 钙 14.70 镁 20.82 |
|
pH 8.20 |
|
(1)该矿泉水是(填“混合物”或“纯净物”)__________;
(2)该矿泉水呈(填“酸性”“碱性”或“中性”)__________;
(3)患骨质疏松的病人应补充该矿泉水成分中的__________元素。
60.小明在校园文化节的晚会上给同学们表演了一套小魔术,其步骤是:
①将一小块生石灰放入盛有清水的大烧杯中,烧杯中冒出大量“白色烟雾”,用玻璃棒搅拌,清水变成了“牛奶”;
②将一朵浸过A试剂的小纸花浸入“牛奶”中,小纸花由白色慢慢变成了红色;
③向烧杯中加入适量无色溶液B,用玻璃棒小心搅拌,杯中“牛奶”消失并变为无色澄清,小红花又变回小白花;
④向烧杯中继续加入另一种无色溶液c,用玻璃棒搅拌,杯中澄清溶液又变成“牛奶”;
⑤向再次出现的“牛奶”中加入溶液B,烧杯中有大量气泡冒出,杯中“牛奶”又变澄清;
⑥向第⑤步的澄清溶液中加入无色溶液D,用玻璃棒搅拌,烧杯中又出现“牛奶”,加入稀硝酸“牛奶”不消失。
请根据你所学化学知识判断:
(1)试剂A是___________;溶液B是___________;C可以是___________溶液;D是___________溶液;第①,④,⑥步操作中的“牛奶”是否是同一物质(填“是”或“不是”)。
(2)写出第⑥步操作所发生的化学反应中的一个化学方程式:
________________________________________________________________________。
59.化学物质及其变化与人类生产、生活密切相关。
(1)目前,一些发达国家已基本采用新一代饮用水消毒剂二氧化氯。二氧化氯中氯元素的化合价为________。
(2)电镀或焊接前,常用稀盐酸除去铁制品表面的铁锈(主要成分为Fe2O3)。用化学方程式表示其反应原理________。
(3)某食品的包装袋内,有一个装有白色颗粒状固体的小纸袋。上面写着“干燥剂,主要成分是生石灰,请勿食用”。生石灰起干燥作用时发生反应的化学方程式为_____________,该反应的基本类型为________。
58.黄瓜中富含维生素C,其分子结构如图。
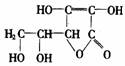
维生素C由______________元素组成。维生素C在pH<5的环境中较稳定,为减少维生素C的损失,黄瓜在烹饪时应加入少量的______________。维生素C片保存时,应注意避热、避光、密封,请你据此推测维生素C的化学性质______________。
57.欲除去N2中的少量H2、CO、CO2、水蒸气等杂质,可使混合气体通过下列物质:①浓硫酸 ②NaOH溶液 ③灼热的CuO,最合理的顺序是___________(用序号表示)。
56.水是宝贵的自然资源,在工农业生产和日常生活中有着极其广泛的应用。
(1)自来水的生产过程大体如图:
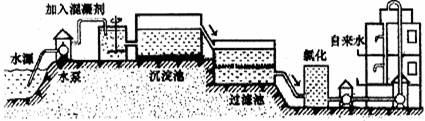
上图过滤池中有活性炭层,活性炭起___________作用,该过程中发生___________变化。氯化时,通常通入一定量氯气,它与水反应生成盐酸和次氯酸。实验室配制AgNO3溶液时不宜使用自来水,其原因是(用化学方程式表示)____________。高铁酸钾(K2FeO4)是一种理想的水处理剂,高铁酸钾中铁元素的化合价是___________。
(2)电解水时,加入少量NaOH可以增强水的导电性。现将0.1gNaOH溶解在99.9g水里,接通直流电源后,与电源正极相连的一端放出的气体是___________,当溶液中NaOH的质量分数变为0.2%时,有___________水被分解。
(3)在河旁有甲、乙、丙、丁四座工厂(位置下图所示),每个工厂排出的废液只含有Na2CO3、FeCl3、NaOH、HCl中的一种。某环保小组对河水监测时发现:甲处河水呈无色;乙处河水呈红褐色;丙处河水由浑变清;丁处产生气泡,河水澄清。请回答:

①甲工厂排出的废液是一种碱性物质,检验该物质呈碱性可选用的试剂是_____________。
②乙处河水呈红褐色的化学方程式是_____________。
③丁处产生气泡的化学方程式是____________。
(4)保护水资源,我们应该采取的措施是____________。
55.X是两种金属氧化物组成的混合物,为了研究混合物的成分,进行了如图所示的实验。
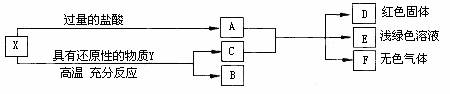
(1)X中含有的金属元素是____________(填元素符号)。
(2)写出X中一种成分与盐酸反应的化学方程式:____________。
(3)若Y为固体,写出Y与X中一种成分反应的化学方程式____________;若Y为气体,Y还可以是____________(填化学式)。
54.推理是化学学习中常用的思维方法。以下4个推断正确的是( )
A.氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物
B.酸与碱反应生成盐和水,所以生成盐和水的反应一定是酸与碱的反应
C.燃烧一般都伴随发光、放热现象,所以有发光、放热的现象就是燃烧
D.醇类物质在空气中完全燃烧生成CO2和H2O,甲醇是醇类的一种,所以甲醇在空气中完全燃烧生成CO2和H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com