
17.(16分)A、B、C、D四种均为短周期元素,原子序数依次增大
(1)A元素原子最外层电子数是核外电子层数的3倍,A与D同主族,A和D可形成两种化合物X和Y,X和水反应后生成一种具有还原性的二元酸M,M可以使溴水褪色。
(2)A元素的单质和C元素的单质化合可生成Z, Z在加热条件下跟水反应的产物1 mol需用3mol KOH才能完全中和。
(3)A元素的单质和B元素的单质一定条件下反应生成化合物N,D元素的单质和B元素的单质反应生成化合物G,化合物N和化合物G的相对分子质量相等,且焰色反应均呈黄色。
回答下列问题:
(1)画出元素D的离子结构示意图:__________
___;写出元素D的原子核外电子排布式

(2)A、B、C、D四种元素的原子半径按由小到大排列的顺序为(用相应的元素符号表示):
_____________________________ ____
(3)M可以使溴水褪色,写出该反应的离子方式 ;
(4)Z与热水反应的化学方程式
。
(5)化合物N与化合物G的水溶液反应,若氧化剂与还原剂物质的量之比为1:1,该反应的离子方程式为
(6)常温下,D的氢化物呈气态,有毒,水溶液呈酸性。脱除天然气中D的氢化物既能减少环境污染,又可回收D的单质。
用过量NaOH溶液吸收D的氢化物后,以石墨作电极电解该溶液可回收D的单质,其电解总反应的化学方程式(忽略溶解氧的氧化还原反应)为__________ ;
该方法的优点是_______________ _____ 。
16. (8分)某溶液由Na+、Cu2+、Fe3+、AlO2-、CO32-、SO42-、Cl-中的若干种离子组成。取适量该溶液进行如下实验:

①向其中加入过量的盐酸,有气体生成,并得到无色透明的溶液

②在①所得的溶液中加入过量氨水,产生白色沉淀,过滤;

③在②所得的滤液中加入过量Ba(OH)2溶液,产生白色沉淀,过滤;

④在③所得的滤液中加入过量稀硝酸,再加入硝酸银溶液,产生白色沉淀。

根据以上实验回答下列问题:

(1)据①可知溶液中肯定存在的离子是
。

(2)③中反应的离子方程式为
。

(3)溶液中肯定不存在的离子是
。

(4)溶液中一定存在的溶质是
。

15.已知在硫酸铝、硫酸钾和明矾的混合溶液中,C(SO42-)=0.2mol/L,若向其中加入等体积0.2mol/L的KOH溶液(混合后体积变化忽略不计),恰好使所生成的沉淀完全溶解,则所得溶液中的C(K+)为(
)
A .0.250mol/L B. 0.225mol/L
C .0.150mol/L D.0.450mol/L

第II卷(非选择题 共55分)
14.某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a,将其全部投入50 mL b mol·L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物)。下列说法正确的是( )
A.若金属有剩余,在溶液中再滴入硫酸后,金属不溶解

B.若金属全部溶解,则溶液中一定不含有Fe3+

C.若金属全部溶解,且产生336 mL气体(标准状况),则b = 0.3

D.当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b≥80y(1-a/3)

13.可逆反应mA(s)+nB(g) eC(g)+fD(g),反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度和不同压强的条件下随时间的变化如图所示。下列叙述正确的是( )
eC(g)+fD(g),反应过程中,当其他条件不变时,C的体积分数φ(C)在不同温度和不同压强的条件下随时间的变化如图所示。下列叙述正确的是( )
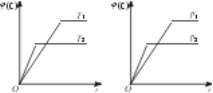

A.达到平衡后,若使用催化剂,C的体积分数将增大
B.化学方程式中,化学计量数的关系为n>e+f
C.达到平衡后,若温度升高,化学平衡向逆反应方向移动
D.达到平衡后,增加A的质量有利于化学平衡向正反应方向移动
12.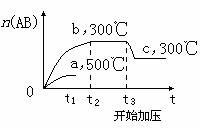 可逆反应:A2(?)+B2(?)
可逆反应:A2(?)+B2(?)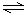 2AB(?);ΔH=-QkJ/mol,当温度和压强改变时n(AB)的变化如下图,下列叙述正确的是( )
2AB(?);ΔH=-QkJ/mol,当温度和压强改变时n(AB)的变化如下图,下列叙述正确的是( )
A.A2、B2及AB均为气体,Q>0
B.AB为气体,A2、B2至少有一种为非气体,Q>0
C.AB为气体,A2、B2有一种为非气体,Q<0
D.AB为固体,A2、B2有一种为非气体,Q>0

11.某体积可变的密闭容器,盛有适量的A和B的混合气体,在一定条件下发生反应:A+3B 2C,若维持温度和压强不变,当达到平衡时,容器的体积为V L,其中C气体的体积占10%,下列推断正确的是
2C,若维持温度和压强不变,当达到平衡时,容器的体积为V L,其中C气体的体积占10%,下列推断正确的是
A.原混合气体的体积为1.2VL B.反应达到平衡时气体B消耗掉0.05VL
C.反应达到平衡时气体A消耗掉0.06V L D.原混合气体的体积为1.1VL
10.对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,下列有关叙述正确的是( )
①生成物的百分含量一定增加 ②生成物的产量一定增加 ③反应物的转化率一定增大
④反应物的浓度一定降低 ⑤正反应速率一定大于逆反应速率 ⑥使用了适宜的催化剂
A.②⑤ B.①② C.③⑤ D.④⑥
9.第29届奥运会已在北京举行,体操王子李宁凌空点火举世瞩目。2008年北京奥运会“祥云”火炬采用的是环保型燃料---丙烷(C3H8),悉尼奥运会火炬所用燃料为65%丁烷(C4H10)和35%丙烷,已知丙烷的燃烧热为:2221.5kJ/mol,下列有关说法正确的是 ( )21世纪A.丙烷的沸点比正丁烷高
B.奥运火炬燃烧主要是将化学能转变为热能和光能
C.丙烷、空气及铂片可组成燃料电池,在丙烷附近的铂极为电池的正极
D.丙烷燃烧的热化学方程式为:C3H8(g)+5O2(g)→3CO2(g)+4H2O(g);△H=2221.5kJ/mol
8.从矿物学资料查得,一定条件下自然界存在如下反应:
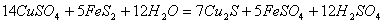 。下列说法正确的是( )
。下列说法正确的是( )
A.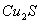 既是氧化产物又是还原产物
既是氧化产物又是还原产物
B.5
mol 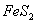 发生反应,有10 mol电子转移
发生反应,有10 mol电子转移
C.产物中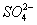 有一部分是氧化产物
有一部分是氧化产物
D.FeS2只作还原剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com