
11.I2在KI溶液中存在下列平衡: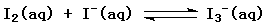 。测得不同温度下该反应的平衡常数置如下表:
。测得不同温度下该反应的平衡常数置如下表:
|
t/℃ |
5 |
15 |
25 |
35 |
50 |
|
K |
1100 |
841 |
680 |
533 |
409 |
下列说法正确的是:
A.反应
B.其他条件不变,升高温度,溶液中c(I3-)减小
C.设反应的平衡常数表达式是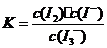
D.25℃时,向溶液中加入少量KI固体,平衡常数K小于680
10.下列叙述正确的是:
A.146C和147N的质子数相同,中子数不同
B.2814Si和 2914Si的质子数相同,是同一种核素
C.Na和K属于IA族元索,Na的金属性比K强
D.Cl和Br属于ⅧA族元素,两原子核外电子数之差为8
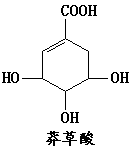
9.莽草酸可用于合成甲型流感药物--达菲。下列关于莽草酸的叙述正确的是:
A.能与氧化铁溶液发生显色反应
B.能发生消去反应生成苯甲酸
C.能使溴的四氯化碳溶液褪色
D.能发生银镜反应
8.下列说法错误的是:
A.硅胶疏松多孔,可用作催化剂的载体
B.日用铝制品表面覆盖着氧化膜,对内部金属起保护作用
C.纯净的二氧化硅是制造光导纤维的基本原料 ,
 D.氮的固定只有在高温、高压、催化剂的条件下才能实现
D.氮的固定只有在高温、高压、催化剂的条件下才能实现
7.下列实验操作正确的是:
A. 过滤时,用玻璃棒搅拌漏斗中的液体以加快过滤速度
B.中和滴定过程中,应注视锥形瓶内溶液颜色的变化,以准确把握滴定终点
C.配制0.1moI-LH2SO4溶液时,将量取的浓H2SO4,注入容量瓶中加水稀释
D.测定溶液的PH值时,用玻璃棒矗取少量溶液点在湿润的pH试纸上再与标准比色卡对照
25.(5分)一定条件下将8mol H2和4molCO充入0.5L的密闭容器中,发生如下反应:2H2(g)+CO(g)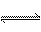 CH3OH(g)。6s后测得容器内生成CH3OH的2mol,求:
CH3OH(g)。6s后测得容器内生成CH3OH的2mol,求:
(1)用H2表示的化学反应速率。
(2)如果此时将反应所得到的混合物充分燃烧,至少需要标准状况下的氧气多少升?
24.(7分)0.5mol 的Y元素的离子得到6.02×1023个电子被还原成中性原子,0.4gY的氧化物恰好与100ml 0.2mol .L-1 的盐酸完全反应,Y原子核内质子数和中子数相等。写出:
(1)Y的名称为 ,它在周期表的位置为 ;
(2)Y的氧化物与盐酸反应的离子方程式为 。
23.(10分)A、B、C 三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

|
|
|
(1)A中反应的离子方程式为 ,
B中Cu极电极反应式为 。
(2)C中被腐蚀的金属是 ,总反应方程式为 ,
A.B、C中铁被腐蚀的速率,由大到小的顺序是 。
22、(10分)A、B、C、D四种短周期元素,原子序数D>A>B>C,且A、B同周期,C、D同主族,A的原子结构示意图为: ,B、C可形成离子化合物B3C2,据此填空:
,B、C可形成离子化合物B3C2,据此填空:
(1)A的元素名称为 ,在周期表位置___________________________
(2)A、B、C、D四种元素的原子,半径由小到大的顺序为 (用元素符号表示)。
(3)B和C最高价氧化物的水化物反应的离子方程式 。
21.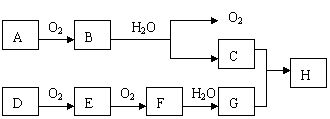 (8分)在下述转化关系中,已知B、D都是淡黄色固体,且A与D为单质,并可反应生成离子化合物。
(8分)在下述转化关系中,已知B、D都是淡黄色固体,且A与D为单质,并可反应生成离子化合物。
试回答:
(1)写出下列物质的化学式:A_________、G_________。
(2) 写出C的电子式 ______________。
(3) 写出C+G →H的化学反应方程式_______ __________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com