
27.物质的分类依据通常有组成和性质,下列对钠的化合物的分类的说法中,只考虑组成的是( )
A.Na2O2是氧化物,不是碱性氧化物
B.Na2CO3不是碱,是一种钠盐
C.NaOH是一元碱、强碱
D.NaClO是氧化性盐、含氧酸盐
[猜题理由]物质的分类是新课改新增加的内容,它能考查学生对分类依据、物质共性和特性的掌握程度。具有相同组成的物质在某些性质上具有相似性,具有相同的某一性质的不同物质,其组成不一定相同,从掌握组成、性质等方面对单质、酸、碱、盐、氧化物进行分类,可加深对物质性质的理解,这种类型是以前高考命题中没有出现过的,是今后高考中值得注意的一个问题。
26.绿藻的胶质中分离出一种有机化合物(用A表示),结构如图,A对人体无害,可用于新鲜食品中对脂肪酶进行抑制来保持风味,也可外用使伤口快速愈合。则关于该物质的说法不正确的有( )
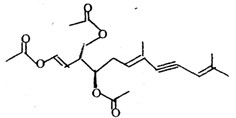
A.该物质的化学式为C21H26O6
B.该物质中含有1个手性碳原子
C.1mol该物质最多能消耗5mol H2和含3mol NaOH的溶液反应
D.该物质能发生加成反应、取代反应、氧化反应
[猜题理由]通过复杂有机物的结构考查学生对手性碳原子、与常见无机物的反应的量的关系、以及官能团的性质。有机物的结构与性质的考查重现率答100%,是各地考试的热点。本体的一个重要特点:江苏今年考试说明新增“手性碳原子”的考查要求
25.下列叙述正确的是( )
A.向体积为Va的0.02mol·L-1CH3COOH溶液中加入体积为Vb的0.02mol·L-1NaOH溶液,Va>Vb时:c (CH3COOH)+c(CH3COO-)>c (Na+)
B.将0.2 mol·L-1的盐酸与0.1 mol·L-1的KAlO2溶液等体积混合,其溶液中离子浓度由小到大的顺序为:c(OH-)<c(Al3+)<c(H+)<c(K+)<c(Cl-)
C.pH=5的HCOOH溶液和pH=5的NH4NO3溶液中,c(H+)不相等
D.25℃时,pH=4,浓度均为0.1mol·L-1的CH3COOH、CH3COONa混合溶液:
c(CH3COO-)+c(OH-)<c(CH3COOH)+c(H+)
[猜题理由]化学反应都是在溶液中进行,电解质溶液间会发生离子反应,涉及到离子共存,电离及盐类水解,比较离子浓度大小是高考重点,考试自然要考查到,体现化学教改精神,符合考纲。
24.常温下,将200ml pH=a的CuSO4和K2SO4的混合溶液用石墨电极电解一段时间,测得溶液的PH变为b(溶液体积的变化忽略不计),在整个电解过程中始终发现只有一个电极有气体产生。下列说法错误的是 ( )
A.若使电解质溶液恢复到电解前的浓度可向溶液中加入9.8×(10-b-10-a)g Cu(OH)2
B.b<a<7
C.阳极产生的气体是O2,其体积(标准状况下)为:1.12×(10-b-10-a)L
D.阴极电极反应式为:Cu2++2e-=Cu
[猜题理由]全国高考理综卷Ⅰ卷化学部分自2004年至2009年电化学部分年年有题,并且涉及的内容均是电解原理的应用及其有关计算,近几年其他省市高考理综化学试题也是年年必出电化学试题(原电池,燃料电池,电解等),尤其是电解原理的应用及其有关计算。常考到的有:用惰性电极电解NaCl、KI、CuSO4、AgNO3、NaOH、Na2SO4等溶液以及电镀和精炼。我预计今年高考理综卷Ⅰ在电解原理的应用及有关计算方面出题的可能性仍然很大。该题以课本电解硫酸铜的习题为基础改编的电解CuSO4和K2SO4的混合溶液试题,由题意知实质还是电解CuSO4溶液及有关计算。
23.物质的量浓度相等的氨水溶液与硫酸溶液等体积混合,则有关混合溶液中离子浓度关系不正确的是( )
A.c(SO42-)>c(H+)>c(NH4+)>c(OH-) B.c(H+)>c(SO42-)>c(NH4+)>c(OH-)
C.c(OH-)-c(NH4+)=c(H+)-2c(SO42-) D.c(OH-)+c(NH3·H2O)=c(H+)-c(SO42-)
[猜题理由]电解质溶液中离子浓度的关系,即离子浓度大小判断、溶液中的三守恒原理是有关电解质溶液化学知识的灵魂。主要考查学生对电解质溶液重离子间关系的理解与判断,有利于考察学生的综合能力。
22.为提高中学生的公益意识,某市团委举办了一次科技下乡活动,在为农民伯伯做铅蓄电池的介绍时,下列分析属于失误的是(已知铅蓄电池的反应为Pb+PbO2+2H2SO4
 2PbSO4+2H2O)(
)
2PbSO4+2H2O)(
)
A.铅蓄电池是生活里最常用的可充电电池,在充电时,电池的正极应接直流电源的正极
B.铅蓄电池在放电时,电解液的酸性减弱
C.铅蓄电池在放电时,PbO2作为负极,不断转化为PbSO4
D.铅蓄电池在充电时,PbO2是氧化产物
[猜题理由]电化学是中学化学中的一个重要知识点,原电池、电解池是化学能与电能相互转化的重要装置,而蓄电池是将二者巧妙结合在一起的装置。通过分析反应中元素化合价的变化来掌握氧化还原反应的规律,是高考的热点。
21.向一体积不变的密闭容器中加入2mol A、0.6mol C和一定量的B三种气体。一定条件下发生反应,各物质浓度随时间变化如图一所示。图二为t2时刻后改变反应条件,平衡体系中反应速率随时间变化的情况,且四个阶段都各改变一种不同的条件。已知t3-t4阶段为使用催化剂;图一中t0-t1阶段c(B)未画出。
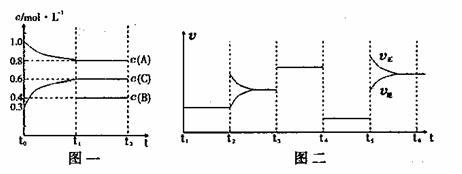
下列说法不正确的是( )
A.此温度下该反应的化学方程式2A(g)+B(g) 2C(g)
2C(g)
B.t4-t5阶段改变的条件为减小压强
C.B的起始物质的量为1.0mol
D.在相同条件下,若起始时容器中加入a mol A、bmol B和cmol C,要达到t1时刻同样的平衡,a、b、c要满足的条件为a+ =2.4 和 b+
=2.4 和 b+ =1.2
=1.2
[猜题理由]必考题型。以图像的形式考查影响化学反应速率以及化学平衡移动的因素。
20.据南京日报2009年11月9日报道,南京的空气质量拉响警报,8日全市污染指数更是超过300,达到重度污染,二氧化硫等污染物的浓度比平时高出2倍之多,秸秆焚烧再度成为城市空气急速污染的“元凶”。关于空气污染,下列说法正确的是( )
A.二氧化硫、二氧化氮、一氧化碳和二氧化碳是空气质量报告中涉及的主要污染物
B.正常雨水的pH等于7
C.二氧化硫和二氧化氮是引起酸雨的主要气体
D.秸秆焚烧总体来说对庄稼是有益的,值得提倡
[猜题理由]环境问题一直是高考的热点,注意与环境相关的时事,如节能减排、哥本哈根会议等。设计本题的目的是对空气质量日报的考查,该知识点是化学与生活中的重要考点,由于二氧化碳属于温室气体,一氧化碳属于有毒气体,许多同学受到思维定势的影响,误认为二者属于空气质量日报内容,而导致答案错误。当前空气质量报告中所包含的物质是二氧化氮、二氧化硫和可吸入颗粒物,做题时要根据此定义内容来确定答案。
19.有机物甲的分子式为 CxHyO2, 其中O%为20.25%,C%为68.35%。在酸性条件下,甲水解为乙和丙两种有机物,在相同温度和压强下,同质量的乙和丙的蒸气所占的体积相同,则甲的可能结构有 ( )。
A.8 种 B.14种 C.16种 D.18种
[猜题理由]同分异构体在高考试题中重现率为100%,可以综合考查的综合运用知识的能力。
18.已知:NaHCO3在潮湿的空气中会缓慢分解,Na2CO3会吸收空气中的水分:
Na2CO3+nH2O=Na2CO3·nH2O(n为平均值,n≤10)。取没有妥善保管的NaHCO3样品A 9.16g,溶于水配成溶液,慢慢滴入稀盐酸并不停地搅拌,加入盐酸的体积与生成的CO2的体积(标准状况)如下表。(不计溶于水的CO2气体)
|
盐酸体积(mL) |
8 |
15 |
20 |
50 |
x |
120 |
 150 150 |
|
生成CO2体积(mL) |
0 |
112 |
224 |
896 |
2240 |
2240 |
2240 |
下列说法中不正确的是( )
A.x的最小值为110
B.x的最小值为100
C.所加盐酸物质的量浓度为1.0mol/L
D.样品A中NaHCO3和Na2CO3·nH2O的物质的量分别为0.090mol和0.010mol
[猜题理由]该题考查知识点为有关溶液物质的量浓度的计算。若纯粹考查计算会比较单一,结合反应和对数据的分析考查能体现学生分析问题的能力。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com