
13.在常温的条件下:
设某PH值的硫酸溶液中水的电离度为α?1,相同PH值的硫酸铝溶液中水的电离度为α2, 那么α1和α2的数值相比较,α2 α2。
某硫酸和硫酸铝两种溶液的PH值都是3,那么硫酸中水电离出的[H+]是硫酸铝中水电离的[H+]的 倍。
若设某PH值的硫酸中水电离出的[H+]=1.0×10-amol/l,设相同PH值的硫酸铝中水电离出的[H+]=1.0×10-bmol/l,(a、b都是小于14的正数),那么a、b之间 满足的关系式是 、 (用一个等式和一个不等式表示)。
知识点:PH值的计算、水的离子积常数,盐类水解
能力点:逆向思维、知识综合运用、计算能力
12.物质的量浓度相同的下列各组物质的溶液中,对指定的离子的浓度作大小比较,其中错 误的是( )
A.[PO43-]:Na3PO4>Na2HPO4>NaH2PO4>H3PO4
B.[CO32-]:(NH4)2CO3>Na2CO3>NaHCO3>NH4HCO3
C.[NH4+]:(NH4)2SO4>(NH4)2CO3>NH4HSO4>NH4Cl
D.[S2-]:Na2S>H2S>NaHS
知识点:盐类的水解
能力点:分析、比较、归纳能力
11.A、B两种酸溶液的pH都是2,各取1mL分别加水稀释成1000 mL,其pH的变化如下图所示,则下列判断正确的是( )
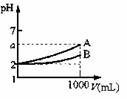 A.原酸溶液的浓度cA=cB
A.原酸溶液的浓度cA=cB
B.原酸溶液的浓度cA>cB
C.若a=5,则A为强酸,B为弱酸
D.若2<a<5,则A、B都是弱酸,酸性A>B
知识点:弱电解质的pH值与电离度的计算与比较。
能力点:识图能力。
10.有一学生在实验室测某溶液的PH值,实验时,其先用蒸馏水润湿PH试纸,然后用洁净干 燥的玻棒蘸取试样进行检测
(1)该生的操作方法是否正确?如不正确,说明理由。
(2)若用此法分别测定[H+]相等的H2SO4和H3PO4溶液的PH值,结果会怎样?
知识点:PH试纸的使用
能力点:实验能力、观察能力、分析能力
9.碘滴定法应在( )
A.强酸性溶液中进行 B.强碱性溶液中进行
C.接近中性溶液中进行 D.以上三种均可
知识点:氧化-还原反应
能力点:创新思维
8.在滴定法中,常用作指示剂的是( )
A.淀粉 B.甲基橙 C.酚酞 D.石蕊
知识点:滴定法测定待测液浓度
能力点:知识的迁移运用,创新思维
7.已知白色PbSO4难溶于水,也不溶于HNO3,却可溶于醋酸铵饱和溶液中,其反应式为:
PbSO4+CH3COONH4 (CH3COO)2Pb+(NH4)2SO4
(CH3COO)2Pb+(NH4)2SO4
在无色的(CH3COO)2Pb溶液中通入H2S气体,有黑色沉淀(PbS)生成,则下列说法正确的是( )
A.(CH3COO)2Pb是难电离的物质 B.CH3COONH4是弱电解质
C.通入H2S时离子反应为:Pb2++2CH3COO-+2H2S PbS↓+2CH3COOH
PbS↓+2CH3COOH
D.PbSO4溶于CH3COONH4溶液的离子反应为:
PbSO4+2CH3COO- (CH3COO)2Pb+SO42-
(CH3COO)2Pb+SO42-
知识点:弱电解质的电离、离子反应的实质
能力点:观察能力、分析综合能力
碘滴定法是以硫代硫酸钠为标准溶液来滴定溶液中I2(或溶解的I2或反应生成的 I2),以测定待测液中一些物质含量的方法,反应为:I2+2S2O32-
 2I-+S4O62-?,根据以上信息回答8、9题。
2I-+S4O62-?,根据以上信息回答8、9题。
6.欲使醋酸稀溶液的电离度和PH值同时降低,应采取的措施是( )
A.加热 B.加盐酸 C.加适量水 D.加冰醋酸
知识点:弱电解质的电离平衡
能力点:发散思维和收敛思维
5.下列关系式中正确的是( )
A.pH=5的盐酸溶液稀释1000倍后,pH=8
B.pH=2和pH=4的两种盐酸等体积混合,混合酸的pH=3
C.pH=10和pH=12的两种NaOH溶液等体积混合,混合碱的pH=10.3
D.0.10 mol/L盐酸和0.06 mol/L Ba(OH)2溶液等体积混合,混合液的pH=12.0
知识点:pH值的应用。
能力点:分析与计算能力。
4.酸碱质子理论认为:凡能给出质子的分子或离子都是酸,凡能结合质子的分子或离子都是碱。按照这个理论,下列属于两性物质的微粒是( )
①H2O ②CN- ③HS- ④CH3COOH ⑤H2PO4- ⑥OH-
A.①②⑤ B.③④⑥ C.①③⑤ D.②④
知识点:物质的组成
能力点:知识的迁移、运用;创新思维
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com