
4.(14分)短周期元素组成的单质X2、Y ,标准状况下X2的密度为3.17g·L-1,;常温下, Y为浅黄色固体。Z是一种化合物,焰色反应呈浅紫色(透过钴玻璃);0.1mol·L-1 Z的水溶液pH=13 。X2、Y 和Z之间有如下转化关系(其他无关物质已略去):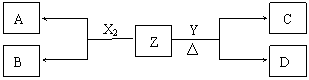
 (1)写出单质X2与Z反应的离子方程式:
(1)写出单质X2与Z反应的离子方程式:
(2)已知16g单质Y完全燃烧放出148kJ热量。写出热化学方程式:
(3)已知C能与硫酸反应生成能使品红溶液褪色的气体
①D的化学式是: ;D的水溶液pH>7,原因是(用离子方程式表示):
;D的水溶液中离子浓度大小顺序为
②将20mL 0.5mol·L-1 C溶液逐滴加入到20 mL 0.2mol·L-1 KMnO4溶液(硫酸酸化)中,溶液恰好褪为无色。写出反应的离子方程式:
(4)石墨和铁做电极,用隔膜电解槽电解A的溶液,阳极产生X2 。
写出电解A溶液的离子方程式:
3.(本题14分)
(1) ②⑤ (2分)
(2) 4Fe2++4Na2O2+6H2O=4Fe(OH)3↓+O2↑+8Na+ (2分)
2Fe3++SO2+2 H2O =2Fe2++SO42-+4 H+ (2分)
(3)Fe3++3 H2O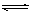 Fe(OH)3+3 H+
(2分)
Fe(OH)3+3 H+
(2分)
(4)MnO2 + 4 HCl(浓) Mn Cl2+Cl2↑+2
H2O
(2分)
Mn Cl2+Cl2↑+2
H2O
(2分)
|
实验步骤 |
实验现象 |
用化学用语解释 |
|
|
蓝(1分) |
Cl2+ 2I-=
I2+2Cl-(1分) |
|
|
|
5Cl2+ I2+6H2O=
2HIO3+10 HCl(2分) |
3.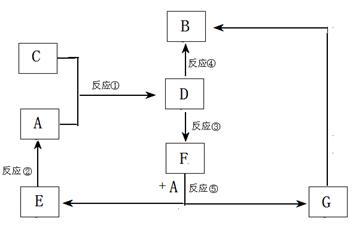 (14分)、A、B、C、D、E、F、G七种物质间存在如图所示的转化关系,其中A、B、D、G含有同种元素。
(14分)、A、B、C、D、E、F、G七种物质间存在如图所示的转化关系,其中A、B、D、G含有同种元素。
已知:(Ⅰ)A为金属单质; B为红褐色固体;E为密度最小的气体;G为浅绿色溶液。
(Ⅱ)D为黄色溶液,能与硝酸银溶液反应生成不溶于稀硝酸的白色沉淀。
(Ⅲ)D能将某种氧化物氧化为F,F是含有三种元素的化合物。
请回答下列问题:
(1)上述反应中属于置换反应的是 (填序号)。
(2)G生成B有多种途径。若在G的溶液中加入与G等物质的量的Na2O2,恰好使C转化为F,写出该反应的离子方程式:
反应③(即D将某种氧化物氧化为F)的离子方程式
(3)D的水溶液显酸性,请用离子方程式解释原因
(4)实验室制取C的化学方程式为
对气体C进行如下实验。已知整个反应过程中,每消耗0.1mol KI,转移的电子数约为3.612×1023 个。请按照要求填空:
|
实验步骤 |
实验现象 |
用化学用语解释 |
|
将少量气体通入淀粉KI溶液 |
溶液最初变成 色 |
(用离子方程式表示) |
|
继续通入气体 |
溶液逐渐变成无色 |
(用化学方程式表示) |
2.(12分) ⑴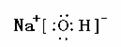 ;三;ⅢA
⑵Al3++3AlO2-+6H2O
= 4Al(OH)3
Fe2O3+2Al
;三;ⅢA
⑵Al3++3AlO2-+6H2O
= 4Al(OH)3
Fe2O3+2Al  2Fe
+ Al2O3 (Fe2O3若写成FeO或Fe3O4并配平也可以)
⑶分子 ⑷ 1∶104
2Fe
+ Al2O3 (Fe2O3若写成FeO或Fe3O4并配平也可以)
⑶分子 ⑷ 1∶104
2.(12分)27.(14分) .A.B.C.D.E是中学化学常见单质,构成它们的元素的原子序数分别为α、b. c.d.е;且3
(a+b)
= 2 (a+c)
= 3 (d-a);X、Y、Z、M、N、W、H、K是常见化合物,X是B和C的化合产物,它们之间有如下转化关系(图中反应物和产物中的H2O已略去):
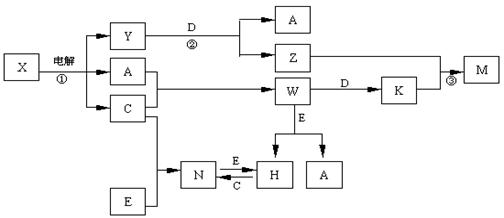
(1)Y的电子式为 ,构成D单质的元素在周期表中位于 周期 族
(2)反应③的离子方程式为 E的氧化物与D在一定条件下反应的化学方程式为: 。
(3)固体N常温下即挥发,183℃升华,几乎溶于所有的有机溶剂和H2O中,据此判断 N为 型晶体
(4)25℃时,PH=5的W和N的水溶液中由H2O电离出来的H+离子浓度之比为
1.(14分)
(1)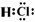 (2分)
(2分)
(2)FeCl3(2分),N可用作催化剂、净水剂、印刷电路铜板腐蚀剂和外伤止血剂等。(1分)
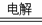 (3)2Cl-+2H2O
(3)2Cl-+2H2O 2OH- + H2↑+ Cl2↑,Al3+ + 3AlO2-+6H2O === 4Al(OH)3↓,
2OH- + H2↑+ Cl2↑,Al3+ + 3AlO2-+6H2O === 4Al(OH)3↓,
Al3+ + 3NH3·H2O === Al(OH)3↓+ 3NH4+ (方程式各3分)
1.(14分)中学化学中几种常见物质的转化关系如图所示(图中部分反应物或生成物及反应条件未列出)。
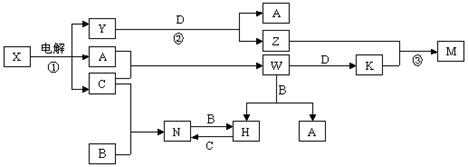
已知:A、B、C、D是单质,其余是化合物。其中B、D是常见金属,且组成B的元素属于过渡元素。又知A在C中点燃有苍白色火焰,M既可溶于盐酸又可溶于NaOH溶液。请回答下列问题:
(1)W的电子式是_______________。
(2)写出N的化学式 ,并任写一种N的主要用途 。
(3)写出下列反应的离子方程式:
反应① ,
反应③__________________________________________________________,
K溶液和过量氨水反应__________________________________________________。
15.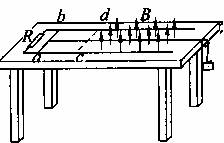 如图所示,宽度为L=0.20m的足够长的平行光滑金属导轨固定在绝缘水平桌面上,导轨的一端连接阻值为R=0.9
如图所示,宽度为L=0.20m的足够长的平行光滑金属导轨固定在绝缘水平桌面上,导轨的一端连接阻值为R=0.9 的电阻.导轨cd段右侧空间存在垂直桌面向上的匀强磁场,磁感应强度B=0.50T.一根质量为m=10g,电阻r=0.1
的电阻.导轨cd段右侧空间存在垂直桌面向上的匀强磁场,磁感应强度B=0.50T.一根质量为m=10g,电阻r=0.1 的导体棒ab垂直放在导轨上并与导轨接触良好.现用一平行于导轨的轻质细线将导体棒ab与一钩码相连,将重物从图示位置由静止释放.当导体棒ab到达cd时,钩码距地面的高度为h=0.3m.已知导体棒ab进入磁场时恰做v=10m/s的匀速直线运动,导轨电阻可忽略不计,取g=10m/s2.求:
的导体棒ab垂直放在导轨上并与导轨接触良好.现用一平行于导轨的轻质细线将导体棒ab与一钩码相连,将重物从图示位置由静止释放.当导体棒ab到达cd时,钩码距地面的高度为h=0.3m.已知导体棒ab进入磁场时恰做v=10m/s的匀速直线运动,导轨电阻可忽略不计,取g=10m/s2.求:
(1)导体棒ab在磁场中匀速运动时,闭合回路中产生的感应电流的大小
(2)挂在细线上的钩码的重力大小
3)求导体棒ab在磁场中运动的整个过程中电阻R上产生的热量
(1)感应电动努为 1分
1分
感应电流 2分
2分
(2)导体棒匀速运动,安培力与拉力平衡,则有
BIL=Mg 1分
所以 2分
2分
(3)导体棒移动30㎝的时间为 1分
1分
根据焦耳定律, (或
(或 )
1分
)
1分
根据能量守恒, 2分
2分
电阻R上产生的热量 2分
2分
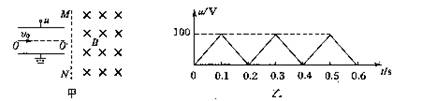
14.如图甲所示,两平行金属板的板长不超过0.2m,板间的电压u随时间t变化的图线如图乙所示,在金属板右侧有一左边界的MN、右边无界的匀强磁场。磁感应强度B=0.01T;方向垂直纸面向里。现有带正电的粒子连续不断地以速度v0=102m/s,沿两板间的中线OO/平行金属板射入电场中,磁场边界MN与中线OO/垂直。已知带电粒子的比荷 ,粒子所受的重力和粒子间的相互作用力均忽略不计。
,粒子所受的重力和粒子间的相互作用力均忽略不计。
(1)在每个粒子通过电场区域的时间内,可以把板间的电场强度看作是恒定的。试说明这种处理能够成立的理由。
(2)设t=0.1s时刻射入电场的带电粒子恰能从平行金属板边缘射出,求该带电粒子射出电场时的速度大小。
(3)对于所有经过电场射入磁场的带电粒子,设其射入磁场的入射点和从磁场射出的出射点间的距离为d,试判断d的大小是否随时间而变化?若不变,证明你的结论;若变,求出d的变化范围。
(1)带电粒子在金属板间的运动时间 ①
①
得 ,(或t时间内金属板间电压变化
,(或t时间内金属板间电压变化 ,变化很小)②
,变化很小)②
…………2分
故t时间内金属板间的电场可以认为是恒定的 …………2分
(2)t=0.1s时刻偏转电压
带电粒子沿两板间的中线射入电场恰从平行金属板边缘飞出电场,电场力做功
 ③ …………2分
③ …………2分
由动能定理: ④ …………2分
④ …………2分
代入数据可得 ⑤ …………2分
⑤ …………2分
(3)设某一任意时刻射出电场的粒子速度为v,速度方向与水平方向的夹角为 ,则
,则

 ⑥ …………2分
⑥ …………2分
粒子在磁场中有 ⑦…………2分
⑦…………2分
可得粒子进入磁场后,在磁场中做圆周运动的半径

由几何关系 ⑧ …………2分
⑧ …………2分
可得: ,故d不随时间而变化。 …………2分
,故d不随时间而变化。 …………2分
13.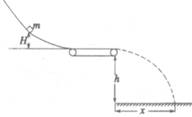 如图所示,一质量为m=0.5kg的小物体从足够高的光滑曲面上自由滑下,然后滑上一水平传送带。已知物体与传送带之间的动摩擦因数为μ=0.2,传送带水平部分的长度L=5m,两端的传动轮半径为R=0.2m,在电动机的带动下始终以ω=15rad/s的角速度沿顺时针匀速转动,传送带下表面离地面的高度h不变。如果物体开始沿曲面下滑时距传送带表面的高度为H,初速度为零,g取10m/s2。求:
如图所示,一质量为m=0.5kg的小物体从足够高的光滑曲面上自由滑下,然后滑上一水平传送带。已知物体与传送带之间的动摩擦因数为μ=0.2,传送带水平部分的长度L=5m,两端的传动轮半径为R=0.2m,在电动机的带动下始终以ω=15rad/s的角速度沿顺时针匀速转动,传送带下表面离地面的高度h不变。如果物体开始沿曲面下滑时距传送带表面的高度为H,初速度为零,g取10m/s2。求:
(1)当H=0.2m时,物体通过传送带过程中,电动机多消耗的电能。
(2)当H=1.25m时,物体通过传送带后,在传送带上留下的划痕的长度。
(3)H在什么范围内时,物体离开传送带后的落地点在同一位置。
解:传送带匀速运动的速度 (1分)
(1分)
物块与传送带问有相对运动时加速度的大小  (1分)
(1分)
(1)当 时,设物块滑上传送带的速度为
时,设物块滑上传送带的速度为 ,
,
则 (1分)
(1分)

相对滑动时间  (1分)
(1分)
物块对地位移  (1分)
(1分)
传送带前进位移  (1分)
(1分)
上述过程中电动机多消耗的电能
 (1分)
(1分)
(2)当 时,物块滑上传送带的速度为
时,物块滑上传送带的速度为
 (1分)
(1分)

物块减速时间  (1分)
(1分)
物块前进距离  (1分)
(1分)
 时间内传送带前进
时间内传送带前进  (1分)
(1分)
 划痕长度
划痕长度 (1分)
(1分)
(3)设物体滑上传送带的初速度为 时,减速到右端的速度刚好为
时,减速到右端的速度刚好为
则 (1分)
(1分)

又  (1分)
(1分)
 (1分)
(1分)
即 时,落地点位置不变。(1分)
时,落地点位置不变。(1分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com