
2.下列关于细胞内化合物的叙述中,正确的是
A.淀粉是植物细胞壁的主要成分,它的基本组成单位是葡萄糖
B.蛋白质是生命活动的主要承担者,它的基本组成单位是氨基酸
C.DNA是一切生物的遗传物质,它的基本组成单位是脱氧核苷酸
D.磷脂是细胞膜的主要成分,它的基本组成单位是甘油和脂肪酸
1.2009年全球爆发了甲型H1N1流感,世界卫生组织把对它的警戒级别提升为六级。下列相关叙述正确的是
A.接种甲型H1N1流感疫苗所引起的免疫属于非特异性免疫中的体液免疫
B.该病的病原体既能寄生在人的呼吸道中,也能在营养丰富的培养液中培养
C.该病的病原体因基因重组而容易变异,所以需要不断研制新疫苗
D.接种该疫苗后若再次接触该病的病原体,则机体可能会迅速反应产生大量抗体
31.(24分)我国于2002年3月25日在酒泉载人航天发射场发射升空的“神舟三号”飞船,遨游太空6天18小时,在预定轨道上环绕地球运行108圈后,准确降落在内蒙古中部地区。我国载人航天第三次飞行试验取得圆成功!
航空航天是一个集物理、化学、生物、天文、地理、工程、气象等多学科的综合性工程,试回答下列问题:
(1)若认为飞船绕地球做匀速圆周运动,试估算其飞行速度(已知地球的质量M=6.0×1024kg,G=6.67×10-11N·m2/kg2,计算结果取一位有效数字)
(2)发射飞船的动载火箭,其推进剂引燃后发生剧烈的反应,产生的高温气体主要是CO2、H2O、N2、NO,这些无色的气体从火箭尾部喷出,但在发射现场看火箭喷出的是大量的“红烟”,其原因是_____________(填正确选项的序号)。
A.高温下N2遇空气生成NO2 B.NO遇空气生成NO2
C.CO2与NO反应生成CO和NO2
(3)如果在“神舟三号”飞船的有轨道舱中做CCl4从水中萃取I2的实验,将溶液振荡后静止一段时间,则__________________(填正确选项的序号)。
A.溶液下层为紫色的CCl4层,上层为水层
B.溶液上层为紫色的CCl4层,下层为水层
C.溶液不分层
(4)航天搭载实验中,有一批基因型为BbCc的实验鼠,已知B决定毛黑色,b决定毛褐色,C决定毛色存在,c决定毛色不存在(即白色)。请推导实验鼠繁殖后,子代表型比的理论值:黑色:褐色:白色为________________;因受太空环境的影响,实验鼠产下的后代全为白色,则这些白鼠的基因型最多有____________种。
2010武汉市部分学校五月调研测试(理综)
30.(16分)根据量子理论,光子的能量E和动量P之间的关系式为E=PC,其中C表示光速,由于光子有动量,照到物体表面的光子被物体吸收或反射时都会对物体产生压强,这就是“光压”,用I表示
(1)一台二氧化碳气体激光器发出的激光,功率为P0、射出的光束的横截面积为S,当它垂自照射到一物体表面并被物体全部反射时,激光对物体表面的压力F=2P·N,其中P表示光子的动量,N表示单位时间内激光器射出的光子数,试用P0和S表示该束激光对物体产生的光压I;
(2)有人设想在宇宙探测中用光为动力推动深测器加速,探测器上安装有面积极大,反射率极高的薄膜,并让它正对太阳,已知太阳光照射膜时每平方米面积上的辐射功率为1.35kW,探测器和薄膜的总质量为m=100kg,薄膜面积为4×104m2,求此时探测器的加速度大小?
29.(18分)如图所示,在直角坐标系xoy的第一象限中分布着与y轴平行的匀强电场,在第四象限内分布着垂直纸面方向的匀强磁场。一个质量为m,电量为q的正粒子(不计重力)在A(0,3)点平行x轴入射,初速vA=120m/s。该粒子从电场进入磁场,又从磁场进入电场,并且只通过x轴上的点P(4.5,0)及Q(8,0)各一次。已知该粒子的荷质比为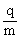 =108C/kg。
=108C/kg。
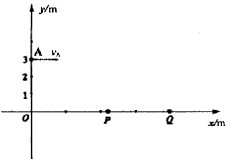
(1)若粒子先通过P点,后通过Q点,则匀强磁场的方向为__________________。
若粒子先通过Q点,后通过P点,则匀强磁场的方向为_________________。
(2)在第(1)问中任选一种情况,求磁感强度的大小。
28.(20分)用电学方法测定风力(风对物体作用力的大小)的仪器的基本结构如图1所示,质量为m的小球P系在一细长的轻金属丝下,悬挂在O点,图中CB是水平放置的光滑电阻丝。已知风力方向水平向左,OC的距离为h,CB的长度为L。实际观测中可以看到无风时,P沿竖直方向处于静止状态;有风时,在风力作用下,小球P会摆起一定的角度θ,而且风速越大,θ角亦越大。小球P在摆起的过程中,电阻丝CB与金属丝始终保持良好的接触,其接触点D处的摩擦以及细金属丝的电阻可以忽略不计。
(1)设小球平衡时,CD的长度为x,则风对球的作用力的大小为____________。
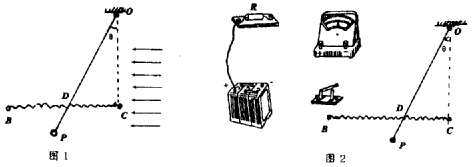
(2)取若干导线将一只电动势为ε、内阻不计的电源、一只电键、一只保护电阻和一只电流表连入基本结构之中(在基本结构中,O、B、C为接线柱),便可用来测量风力的大小。请你将图2中的实验器材用导线连接起来,使其能够用来测量风力的大小。
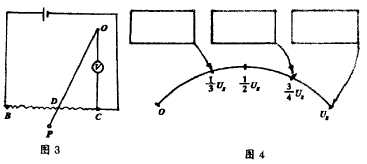
(3)若用电压表取代上述测量装置中的电流表,将电路连成如图3所示的电路亦可用来测量风力。为了能直接从表盘上读出风力的大小,需要对电压表的表盘上的刻度重新标度。若在测量风力时,电压表的示数没有超过其满偏电压值Ug,请在图4所示的方框内填入用m、L、h、ε、Ug表示的风力值。(表盘上刻度线下的标度值为原电压表的标度值)。
27.(17分)A、B都是芳香族化合物,1molA水解得到1mol B和1mol醋酸。A、B的相对分子质量都不超过200,完全燃攻都只生成CO2和H2O;B分子中碳和氢两元素的总质量分数为0.652;A溶液具有酸性,不能使FeCl3溶液显色。
请回答下列问题:
(1)A、B的相对分子质量之差为_____________。
(2)1个B分子中应该有多少个氧原子?(要求写出推理过程)
(3)求出A的分子式。(要求写出推理过程)
(4)写出B可能的三种结构简式。
26.(26分)用下图装置(酒精灯、铁架台等没有画出)制取三氯化磷,在d中放入足量的白磷,将氯气迅速而不间断地通入d中,氯气与白磷就会发生反应,产生火焰。其三氯化磷和五氯化磷的物理量如下:
熔点 沸点
三氯化磷 -112℃ 76℃
五氯化磷 148℃ 200℃分解
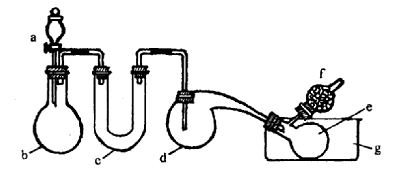
(1)若在b中装入MnO2,则a中应装入_____________。在整个装置中_____________仪器需要加热(填写仪器对应的字母)。
(2)e仪器的作用是_____________,在g中盛放冷水的目的是_____________。
(3)PCl3遇水剧烈反应,c中装入的物质是_____________,其目的是_____________。
(4)先在d中底部放人少量细砂,然后放入完全除去了水分的白磷。请回答:为什么要在d中放人少量细砂?
_________________________________________________
(5)f中碱石灰的作用是_____________。
(6)如果要除去Cl2中的HCl,实验装置应作何改进?
_________________________________________________
25.(17分)过氧化氢(H2O2)又称双氧水,也称其为绿色氧化剂。为了贮存、运输、使用的方便,工业上采用“醇析法”将其转化成固态的过碳酸钠晶体(其化学式为2Na2CO3·3H2O2),该晶体具有Na2CO3和H2O2的双重性质。“醇析法”的生产工艺过程如下:
在0-5℃下,往饱和的Na2CO3溶液中,先加入H2O2和稳定剂(MgCl2和Na2SiO3)经充分反应后,再加入异丙醇,过滤分离,即得过碳酸钠晶体。
根据以上材料,回答下列问题:
(1)写出H2O2的电子式:__________________。
(2)H2O2被称为绿色氧化剂的主要原因是___________________。
(3)稳定剂能反应生成难溶物将过碳酸钠粒子包裹住,写出稳定剂反应生成难溶物的化学方程式:_______________。
(4)加入异丙醇的作用是_________________。
(5)下列物质不会使过碳酸钠失效的是_______________。
A.MnO2 B.NaHCO3 C.H2S D.CH3COOH
24.(12分)为了降低汽车尾气对大气的污染,某城市拟用甲醇替代液化石油气作为公交车的燃料。
(1)(6分)1g甲醇在25℃完全燃烧生成液态水时,可放出24.2kJ的热量,写出该反应的热化学方程式。
(2)(6分)某汽车公司设计的一种以甲醇为燃料的汽车的质量为6t,阻力是车重的0.05倍,最大输出功率为60kW。求该车最大行驶速度是多少(g取10m/s2)?
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com