
17.
CuIЪЧвЛжжВЛШмгкЫЎЕФАзЩЋЙЬЬхЃЌЫќПЩгЩЗДгІЃК2Cu2++4IЃЃН2CuIЁ§+I2ЖјЕУЕН. ЯжвдЪЏФЋЮЊвѕМЋЃЌвдCuЮЊбєМЋЕчНтKIШмвКЃЌЭЈЕчЧАЕч НтвКжаМгШыЩйСПЗгЬЊКЭЕэЗлШмвК. ЕчНтПЊЪМВЛОУвѕМЋЧјШмвКГЪКьЩЋЃЌЖјбєМЋЧјШмвКГЪРЖЩЋЃЌЖдетИіЯжЯѓе§ШЗЕФНтЪЭЪЧ(ЁЁЁЁ)
НтвКжаМгШыЩйСПЗгЬЊКЭЕэЗлШмвК. ЕчНтПЊЪМВЛОУвѕМЋЧјШмвКГЪКьЩЋЃЌЖјбєМЋЧјШмвКГЪРЖЩЋЃЌЖдетИіЯжЯѓе§ШЗЕФНтЪЭЪЧ(ЁЁЁЁ)
ЂйвѕМЋЕчМЋЗДгІ2H++2eЃЃНH2ЁќЪЙc(OHЃ)>c(H+)ЁЁ
ЂкбєМЋ2Cu+4IЃЈD4eЃЃН2CuIЁ§+2I2ЃЛI2гіЕэЗлБфРЖЁЁ
ЂлбєМЋCuЃ2eЃЃНCu2+ЃЌCu2+ЯдРЖЩЋЁЁ
ЂмбєМЋ2IЈDЈD2eЃЃНI2ЃЌI2гіЕэЗлБфРЖ
A. ЂйЂкЁЁЁЁЁЁB. ЂйЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ C. ЂйЂмЁЁЁЁЁЁЁЁD. ЂлЂм
НтЮіЃКвдЪЏФЋЮЊвѕМЋЃЌCuЮЊбєМЋЕчНтKIШмвКЃЌЭЈЕчвЛЖЮЪБМфКѓЃЌбєМЋЧјШмвКГЪРЖЩЋЃЌЫЕУїгаI2ВњЩњЃЌI2гіЕэЗлЯдРЖЩЋЃЌМДбєМЋ2Cu+4IЃЈD4eЃЃН2CuIЁ§+I2ЃЛЖјвѕМЋЧјШмвКБфКьЃЌЫЕУїгаМюЩњГЩЃЌЗгЬЊЪдвКгіМюЯдКьЩЋЃЌдђга2H++2eЃЃНH2ЁќЪЙc(OHЃ)>c(H+)ЁЃзлЩЯЫљЪіЃЌБОЬтЕФД№АИЮЊA
Д№АИЃКA
16. гУЖшадЕчМЋЕчНтM(NO3)xЕФЫЎШмвКЃЌЕБвѕМЋЩЯдіжиagЪБЃЌдкбєМЋЩЯЭЌЪБВњЩњbLбѕЦј(БъзМзДПі)ЃЌДгЖјПЩжЊMЕФЯрЖддзгжЪСПЮЊ
гУЖшадЕчМЋЕчНтM(NO3)xЕФЫЎШмвКЃЌЕБвѕМЋЩЯдіжиagЪБЃЌдкбєМЋЩЯЭЌЪБВњЩњbLбѕЦј(БъзМзДПі)ЃЌДгЖјПЩжЊMЕФЯрЖддзгжЪСПЮЊ
A.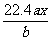 ЁЁЁЁЁЁЁЁ BЃЎ
ЁЁЁЁЁЁЁЁ BЃЎ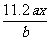 ЁЁЁЁЁЁЁЁЁЁ CЃЎ
ЁЁЁЁЁЁЁЁЁЁ CЃЎ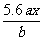 ЁЁЁЁЁЁЁЁ DЃЎ
ЁЁЁЁЁЁЁЁ DЃЎ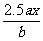
НтЮіЃКгУЖшадЕчМЋЕчНтЯѕЫсбЮШмвКЪБЃЌСНМЋЗЂЩњЕФЗДгІЗжБ№ЪЧЃКбєМЋ4OHЃЃ4eЃ====2H2O+O2ЁќЃЌвѕМЋMx++xeЃ====MЃЛЩшmЮЊMЕФЯрЖддзгжЪСПЃЌИљОнЕчзгЪиКудРэЃЌЕУЃК
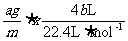
m=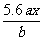 ЁЃ
ЁЃ
Д№АИЃКC
15.гУЖшадЕчМЋЪЕЯжЕчНтЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ
A.ЕчНтЯЁСђЫсШмвКЃЌЪЕжЪЩЯЪЧЕчНтЫЎЃЌЙЪШмвКpHВЛБф
B.ЕчНтЯЁЧтбѕЛЏФЦШмвКЃЌвЊЯћКФOHЃЃЌЙЪШмвКpHМѕаЁ
C.ЕчНтСђЫсФЦШмвКЃЌдквѕМЋЩЯКЭбєМЋЩЯЮіГіВњЮяЕФЮяжЪЕФСПжЎБШЮЊ1ЁУ2
D.ЕчНтТШЛЏЭШмвКЃЌдквѕМЋЩЯКЭбєМЋЩЯЮіГіВњЮяЕФЮяжЪЕФСПжЎБШЮЊ1ЁУ1
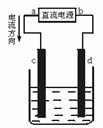
14.гвЭМЪЧЕчНтCuCl2ШмвКЕФзАжУЃЌЦфжаcЁЂdЮЊЪЏФЋЕчМЋЁЃдђЯТСагаЙиЕФХаЖЯе§ШЗЕФЪЧ
A.aЮЊИКМЋЁЂbЮЊе§МЋ
 B.aЮЊбєМЋЁЂbЮЊвѕМЋ
B.aЮЊбєМЋЁЂbЮЊвѕМЋ
C.ЕчНтЙ§ГЬжаЃЌdЕчМЋжЪСПдіМг
D.ЕчНтЙ§ГЬжаЃЌТШРызгХЈЖШВЛБф
НтЮіЃКОнЕчСїЕФЗНЯђХаЖЯaЮЊе§МЋЃЌbЮЊИКМЋЃЌcЮЊбєМЋЃЌdЮЊвѕМЋЁЃЕчНтCuCl2ШмвКЕчМЋЗДгІЪНЮЊЃКбєМЋ(cЕчМЋ)2ClЃЃ2eЃ====Cl2ЁќЃЌвѕМЋ(dЕчМЋ)Cu2++2eЃ====CuЃЌЙЪCе§ШЗЁЃ
Д№АИЃКC
13ЃЎдквЛШнЦїжаЗХШыКЃЫЎЃЌМИжжЬњжЦЦЗдкЦфжаБЛИЏЪДЕФЫйТЪгЩПьЕНТ§ЕФЫГађЪЧ(ЁЁ )
ЂйЬњЁЁЁЁЁЁЁЁ ЂкЖЦЮ§ЕФЬњЁЁЁЁЁЁЁЁ ЂлЖЦаПЕФЬњЁЁЁЁЁЁ ЂмЖЦЭЕФЬњ
AЃЎЂм>Ђк>Ђй>ЂлЁЁЁЁ ЁЁЁЁЁЁЁЁBЃЎЂк>Ђй>Ђл>Ђм
CЃЎЂм>Ђк>Ђл>ЂйЁЁЁЁЁЁЁЁЁЁЁЁ DЃЎЂл>Ђк>Ђм>Ђй
НтЮіЃКБОЬтПМВьЕФжЊЪЖЕуЪЧН№ЪєЕФатЪДЕФдвђМАЭтНчЕФгАЯьЃЎЂкЁЂЂлЁЂЂмЕФзАжУЮЊдЕчГизАжУЃЎЂлжаЬњЮЊе§МЋЃЌБЛБЃЛЄЃЛЂкЁЂЂмжаЬњЮЊИКМЋЃЌОљБЛИЏЪДЃЌЕЋЯрЖдРДЫЕЬњгыЭЕФН№ЪєЛюЖЏадНЯЬњКЭЮ§ЕФВюБ№ДѓЃЌЫљвдЬњвЛЭдЕчГижаЕФЬњБЛИЏЪДЕФПьвЛаЉЃЌЂйжаЕФЬњВЛДПЖјЗЂЩњдЕчГиЕФЗДгІЃЎ
Д№АИЃКA
12. гУВЌзїЕчМЋЕчНтвЛЖЈХЈЖШЕФЯТСаЮяжЪЕФЫЎШмвКЃЌЕчНтНсЪјКѓЃЌЯђЪЃгрЕчНтвКжаМгЪЪСПЫЎЃЌФмЪЙШмвККЭЕчНтЧАЯрЭЌЕФЪЧ(ЁЁЁЁ )
гУВЌзїЕчМЋЕчНтвЛЖЈХЈЖШЕФЯТСаЮяжЪЕФЫЎШмвКЃЌЕчНтНсЪјКѓЃЌЯђЪЃгрЕчНтвКжаМгЪЪСПЫЎЃЌФмЪЙШмвККЭЕчНтЧАЯрЭЌЕФЪЧ(ЁЁЁЁ )
A. AgNO3ЁЁЁЁ B. H2SO4ЁЁЁЁC. NaOHЁЁЁЁЁЁЁЁЁЁ D. NaCl
НтЮіЃКЩѓЬтжЊЕчМЋЮЊЖшадЕчМЋЃЌЙиМќОфЪЧЁАЯђЪЃгрЕчНтвКжаМгЪЪСПЫЎЃЌФмЪЙШмвККЭЕчНтЧАЯрЭЌЁБЃЌФЧОЭЪЧвЊевбЁЯюжаЕчНтЪБжЛЯћКФСЫЫЎЕФЁЃ
A. AgNO3ШмвКЕчНтЪБЃЌAg+ЗХЕчЃЌOHЃЗХЕчЃЌВЛЪЧЕчНтЫЎ
B. H2SO4ШмвКЕчНтЪБH+ЗХЕчЃЌOHЃЗХЕчЃЌЪЕжЪЪЧЕчНтЫЎ
C. NaOHШмвКЕчНтЪБH+ЗХЕчЃЌOHЃЗХЕчЃЌЪЕжЪЩЯЪЧЕчНтЫЎ
D. NaClШмвКЕчНтЪБЃЌClЃЗХЕчЃЌH+ЗХЕчЃЌВЛЪЧЕчНтЫЎ
Д№АИЃКB C
11.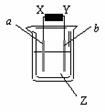 ШчЭМЫљЪОЃЌXЁЂYЗжБ№ЪЧжБСїЕчдДЕФСНМЋЃЌЭЈЕчКѓЗЂЯжaМЋАхжЪСПдіМгЃЌbМЋАхДІгаЮоЩЋЮоЮЖЕФЦјЬхЗХГіЁЃЗћКЯетвЛЧщПіЕФЪЧ(ЁЁ )
ШчЭМЫљЪОЃЌXЁЂYЗжБ№ЪЧжБСїЕчдДЕФСНМЋЃЌЭЈЕчКѓЗЂЯжaМЋАхжЪСПдіМгЃЌbМЋАхДІгаЮоЩЋЮоЮЖЕФЦјЬхЗХГіЁЃЗћКЯетвЛЧщПіЕФЪЧ(ЁЁ )
ЁЁaМЋАхЁЁ bМЋАх ЁЁ XЕчМЋ ЁЁЁЁZШмвК
A. Zn ЁЁC ЁЁЁЁИКМЋ ЁЁЁЁCuSO4
B. C ЁЁ C ЁЁЁЁИКМЋ ЁЁЁЁNaOH
C. Ag ЁЁFe ЁЁ е§МЋ ЁЁЁЁAgNO3
D. Cu ЁЁC ЁЁЁЁИКМЋ ЁЁЁЁCuCl2
10.
 ФГбЇЩњЯыжЦзївЛжжМвгУЛЗБЃаЭЯћЖОвКЗЂЩњЦїЃЌгУЪЏФЋзїЕчМЋЕчНтБЅКЭТШЛЏФЦШмвКЃЌЭЈЕчЪБЃЌЮЊЪЙCl2БЛЭъШЋЮќЪеЃЌжЦЕУгаНЯЧПЩБОњФмСІЕФЯћЖОвКЃЌЩшМЦСЫШчЭМЕФзАжУЃЌдђЖдЕчдДЕчМЋУћГЦКЭЯћЖОвКЕФжївЊГЩЗжХаЖЯе§ШЗЕФЪЧ(ЁЁ )
ФГбЇЩњЯыжЦзївЛжжМвгУЛЗБЃаЭЯћЖОвКЗЂЩњЦїЃЌгУЪЏФЋзїЕчМЋЕчНтБЅКЭТШЛЏФЦШмвКЃЌЭЈЕчЪБЃЌЮЊЪЙCl2БЛЭъШЋЮќЪеЃЌжЦЕУгаНЯЧПЩБОњФмСІЕФЯћЖОвКЃЌЩшМЦСЫШчЭМЕФзАжУЃЌдђЖдЕчдДЕчМЋУћГЦКЭЯћЖОвКЕФжївЊГЩЗжХаЖЯе§ШЗЕФЪЧ(ЁЁ )
AЁЂaЮЊе§МЋЃЌbЮЊИКМЋЃЛNaClOКЭNaCl
BЁЂaЮЊИКМЋЃЌbЮЊе§МЋЃЛNaClOКЭNaCl
CЁЂaЮЊбєМЋЃЌbЮЊвѕМЋЃЛHClOКЭNaCl
DЁЂaЮЊвѕМЋЃЌbЮЊбєМЋЃЛHClOКЭNaClЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
НтЮіЃКЕчНтNaClШмвКЕУЕНCl2ЁЂH2ЁЂNaOHЪЧБШНЯЪьЯЄЕФЃЌНтЬтЙиМќЪЧДгЪЕЮяМђЭМжаЛёШЁаХЯЂЃЌЮЊСЫжЦНЯЧПЩБОњФмСІЕФЯћЖОМСЃЌгжВЛЪЙCl2внЩЂЮлШОЛЗОГЁЃвђДЫCl2гІгЩЯТЖЫЕчМЋЩЯВњЩњЃЌдкЩЯвнЙ§ГЬжаЃЌБЛNaOHНЯГфЗжЮќЪеЃЌВХФмЕУЕНгаНЯЧПЩБОњФмСІЕФNaClOЃЌЫљвдbгІЪЧжБСїЕчдДе§МЋЃЌBбЁЯюЗћКЯЬтвЊЧѓ ЁЃ
Д№АИЃКB
9.ЬьНђЪЧЮвЙњбаЗЂКЭЩњВњяЎРызгЕчГиЕФживЊЛљЕиЁЃяЎРызгЕчГие§МЋВФСЯЪЧКЌяЎЕФЖўбѕ ЛЏюм(LiCoO2)ЃЌГфЕчЪБLiCoO2жаLiБЛбѕЛЏЃЌLi+ЧЈвЦВЂвддзгаЮЪНЧЖШыЕчГиИКМЋВФСЯЬМ(C6)жаЃЌвдLiC6БэЪОЁЃЕчГиЗДгІЮЊLiCoO2 + C6
ЛЏюм(LiCoO2)ЃЌГфЕчЪБLiCoO2жаLiБЛбѕЛЏЃЌLi+ЧЈвЦВЂвддзгаЮЪНЧЖШыЕчГиИКМЋВФСЯЬМ(C6)жаЃЌвдLiC6БэЪОЁЃЕчГиЗДгІЮЊLiCoO2 + C6 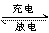 CoO2
+ LiC6 ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁ )
CoO2
+ LiC6 ЃЌЯТСаЫЕЗЈе§ШЗЕФЪЧ(ЁЁ )
AЃЎГфЕчЪБЃЌЕчГиЕФИКМЋЗДгІЮЊ LiC6 Ѓ eЃ == Li ++ C6
BЃЎЗХЕчЪБЃЌЕчГиЕФе§МЋЗДгІЮЊ CoO2 + Li+ + eЃ == LiCoO2 ЃЌ
CЃЎєШЫсЁЂДМЕШКЌЛюЦУЧтЕФгаЛњЮяПЩгУзїяЎРызгЕчГиЕФЕчНтжЪ
DЃЎяЎРызгЕчГиЕФБШФмСП(ЕЅЮЛжЪСПЪЭЗХЕФФмСП)ЕЭ
8.НЋЗжБ№ЪЂгаШлШкЕФТШЛЏМиЁЂТШЛЏУОЁЂбѕЛЏТСЕФШ§ИіЕчНтВлДЎСЊЃЌдквЛЖЈЬѕМўЯТЭЈЕчвЛЖЮЪБМфКѓЃЌЮіГіМиЁЂУОЁЂТСЕФЮяжЪЕФСПжЎБШЮЊ(ЁЁЁЁ )
A.1ЁУ2ЁУ3ЁЁЁЁ ЁЁЁЁ B.3ЁУ2ЁУ1ЁЁ ЁЁЁЁЁЁC.6ЁУ3ЁУ1ЁЁЁЁ ЁЁ ЁЁD.6ЁУ3ЁУ2
НтЮіЃКШ§ИіЕчНтВлЭЈЙ§ЕФЕчзгЪ§ЯрЕШЃЌЩшЖМЭЈЙ§6 molЕчзг(ДЫЮЊВЮееЪ§ЗЈ)ЃЌдђЮіГіН№ЪєМиЁЂУОЁЂТСЕФЮяжЪЕФСПЗжБ№ЮЊ6 molЁЂ3 molЁЂ2 molЃЌЫљвдБШЮЊ6ЁУ3ЁУ2ЁЃ
Д№АИЃКD
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com