
7£® X”¢Y”¢Z”¢M“ś±ķĖÄÖÖ½šŹōŌŖĖŲ£¬½šŹōXŗĶZÓƵ¼ĻßĮ¬½Ó·ÅČėĻ”ĮņĖįÖŠŹ±£¬XČܽā£¬Z¼«ÉĻÓŠĒāĘų·Å³ö£»Čōµē½āY2+ŗĶZ2+¹²“ęµÄČÜŅŗŹ±£¬YĻČĪö³ö£»ÓÖÖŖM2+µÄŃõ»ÆŠŌĒæÓŚY2+”£ŌņÕāĖÄÖÖ½šŹōµÄ»ī¶ÆŠŌÓÉĒæµ½ČõµÄĖ³ŠņĪŖ(”” )
A.X>Z>Y>M”” ”””””” B.X>Y>Z>M”””””” C.M>Z>X>Y”””””””””” D.X>Z>M>Y
½āĪö£ŗ½šŹōXŗĶZÓƵ¼ĻßĮ¬½Ó·ÅČėĻ”H2SO4ÖŠ£¬ŠĪ³ÉŌµē³Ų£¬XČܽāĖµĆ÷½šŹō»ī¶ÆŠŌX>Z£»µē½āY2+ŗĶZ2+¹²“ęµÄČÜŅŗŹ±£¬YĻČĪö³ö£¬Ōņ½šŹō»ī¶ÆŠŌZ>Y£»Ąė×ÓµÄŃõ»ÆŠŌŌ½Ē棬Ę䵄֏µÄ½šŹō»ī¶ÆŠŌŌ½Čõ£¬Ōņ½šŹō»ī¶ÆŠŌY>M£¬ĖłŅŌÕżČ·“š°øĪŖA”£
“š°ø£ŗA
6£®øÖĢś·¢Éśµē»ÆѧøÆŹ“Ź±£¬øŗ¼«·¢ÉśµÄ·“Ó¦ŹĒ(”” )
A.2H++2e£ H2
H2
B.2H2O+O2+4e£ 4OH£
4OH£
C.Fe£2e£ Fe2+
Fe2+
D.4OH££4e£ 2H2O+O2
2H2O+O2
½āĪö£ŗøÖĢś·¢Éśµē»ÆѧøÆŹ“Ź±£¬Ģś×÷øŗ¼«±»Ńõ»Æ£¬µē¼«·½³ĢŹ½ĪŖ£ŗFe£2e£===Fe2+”£
“š°ø£ŗC
5£® Ėę×ÅČĖĆĒÉś»īÖŹĮæµÄ²»¶ĻĢįøߣ¬·Ļµē³Ų±ŲŠė½ųŠŠ¼ÆÖŠ“¦ĄķµÄĪŹĢā±»Ģįµ½ŅéŹĀČÕ³Ģ£¬ĘäŹ×ŅŖŌŅņŹĒ(”” )
Ėę×ÅČĖĆĒÉś»īÖŹĮæµÄ²»¶ĻĢįøߣ¬·Ļµē³Ų±ŲŠė½ųŠŠ¼ÆÖŠ“¦ĄķµÄĪŹĢā±»Ģįµ½ŅéŹĀČÕ³Ģ£¬ĘäŹ×ŅŖŌŅņŹĒ(”” )
A.ĄūÓƵē³ŲĶāæĒµÄ½šŹō²ÄĮĻ
B.·ĄÖ¹µē³ŲÖŠ¹Æ”¢ļÓŗĶĒ¦µČÖŲ½šŹōĄė×Ó¶ŌĶĮČĄŗĶĖ®Ō“µÄĪŪČ¾
C.²»Ź¹µē³ŲÖŠÉųŠ¹µÄµē½āŅŗøÆŹ“ĘäĖūĪļĘ·
D.»ŲŹÕĘäÖŠµÄŹÆÄ«µē¼«
½āĪö£ŗĖę×ÅÉś²śµÄ·¢Õ¹ŗĶČĖĆĒÉś»īĖ®Ę½µÄĢįøߣ¬»·¾³ĪŪČ¾ŗĶ»·±£ĪŹĢāŅŃŌ½Ą“Ō½ŹÜµ½ČĖĆĒÖŲŹÓ£¬·Ļµē³ŲÖŠŗ¬ÓŠ¹ÆµČ¶ąÖÖÖŲ½šŹōĄė×Ó£¬¼«Ņ׶Ō»·¾³Ōģ³ÉĪŪČ¾”£
“š°ø£ŗB
4£®100 mLÅضČĪŖ2 mol”¤L£1µÄŃĪĖįøś¹żĮæµÄŠæʬ·“Ó¦£¬ĪŖ¼Óæģ·“Ó¦ĖŁĀŹ£¬ÓÖ²»Ó°ĻģÉś³ÉĒāĘųµÄ×ÜĮ棬æɲÉÓƵķ½·ØŹĒ(”” )
A.¼ÓČėŹŹĮæµÄ3 mol”¤L£1µÄŃĪĖį
B.¼ÓČėŹżµĪĀČ»ÆĶČÜŅŗ
C.¼ÓČėŹŹĮæÕōĮóĖ®
D.¼ÓČėŹŹĮæµÄĀČ»ÆÄĘČÜŅŗ
3£®ĶʬŗĶŠæʬÓƵ¼ĻßĮ¬½Óŗó²åČėĻ”ĮņĖįÖŠ£¬ŠæʬŹĒ(”” )
A.Ņõ¼«”””””””””” B.Õż”” ¼«”””””””””””” C.Ńō¼«”””””””””””” D.øŗ¼«
½āĪö£ŗµē½ā³ŲµÄĮ½¼«·Ö±šĆüĆūĪŖŅõŃō¼«£¬Ōµē³ŲµÄĮ½¼«·Ö±šĆüĆūĪŖÕżøŗ¼«”£ĶʬŗĶŠæʬÓƵ¼ĻßĮ¬½Óŗó²åČėĻ”ĮņĖįÖŠŠĪ³ÉĮĖŌµē³Ų£¬ĘäÖŠŠæŹ§µē×Ó×÷Ōµē³ŲµÄøŗ¼«”£
“š°ø£ŗD
2£®¼ŅÓĆ³“²ĖĢś¹ųÓĆĖ®ĒåĻ“·ÅÖĆŗ󣬳öĻÖŗģ×ŲÉ«µÄŠā°ß£¬ŌŚ“Ė±ä»Æ¹ż³ĢÖŠ²»·¢ÉśµÄ»Æѧ·“Ó¦ŹĒ(”” )
A.4Fe(OH)2+2H2O+O2===4Fe(OH)3”ż
B.2Fe+2H2O+O2===2Fe(OH)2”ż
C.2H2O+O2+4e£===4OH£
D.Fe£3e£===Fe3+
½āĪö£ŗĻ“¹żµÄĢś¹ųŌŚæÕĘųÖŠ·ÅÖĆ,æÉ·¢ÉśĪüŃõøÆŹ“”£øŗ¼«·¢ÉśµÄ·“Ó¦ĪŖ2Fe£4e£==2Fe2+£¬Õż¼«·¢ÉśµÄ·“Ó¦ĪŖ2H2O+O2+4e£===4OH££¬×Ü·“Ó¦Ź½ĪŖ2Fe+2H2O+O2===2Fe(OH)2£¬¶ųFe(OH)2ÓÖ±»O2Ńõ»ÆĪŖŗģŗÖÉ«µÄFe(OH)3”£
“š°ø£ŗD
1£®øÖĢś·¢ÉśĪüŃõøÆŹ“Ź±£¬Õż¼«ÉĻ·¢ÉśµÄµē¼«·“Ó¦ŹĒ(”” )
A.2H++2e£===H2”””””””””””””””””””” B.Fe2++2e£===Fe
C.2H2O+O2+4e£===4OH£”””””””””””””””””””””””””” D.Fe3++e£===Fe2+
½āĪö£ŗøÖĢś·¢ÉśĪüŃõøÆŹ“£¬Õż¼«ÉĻŹĒŃõĘųµĆµē×Ó±»»¹ŌµÄ·“Ó¦£ŗ2H2O+O2+4e£===4OH£”£
“š°ø£ŗC
3£®ĀČ¼ī¹¤Ņµ
(1)µē½ā±„ŗĶŹ³ŃĪĖ®·“Ó¦ŌĄķ
¢ŁŹµŃé²½Öč
°“Ķ¼×°ÖĆ£¬ŌŚUŠĪ¹ÜĄļµ¹Čė±„ŗĶŹ³ŃĪĖ®£¬²åČėŅ»øłŹÆÄ«°ō×÷Ńō¼«£¬Ņ»øłĢś°ō×÷Ņõ¼«”£Ķ¬Ź±ŌŚĮ½±ß¹ÜÖŠø÷µĪČė¼øµĪ·ÓĢŖŹŌŅŗ£¬²¢ÓĆŹŖČóµÄµā»Æ¼Ųµķ·ŪŹŌÖ½¼ģŃéŃō¼«·Å³öµÄĘųĢ唣½ÓĶØÖ±Į÷µēŌ“ŗó£¬×¢Ņā¹ÜÄŚ·¢ÉśµÄĻÖĻó”£
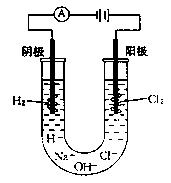
¢ŚŹµŃéĻÖĻó
Ńō¼«ÉĻÓŠĘųÅŻŅŻ³ö£¬ĘųĢå³Ź»ĘĀĢÉ«£¬ÓŠ“Ģ¼¤ŠŌĘųĪ¶£¬Ź¹ŹŖČóµÄµā»Æ¼Ųµķ·ŪŹŌÖ½±äĪŖĄ¶É«£¬Ńō¼«ĒųČÜŅŗÓÉĪŽÉ«±äĪŖ»ĘĀĢÉ«”£Ņõ¼«ÉĻÓŠĘųÅŻŅŻ³ö£¬ĘųĢåĪŽÉ«”¢ĪŽĪ¶”£Ņõ¼«ĒųČÜŅŗÓÉĪŽÉ«±äĪŖĒ³ŗģÉ«£¬ŗģÉ«Öš½„¼ÓÉī”¢ĒųÓņÖš½„Ą©“ó”£
¢ŪŹµŃé½įĀŪ
ÓƶčŠŌ²ÄĮĻ×÷Ńō¼«£¬µē½āŹ³ŃĪµÄ±„ŗĶČÜŅŗ£¬Éś³ÉCl2”¢H2ŗĶNaOH”£
Ńō¼«£ŗ2Cl££2e£=Cl2”ü(·ÅµēĖ³Šņ£ŗC l£>OH£)
l£>OH£)
Ņõ¼«£ŗ2H++2e£=H2”ü(·ÅµēĖ³Šņ£ŗH+>Na+)
ŌŚÉĻŹö·“Ó¦ÖŠ£¬ÓÉÓŚH+ŌŚŅõ¼«ÉĻµĆµ½µē×Ó¶ųÉś³ÉH2£¬ĘĘ»µĮĖø½½üµÄĖ®µÄµēĄėĘ½ŗā£¬“Ł½ųĮĖĖ®¼ĢŠųµēĄė£¬½į¹ūŅõ¼«ĒųČÜŅŗĄļOH£µÄÅضČŌö“ó¶ų³ŹĻÖ¼īŠŌ”£
×Ü·“Ó¦£ŗ2NaCl+2H2O 2NaOH+H2”ü+Cl2”ü
2NaOH+H2ӟ+Cl2ӟ
(2)Ąė×Ó½»»»Ä¤·ØÖĘÉÕ¼ī
¢ŁĄė×Ó½»»»Ä¤µē½ā²ŪµÄ×é³É
ÓÉŃō¼«(½šŹōīŃĶų)”¢Ņõ¼«(Ģ¼øÖĶų)”¢Ąė×Ó½»»»Ä¤”¢µē½ā²ŪæņŗĶµ¼µēĶ°ōµČ×é³É£¬µē½ā²ŪÓÉČōøÉøöµ„ŌŖ²Ū“®ĮŖ»ņ²¢ĮŖ×é³É”£ĻĀĶ¼±ķŹ¾Ņ»øöµ„ŌŖ²ŪµÄŹ¾ŅāĶ¼”£
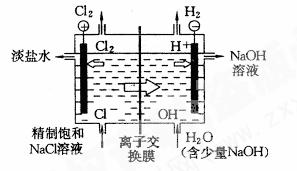
¢ŚŃōĄė×Ó½»»»Ä¤µÄ×÷ÓĆ
½«µē½ā²Ūøō³ÉŅõ¼«ŹŅŗĶŃō¼«ŹŅ£¬ĖüÖ»ŌŹŠķŃōĄė×Ó(Na+)Ķعż£¬¶ų×čÖ¹ŅõĄė×Ó(Cl£”¢OH£)ŗĶĘųĢåĶعż”£ÕāŃł¼ČÄÜ·ĄÖ¹Ņõ¼«²śÉśµÄH2ŗĶŃō¼«²śÉśµÄCl2Ļą»ģŗĻ¶ųŅżĘš±¬ÕØ£¬ÓÖÄܱÜĆāCl2ŗĶNaOH×÷ÓĆÉś³ÉNaClO¶ųÓ°ĻģÉÕ¼īµÄÖŹĮ攣
¢ŪĄė×Ó½»»»Ä¤·Øµē½āÖĘÉÕ¼īµÄÖ÷ŅŖÉś²śĮ÷³Ģ(ČēĻĀĶ¼)
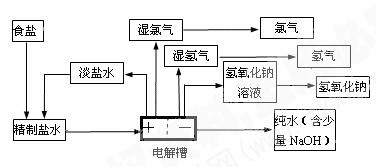
Ąż1”¢(2009ÉĻŗ£) ””ÓŅĶ¼×°ÖĆÖŠ£¬UŠĶ¹ÜÄŚĪŖŗģÄ«Ė®
””ÓŅĶ¼×°ÖĆÖŠ£¬UŠĶ¹ÜÄŚĪŖŗģÄ«Ė® £¬a”¢bŹŌ¹ÜÄŚ·Ö±šŹ¢ÓŠŹ³ŃĪĖ®ŗĶĀČ»Æļ§ČÜŅŗ£¬ø÷¼ÓČėÉśĢśæ飬·ÅÖĆŅ»¶ĪŹ±¼ä”£ĻĀĮŠÓŠ¹ŲĆčŹö“ķĪóµÄŹĒ
£¬a”¢bŹŌ¹ÜÄŚ·Ö±šŹ¢ÓŠŹ³ŃĪĖ®ŗĶĀČ»Æļ§ČÜŅŗ£¬ø÷¼ÓČėÉśĢśæ飬·ÅÖĆŅ»¶ĪŹ±¼ä”£ĻĀĮŠÓŠ¹ŲĆčŹö“ķĪóµÄŹĒ
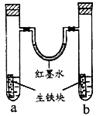
 A£®ÉśĢśæéÖŠµÄĢ¼ŹĒŌµē³ŲµÄÕż¼«
A£®ÉśĢśæéÖŠµÄĢ¼ŹĒŌµē³ŲµÄÕż¼«
 B£®ŗģÄ«Ė®ÖłĮ½±ßµÄŅŗĆę±äĪŖ×óµĶÓŅøß
B£®ŗģÄ«Ė®ÖłĮ½±ßµÄŅŗĆę±äĪŖ×óµĶÓŅøß
 C£®Į½ŹŌ¹ÜÖŠĻąĶ¬µÄµē¼«·“Ó¦Ź½ŹĒ£ŗ
C£®Į½ŹŌ¹ÜÖŠĻąĶ¬µÄµē¼«·“Ó¦Ź½ŹĒ£ŗ
 D£®aŹŌ¹ÜÖŠ·¢ÉśĮĖĪüŃõøÆŹ“£¬bŹŌ¹ÜÖŠ·¢ÉśĮĖĪöĒāøÆŹ“
D£®aŹŌ¹ÜÖŠ·¢ÉśĮĖĪüŃõøÆŹ“£¬bŹŌ¹ÜÖŠ·¢ÉśĮĖĪöĒāøÆŹ“
[“š°ø]B
[½āĪö]ÉśĢśæéŌŚŹ³ŃĪĖ®ŗĶĀČ»Æļ§ČÜŅŗÖŠ¾łÄÜŠĪ³ÉŌµē³Ų£¬ÉśĢśæéÖŠµÄĢ¼ĪŖÕż¼«£¬ĢśĪŖøŗ¼«£¬µē¼«·“Ó¦Ź½ĪŖ £¬ĖłŅŌA”¢C¶Ō”£ĘäÖŠĀČ»Æļ§ČÜŅŗĻŌĖįŠŌ£¬·¢ÉśĪöĒāøÆŹ“£¬¶ųŹ³ŃĪĖ®ĻŌÖŠŠŌ£¬·¢ÉśĪüŃõøÆŹ“£¬ĖłŅŌĻąĶ¬Ģõ¼žĻĀ£¬ĪöĒāøÆŹ“µÄĖŁĀŹ±ŅĪüŃõøÆŹ“µÄæģ£¬ĖłŅŌŗģÄ«Ė®Į½±ßŅŗĆę×óøßÓŅµĶ£¬ĖłŅŌB“ķD¶Ō”£
£¬ĖłŅŌA”¢C¶Ō”£ĘäÖŠĀČ»Æļ§ČÜŅŗĻŌĖįŠŌ£¬·¢ÉśĪöĒāøÆŹ“£¬¶ųŹ³ŃĪĖ®ĻŌÖŠŠŌ£¬·¢ÉśĪüŃõøÆŹ“£¬ĖłŅŌĻąĶ¬Ģõ¼žĻĀ£¬ĪöĒāøÆŹ“µÄĖŁĀŹ±ŅĪüŃõøÆŹ“µÄæģ£¬ĖłŅŌŗģÄ«Ė®Į½±ßŅŗĆę×óøßÓŅµĶ£¬ĖłŅŌB“ķD¶Ō”£
Ąż2”¢ Li-SOCl2µē³ŲæÉÓĆÓŚŠÄŌąĘš²«Ę÷”£øƵē³ŲµÄµē¼«²ÄĮĻ·Ö±šĪŖļ®ŗĶĢ¼£¬µē½āŅŗŹĒLiAlCl4-SOCl2”£µē³ŲµÄ×Ü·“Ó¦æɱķŹ¾ĪŖ£ŗ4Li+2SOCl2 = 4LiCl +S +SO2”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
(1)µē³ŲµÄøŗ¼«²ÄĮĻĪŖ”””””””””””” £¬·¢ÉśµÄµē¼«·“Ó¦ĪŖ”””””””””””””””” £»
(2)µē³ŲÕż¼«·¢ÉśµÄµē¼«·“Ó¦ĪŖ”””””””””””””””””””” £»
(3)SOCl2Ņ×»Ó·¢£¬ŹµŃéŹŅÖŠ³£ÓĆNaOHČÜŅŗĪüŹÕSOCl2£¬ÓŠNa2SO3ŗĶNaClÉś³É”£ Čē¹ū°ŃÉŁĮæĖ®µĪµ½SOCl2ÖŠ£¬ŹµŃéĻÖĻóŹĒ”””””””””””” £¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ”””””””””””” £»
(4)×é×°øƵē³Ų±ŲŠėŌŚĪŽĖ®”¢ĪŽŃõµÄĢõ¼žĻĀ½ųŠŠ£¬ŌŅņŹĒ”” ”””””””””””””””””””£
[“š°ø]

[½āĪö]£ŗ(1)LiŌŚµē³Ų·“Ó¦ÖŠŹ§µē×Ó,øł¾Żµē×ÓĮ÷³ö µÄŅ»¼«ŹĒøŗ¼«,¹ŹLiŹĒøŗ¼«,·¢ÉśµÄµē¼«·“Ó¦Ź½ĪŖLi-e-=Li+£»(2)SOCl2µē³Ų·“Ó¦ÖŠµĆµē×ÓĪŖÕż¼«·“Ó¦Īļ£¬Ęäµē¼«·“Ó¦Ź½ĪŖ
µÄŅ»¼«ŹĒøŗ¼«,¹ŹLiŹĒøŗ¼«,·¢ÉśµÄµē¼«·“Ó¦Ź½ĪŖLi-e-=Li+£»(2)SOCl2µē³Ų·“Ó¦ÖŠµĆµē×ÓĪŖÕż¼«·“Ó¦Īļ£¬Ęäµē¼«·“Ó¦Ź½ĪŖ
2 SOCl2+4 e-=4Cl-+S+SO2
(3) SOCl2ÓėĖ®ĒæĮŅĖ®½āÉś³É¶žŃõ»ÆĮņŗĶHCl£¬HClÓėĖ®ŠĪ³É“óĮæµÄ°×Īķ£¬¹Ź³öĻÖ°×ĪķĶ¬Ź±Īŵ½ŲŻ¼¤ŠŌĘųĪ¶µÄĘųĢåÉś³É”£·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖSOCl2+H2O=2HCl”ü+ SO2”ü
(4)ÓÉÓŚļ®ŹĒ»īĘĆµÄ½šŹōÓėĖ®”¢ŃõµČ·“Ó¦£¬SOCl2ÄÜÓėĖ®·“Ó¦£¬ĖłŅŌ×é×°øƵē³Ų±ŲŠėŌŚĪŽĖ®”¢ĪŽŃõµÄĢõ¼žĻĀ½ųŠŠ”£
Ąż3”¢(2009¹ć¶«)10£®³öĶĮµÄĪżĒąĶ(ĶĪżŗĻ½š)ĪÄĪļ³£ÓŠCu2(OH)3Clø²øĒŌŚĘä±ķĆę”£ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®ĪżĒąĶµÄČŪµć±Č“æĶøß
B£®ŌŚ×ŌČ»»·¾³ÖŠ£¬ĪżĒąĶÖŠµÄĪż¶ŌĶĘš±£»¤×÷ÓĆ
C£®ĪżĒąĶĪÄĪļŌŚ³±ŹŖ»·¾³ÖŠµÄøÆŹ“±ČøÉŌļ»·¾³ÖŠæģ
D£®Éś³ÉCu2(OH)3Clø²øĒĪļŹĒµē»ÆѧøÆŹ“¹ż³Ģ£¬µ«²»ŹĒ»Æѧ·“Ó¦¹ż³Ģ
[“š°ø]BC
[½āĪö]ĪżĒąĶŗĻ½š¾ßÓŠŗĻ½šµÄĢŲŠŌ£¬ČŪµć±ČČĪŗĪŅ»Ö֓潚ŹōµÄµĶ£¬A“ķ£»ÓÉÓŚĪżµÄ»īĘĆŠŌĒæÓŚĶ£¬¹ŹŌŚŠĪ³Éµē»ÆѧøÆŹ“Ź±£¬Īż¶ŌĶĘšµ½ĮĖ±£»¤×÷ÓĆ£¬BÕżČ·£»³±ŹŖµÄ»·¾³øüĄūÓŚ½šŹōµÄµē»ÆѧøÆŹ“£¬CÕżČ·£»µē»ÆѧøÆŹ“¹ż³ĢÖŠÉę¼°µē×ÓµÄ×ŖŅĘ£¬ÓÖÓŠŠĀĪļÖŹÉś³É£¬ŹōÓŚ»Æѧ·“Ó¦¹ż³Ģ£¬D“ķ”£
Ąż4”¢(2009ø£½Ø) 11. æŲÖĘŹŹŗĻµÄĢõ¼ž£¬½«·“Ó¦
11. æŲÖĘŹŹŗĻµÄĢõ¼ž£¬½«·“Ó¦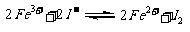
Éč¼Ę³ÉČēÓŅĶ¼ĖłŹ¾µÄŌµē³Ų”£ĻĀĮŠÅŠ¶Ļ²»ÕżČ·µÄŹĒ
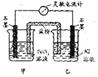
 ”””” A. ·“Ó¦æŖŹ¼Ź±£¬ŅŅÖŠŹÆÄ«µē¼«ÉĻ·¢ÉśŃõ»Æ·“Ó¦
”””” A. ·“Ó¦æŖŹ¼Ź±£¬ŅŅÖŠŹÆÄ«µē¼«ÉĻ·¢ÉśŃõ»Æ·“Ó¦
 ”””” B. ·“Ó¦æŖŹ¼Ź±£¬¼×ÖŠŹÆÄ«µē¼«ÉĻFe3+±»»¹Ō
”””” B. ·“Ó¦æŖŹ¼Ź±£¬¼×ÖŠŹÆÄ«µē¼«ÉĻFe3+±»»¹Ō
 ”””” C. µēĮ÷¼Ę¶ĮŹżĪŖĮ揱£¬·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬
”””” C. µēĮ÷¼Ę¶ĮŹżĪŖĮ揱£¬·“Ó¦“ļµ½»ÆŃ§Ę½ŗāדĢ¬
 ”””” D. µēĮ÷¼Ę¶ĮŹżĪŖĮćŗó£¬ŌŚ¼×ÖŠČÜČėFeCl2¹Ģ¶Ø£¬ŅŅÖŠŹÆÄ«µē¼«ĪŖøŗ¼«
”””” D. µēĮ÷¼Ę¶ĮŹżĪŖĮćŗó£¬ŌŚ¼×ÖŠČÜČėFeCl2¹Ģ¶Ø£¬ŅŅÖŠŹÆÄ«µē¼«ĪŖøŗ¼«
 Ąż5”¢(2009Õć½)12.ŹŠ³”ÉĻ¾³£¼ūµ½µÄ±ź¼ĒĪŖLi-ionµÄµē³Ų³ĘĪŖ”°ļ®Ąė×Óµē³Ų”±”£ĖüµÄøŗ¼«²ÄĮĻŹĒ½šŹōļ®ŗĶĢ¼µÄø“ŗĻ²ÄĮĻ(Ģ¼×÷ĪŖ½šŹōļ®µÄŌŲĢå)£¬µē½āÖŹĪŖŅ»ÖÖÄÜ“«µ¼Li
Ąż5”¢(2009Õć½)12.ŹŠ³”ÉĻ¾³£¼ūµ½µÄ±ź¼ĒĪŖLi-ionµÄµē³Ų³ĘĪŖ”°ļ®Ąė×Óµē³Ų”±”£ĖüµÄøŗ¼«²ÄĮĻŹĒ½šŹōļ®ŗĶĢ¼µÄø“ŗĻ²ÄĮĻ(Ģ¼×÷ĪŖ½šŹōļ®µÄŌŲĢå)£¬µē½āÖŹĪŖŅ»ÖÖÄÜ“«µ¼Li µÄøß·Ö×Ó²ÄĮĻ”£ÕāÖÖļ®Ąė×Óµē³ŲµÄµē³Ų·“Ó¦ĪŖ£ŗ
µÄøß·Ö×Ó²ÄĮĻ”£ÕāÖÖļ®Ąė×Óµē³ŲµÄµē³Ų·“Ó¦ĪŖ£ŗ
””””””””””””””””””
Li+2Li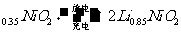
ĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ
A£®·ÅµēŹ±£¬øŗ¼«µÄµē¼«·“Ó¦Ź½£ŗLi-e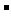 =Li
=Li
B£®³äµēŹ±£¬Li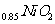 ¼Č·¢ÉśŃõ»Æ·“Ó¦ÓÖ·¢Éś»¹Ō·“Ó¦
¼Č·¢ÉśŃõ»Æ·“Ó¦ÓÖ·¢Éś»¹Ō·“Ó¦
C£®øƵē³Ų²»ÄÜÓĆĖ®ČÜŅŗ×÷ĪŖµē½āÖŹ
D£®·Åµē¹ż³ĢÖŠLi Ļņøŗ¼«ŅʶÆ
Ļņøŗ¼«ŅʶÆ
[“š°ø]D
[½āĪö]AĻī£¬Li“ÓĮć¼ŪÉżÖĮÕż¼Ū£¬Ź§Č„µē×Ó£¬×÷ĪŖøŗ¼«£¬ÕżČ·£»BĻī£¬·“Ó¦ÄęĻņ½ųŠŠŹ±”£·“Ó¦ĪļÖ»ÓŠŅ»ÖÖ£¬¹Ź»ÆŗĻ¼Ū¼ČÓŠÉż£¬ÓÖÓŠ½µ£¬ĖłŅŌ¼Č·¢ÉśŃõ»Æ·“Ó¦ÓÖ·¢Éś»¹Ō·“Ó¦£¬ÕżČ·£»CĻī£¬ÓÉÓŚLiæÉŅŌÓėĖ®·“Ó¦£¬¹ŹÓ¦ĪŖ·ĒĖ®²ÄĮĻ£¬ÕżČ·£»DĻī£¬Ōµē³ŲÖŠŃōĄė×ÓÓ¦ĒØŅĘÖĮÕż¼«Ź§µē×Ó£¬¹Ź“ķ”£
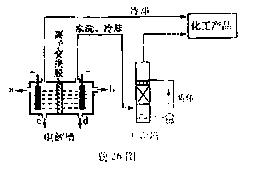
Ąż 6”¢(2009ÖŲĒģ)¹¤ŅµÉĻµē½ā±„ŗĶŹ³ŃĪÄÜÖĘČ”¶ąÖֻƹ¤ŌĮĻ£¬ĘäÖŠ²æ·ÖŌĮĻæÉÓĆÓŚÖʱø¶ą¾§¹č”£
(1)Ģā26Ķ¼ŹĒĄė×Ó½»»»Ä¤·Øµē½ā±„ŗĶŹ³ŃĪĖ®Ź¾ŅāĶ¼£¬µē½ā²ŪŃō¼«²śÉśµÄĘųĢåŹĒ”””” £»NaOHČÜŅŗµÄ³öæŚĪŖ”””””” (Ģī×ÖÄø)£»¾«Öʱ„ŗĶŹ³ŃĪĖ®µÄ½ųæŚĪŖ””””””
(Ģī×ÖÄø)£»øÉŌļĖžÖŠÓ¦Ź¹ÓƵÄŅŗĢåŹĒ””  ”””””£
”””””£
(2)¶ą¾§¹čÖ÷ŅŖ²ÉÓĆSiHCl3»¹Ō¹¤ŅÕÉś²ś£¬Ęäø±²śĪļSiCl4µÄ×ŪŗĻĄūÓĆŹÕµ½¹ć·ŗ¹Ų×¢”£
¢ŁSiCl4æÉÖĘĘųĻą°×ĢæŗŚ(Óė¹āµ¼ĻĖĪ¬Ö÷ŅŖŌĮĻĻąĶ¬)£¬·½·ØĪŖøßĪĀĻĀSiCl4ÓėH2ŗĶO2·“Ó¦£¬²śĪļÓŠĮ½ÖÖ£¬»Æѧ·½³ĢŹ½ĪŖ””””””””””””””””””
 ”””””””””””””””””””””£
”””””””””””””””””””””£
¢ŚSiCl4æÉ×Ŗ»ÆĪŖSiHCl3¶ųŃ»·Ź¹ÓĆ”£Ņ»¶ØĢõ¼žĻĀ£¬ŌŚ20LŗćČŻĆܱÕČŻĘ÷ÖŠµÄ·“Ó¦£ŗ
””3 SiCl4(g)+2
H2(g)+Si(g)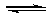 4 SiHCl3(g)
4 SiHCl3(g)
“ļĘ½ŗāŗó£¬H2ÓėSiHCl3ĪļÖŹµÄĮæÅØ¶Č·Ö±šĪŖ0.140mol/LŗĶ0.020mol/L£¬ČōH2Č«²æĄ“Ō“ÓŚĄė×Ó½»»»Ä¤·ØµÄµē½ā²śĪļ£¬ĄķĀŪÉĻŠčĻūŗÄ“æNaClµÄÖŹĮæĪŖ”” kg”£
(3)²ÉÓĆĪŽÄ¤µē½ā²Ūµē½ā±„ŗĶŹ³ŃĪĖ®£¬æÉÖĘČ” ĀČĖįÄĘ£¬Ķ¬Ź±Éś³ÉĒāĘų£¬ĻÖÖʵĆĀČĖįÄĘ213.0kg£¬ŌņÉś³ÉĒāĘų””””””
ĀČĖįÄĘ£¬Ķ¬Ź±Éś³ÉĒāĘų£¬ĻÖÖʵĆĀČĖįÄĘ213.0kg£¬ŌņÉś³ÉĒāĘų””””””
 (±ź×¼×“æö)”£
(±ź×¼×“æö)”£
[“š°ø]¢Å¢ŁĀČĘų£»a£»d£»ÅØĮņĖį”” ¢Ę¢ŁSiCl4+2H2+O2
 SiO2+4HCl
¢Ś0.35”” ¢Ē134.4
SiO2+4HCl
¢Ś0.35”” ¢Ē134.4
[½āĪö]µē½ā±„ŗĶĀČ»ÆÄĘČÜŅŗŹ±£¬ČÜŅŗÖŠµÄŃōĄė×ÓNa+ŗĶH+ ĻņŅõ¼«ŅĘ¶Æ£¬ĒŅŃõ»ÆŠŌ½ĻĒæµÄH+Ź×ĻČ·Åµē·¢Éś»¹Ō·“Ó¦£¬Éś³ÉĒāĘų£¬Ņõ¼«ø½½üµÄČÜŅŗŅņĻūŗÄĒāĄė×ÓŹ¹ČÜŅŗĻŌ¼īŠŌ£¬ÓėNa+ŠĪ³ÉNaOHČÜŅŗ£¬ŅõĄė×ÓCl-ŗĶOH-ĻņŃō¼«ŅĘ¶Æ£¬»¹ŌŠŌ½ĻĒæµÄŅõĄė×ÓCl-Ź×ĻČ·Åµē£¬·¢ÉśŃõ»Æ·“Ӧɜ³ÉĀČĘų”£
øł¾Ż·½³ĢŹ½æÉµĆ£ŗH2~2SiHCl3£¬Éś³ÉµÄSiHClµÄĪļÖŹµÄĮæÅضČĪŖ0.020mol/L£¬ĖłŅŌ²Ī¼Ó·“Ó¦µÄĒāĘųµÄĪļÖŹµÄĮæÅضČĪŖ0.01mol”£Ź£ÓąĒāĘųµÄĪļÖŹµÄĮæĪŖ0.14mol/L£¬Ōņ¹²ŠčŅŖĒāĘųµÄĪļÖŹµÄĮæÅضČĪŖ0.15mol/L£¬ĪļÖŹµÄĮæĪŖ3mol”£Óɵē½ā±„ŗĶNaClµÄ·½³ĢŹ½æÉÖŖ£¬2NaCl~H2£¬ŌņĻūŗÄNaClµÄĪļÖŹµÄĮæĪŖ6mol£¬ÖŹĮæĪŖ6mol”Į58.5g/mol=351g=0.35kg”£øł¾Ż»ÆŗĻ¼ŪµÄ±ä»ÆæÉÖŖ£¬ÓÉCl-Éś³É1molNaClO3Ź§Č„6molµē×Ó£¬Éś³É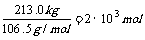 NaClO3×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ12”Į103
molµē×Ó£¬Ņņ“ĖÉś³ÉĒāĘųµÄĪļÖŹµÄĮæĪŖ6”Į103 mol£¬ŌŚ±źæöĻĀĘųĢåĢå»żĪŖ134.4m3”£
NaClO3×ŖŅʵē×ÓµÄĪļÖŹµÄĮæĪŖ12”Į103
molµē×Ó£¬Ņņ“ĖÉś³ÉĒāĘųµÄĪļÖŹµÄĮæĪŖ6”Į103 mol£¬ŌŚ±źæöĻĀĘųĢåĢå»żĪŖ134.4m3”£
[2010øßæ¼Ō¤²ā]ׯ¹ŪĄśÄźøßæ¼ŹŌĢāæÉ·¢ĻÖ£¬½āæɳäµēµē³ŲŹŌĢāµÄ¹Ų¼üŌŚÓŚÄÜ·ńÕżČ·ŹéŠ“µē¼«·“Ó¦Ź½”£ŹéŠ“µē¼«·“Ó¦Ź½µÄ¹Ų¼üŹĒÄÜ·ńÕżČ·ŹéŠ“·ÅµēŹ±µÄµē¼«·“Ó¦Ź½”£ŅŖÕżČ·ŹéŠ“·ÅµēŹ±µÄµē¼«·“Ó¦Ź½£¬¼ČŅŖÅŖĒåµĆŹ§µē×ÓµÄĪļÖŹ£¬»¹ŅŖĢŲ±š×¢ Ņāµē¼«²śĪļŹĒ·ńÓėµē½āÖŹČÜŅŗ¹²“ę£¬ŅŖŠ“³öŹµ¼Ź“ęŌŚµÄµē¼«·“Ó¦Ź½”£Č»ŗóøł¾ŻŌµē³ŲµÄøŗ¼«·“Ó¦Óėµē½ā³ŲµÄŃō¼«·“Ó¦”¢Ōµē³ŲµÄÕż¼«·“Ó¦Óėµē½ā³ŲµÄŅõ¼«·“Ó¦»„ĪŖÄę·“Ó¦£¬¼“æÉæģĖŁŠ“³ö³äµēŹ±µÄµē¼«·“Ó¦Ź½”£ø÷µē¼«·“Ó¦Ź½Ė³ĄūŠ“³öŅŌŗ󣬼“æÉÕżČ·½āĢā”£
Ņāµē¼«²śĪļŹĒ·ńÓėµē½āÖŹČÜŅŗ¹²“ę£¬ŅŖŠ“³öŹµ¼Ź“ęŌŚµÄµē¼«·“Ó¦Ź½”£Č»ŗóøł¾ŻŌµē³ŲµÄøŗ¼«·“Ó¦Óėµē½ā³ŲµÄŃō¼«·“Ó¦”¢Ōµē³ŲµÄÕż¼«·“Ó¦Óėµē½ā³ŲµÄŅõ¼«·“Ó¦»„ĪŖÄę·“Ó¦£¬¼“æÉæģĖŁŠ“³ö³äµēŹ±µÄµē¼«·“Ó¦Ź½”£ø÷µē¼«·“Ó¦Ź½Ė³ĄūŠ“³öŅŌŗ󣬼“æÉÕżČ·½āĢā”£
²āŹŌĢā
2£®µē¶Ę
(1)µē¶ĘµÄŗŅå
µē¶ĘŹĒÓ¦ÓƵē½āŌĄķŌŚÄ³Š©½šŹō±ķĆę¶ĘÉĻŅ»±”²ćĘäĖū½šŹō»ņŗĻ½šµÄ¹ż³Ģ”£
(2)µē¶ĘµÄÄæµÄ
µē¶ĘµÄÄæµÄÖ÷ŅŖŹĒŹ¹½šŹōŌöĒææ¹øÆŹ“ÄÜĮ¦”¢Ōö¼ÓĆĄ¹ŪŗĶ±ķĆęÓ²¶Č”£
(3)µē¶ĘµÄŌĄķ
µē¶ĘµÄŌĄķÓėµē½ā¾«Į¶ĶµÄŌĄķŹĒŅ»ÖĀµÄ”£µē¶ĘŹ±£¬Ņ»°ć¶¼ŹĒÓĆŗ¬ÓŠ¶Ę²ć½šŹōĄė×ӵĵē½āÖŹÅä³Éµē¶ĘŅŗ£»°Ń“ż¶Ę½šŹōÖĘĘ·½žČėµē¶ĘŅŗÖŠÓėÖ±Į÷µēŌ“µÄøŗ¼«ĻąĮ¬£¬×÷ĪŖŅõ¼«£»ÓĆ¶Ę²ć½šŹō×÷ĪŖŃō¼«£¬ÓėÖ±Į÷µēŌ“Õż¼«ĻąĮ¬”£ĶØČėµĶŃ¹Ö±Į÷µē£¬Ńō¼«½šŹōČܽāŌŚČÜŅŗÖŠ³ÉĪŖŃōĄė×Ó£¬ŅĘĻņŅõ¼«£¬ÕāŠ©Ąė×ÓŌŚŅõ¼«»ńµĆµē×Ó±»»¹Ō³É½šŹō£¬ø²øĒŌŚŠčŅŖµē¶ĘµÄ½šŹōÖĘĘ·ÉĻ”£
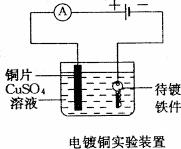
1£® ĶµÄµē½ā¾«Į¶
(1)µē½ā·Ø¾«Į¶ĶµÄ×°ÖĆ(ČēĶ¼)
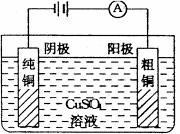
(2)µē½ā·Ø¾«Į¶ĶµÄ»ÆѧŌĄķ
Ńō¼«(“ÖĶ)£ŗCu£2e£=Cu2+
Ņõ¼«(“æĶ)£ŗCu2++2e£=Cu
ĖµĆ÷£ŗ
¢Ł ŅŌĶĪŖ²ÄĮĻ×öµÄµē¼«ŹōÓŚ»īŠŌµē¼«”£ŌŚŅ»°ćµÄµē½āĢõ¼žĻĀ£¬»īŠŌŃō¼«ĻČÓŚµē½āÖŹČÜŅŗÖŠµÄ³É·Ö·¢ÉśŃõ»Æ·“Ó¦”£
¢Ś“ÖĶÖŠĶłĶłŗ¬ÓŠŠæ”¢Ģś”¢Äų”¢Ņų”¢½šµČ¶ąÖÖŌÓÖŹ£¬µ±ŗ¬ŌÓÖŹµÄĶŌŚŃō¼«²»¶ĻČܽāŹ±£¬
Ī»ÓŚ½šŹō»ī¶ÆŠŌĖ³ŠņĶŅŌĒ°µÄ½šŹōŌÓÖŹČēZn”¢Fe”¢NiµČ£¬Ņ²»įĶ¬Ź±Ź§Č„µē×Ó£¬Čē£ŗ
Zn£2e£=Zn2+”” £»Ni£2e£=Ni2+
µ«ŹĒĖüĆĒµÄŃōĄė×Ó±ČĶĄė×ÓÄŃŅŌ»¹Ō£¬ĖłŅŌĖüĆĒ²¢²»ŌŚŅõ¼«»ńµĆµē×ÓĪö³ö£¬¶ųÖ»ŹĒĮōŌŚµē½āŅŗĄļ”£¶ųĪ»ÓŚ½šŹō»ī¶ÆŠŌĖ³ŠņĶÖ®ŗóµÄŅų”¢½šµČŌÓÖŹ£¬ŅņĪŖøų³öµē×ÓµÄÄÜĮ¦±ČĶČõ£¬ÄŃŅŌŌŚŃō¼«Ź§Č„µē×Ó±ä³ÉŃōĄė×ÓČܽāĻĀĄ“£¬µ±Ńō¼«ÉĻµÄĶŹ§Č„µē×Ó±ä³ÉĄė×ÓČܽāÖ®ŗó£¬ĖüĆĒŅŌ½šŹōµ„ÖŹµÄŠĪŹ½³Į»żŌŚµē½ā²Ūµ×£¬ŠĪ³ÉŃō¼«Äą(Ńō¼«ÄąæÉ×÷ĪŖĢįĮ¶½š”¢ŅųµČ¹óÖŲ½šŹōµÄŌĮĻ)
¢ŪÓƵē½ā¾«Į¶·ØĖłµĆµ½µÄĶ½Š×öµē½āĶ£¬ĖüµÄ“æ¶ČæÉ“ļµ½99.95%-99.98%”£
¹ś¼ŹŃ§Š£ÓÅŃ” - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com