
20.(10分)用电子式写出下列物质的形成过程
①H2S: ②NaOH:
③K2O2: ④Na2S:
⑤N2:
19.(6分)图为元素周期表的一部分,已知四种元素全为短周期元素,原子序数之和为32。
|
A |
B |
C |
|
|
D |
|
①元素符号:A ;B ;C ;D ;
②BCD气态氢化物的稳定性顺序: ;
③BCD最高价氧化物相应水化物酸性强弱顺序: 。
18.(6分)某微粒XO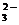 中共有42个电子,X元素位于周期表中的第 周期,第 族,它的最高价氧化物对应的水化物分子式为: 。
中共有42个电子,X元素位于周期表中的第 周期,第 族,它的最高价氧化物对应的水化物分子式为: 。
17.(6分)在水溶液中,YO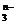 和S2-发生反应的离子方程式如下:YO
和S2-发生反应的离子方程式如下:YO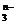 +3S2-+6H+=Y-+3S↓+3H2O①YO
+3S2-+6H+=Y-+3S↓+3H2O①YO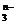 中Y元素的化合价是: ;
中Y元素的化合价是: ;
②Y元素原子的最外层电子数是: ;
③比较S2-和 Y-还原性: 。
16.(10分)用符号:A:质子数 B:中子数 C:核外电子数 D:最外层电子数E:电子层数,填写下列空白。
①原子种类由 决定;
②元素的种类由 决定;
③相对原子质量由 决定;
④元素的化合价由 决定;
⑤同位素由 决定。(有些答案不只一个)
15.关于H2O2的叙述不正确的是 ( )
A.H2O2可用于实验室中制O2 B.H2O2具有还有性及强氧化性
C.H2O2具有漂白性 D.H2O2四个原子在同一平面上
14.科学家最近发现一种只由四个中子构成的微粒,称为“四中子”也有人称为“零号元素”,下列有关“四中子”微粒的说法中正确的是 ( )
A.该微粒带四个单位的正电荷 B.该微粒质量数为4
C.在周期表中与氢元素占同一位置 D.该微粒带2个单位的正电
13.某元素构成的双原子单质分子有三种,其分子式量分别为70、72、74,此三种单质的物质的量之比为9∶6∶1,由此推断,下列结论中正确的是 ( )
A.此元素有三种同位素
B.其中有一种同位素原子的质量为36
C.其中质量数为37的同位素原子在该元素里占原子总数的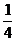
D.此元素单质的平均相对分子质量为72
12.一瓶气体只含一种元素则该气体是 ( )
A.一种单质
B.一种化合物
C.单质与化合物的混合物
D.既可能是一种单质也可能是几种单质的混合物
11.下列物质的晶体中既含有离子键,又含有非极性键的是 ( )
A.NaOH B.Na2O2 C.CaCl2 D.H2O2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com