
3、某研究小组成员在讨论鉴别浓硫酸和稀硫酸的方案时,设计如下方案:
|
|
操作 |
结论 |
|
甲 |
火柴梗 |
变黑者为浓硫酸 |
|
乙 |
加入金属铝片 |
产生刺激性气味者为浓硫酸 |
|
丙 |
分别加入到盛水的试管中 |
放热者为浓硫酸 |
|
丁 |
用玻璃棒蘸浓氨水靠近盛酸的瓶口 |
冒白烟者为浓硫酸 |
|
戊 |
加到CuSO4·5H2O晶体中 |
变白者为浓硫酸 |
(1)其中可行的是甲、丙、戊。
(2)其中一个稍作改进就能成为可行的是乙,改进方法是加热。
(3)完全错误的是丁,因为硫酸是高沸点的酸,没有挥发性。
(4)请给出另外至少两种鉴别方法
|
|
操作 |
根据现象做出结论 |
|
A |
滴加到氯化钠固体中加热 |
产生白雾的是浓硫酸 |
|
B |
加入铝片 |
常温下产生气体的是稀硫酸,无明显现象的是浓硫酸 |
|
C |
加入品红溶液 |
褪色的是浓硫酸 |
|
D |
加入木炭 |
产生刺激性气味气体的是浓硫酸 |
|
E |
称量相同体积的酸 |
质量大的是浓硫酸 |
|
F |
在相同条件下加热 |
先沸腾的是稀硫酸 |
[高考模拟]
2、关于浓H2SO4、稀H2SO4的叙述中正确的是( A )
A、浓H2SO4、稀H2SO4都难挥发
B、浓H2SO4、稀H2SO4都能氧化金属Zn,且反应产物相同
C、浓H2SO4、稀H2SO4在加热时都能与铜反应
D、浓H2SO4、稀H2SO4在常温下都能用铁容器贮存
|
|
浓硫酸 |
稀硫酸 |
|
|
酸 性 |
化学方程式 |
 2NaCl+H2SO4(浓) Na2SO4 2NaCl+H2SO4(浓) Na2SO4+2HCl↑ |
Zn+H2SO4=ZnSO4+H2↑ H2SO4+2NaOH=Na2SO4+2H2O |
|
应用 |
制氯化氢等挥发性酸 |
除铁锈、制硫酸铵等盐类 |
|
|
氧 化 性 |
强弱 |
强氧化性(硫元素被还原,可以与不 活泼金属如Cu及非金属如C等发生氧 化还原反应) |
弱氧化性(氢元素被还原,只能 与金属活动性顺序表中排在氢前 面的金属反应) |
|
化学方程式 |
 Cu+2H2SO4(浓) CuSO4+ Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O |
Fe+H2SO4=FeSO4+H2↑ |
|
|
应用 |
精炼石油、制造炸药等 |
实验室制氢气、制盐等 |
|
|
吸水 性 |
有无 |
有吸水性 |
无吸水性 |
|
应用 |
干燥剂 |
-- |
|
|
脱 水 性 |
有无 |
有脱水性 |
无脱水性 |
|
化学方程式 |
 C12H22O11 12C+11H2O C12H22O11 12C+11H2O |
-- |
|
|
应用 |
在有机反应中作脱水剂、制染料等 |
-- |
[思考感悟]如何稀释浓硫酸?
稀释浓H2SO4时应将浓H2SO4沿器壁缓缓地加入水中,并用玻璃棒不断搅拌,使热量不断地散发。
[基础训练]
1、将预先称量的20g蔗糖放入100mL烧杯中,加几滴水搅拌均匀,再加入15mL浓硫酸,用玻璃棒迅速搅拌,观察到蔗糖由白变黑,体积膨胀,呈疏松海绵状,有刺激性气味气体生成,放出大量的热,在此过程中浓硫酸没有表现出的化学性质是( C )
A、吸水性 B、脱水性 C、酸性 D、氧化性
(二)H2SO4的性质
1、物理性质:沸点高,难挥发,水中溶解性:极易溶于水;浓硫酸溶解时可放出大量的热。
2、稀H2SO4的性质:硫酸是强电解质,在水溶液中发生电离的方程式为H2SO4=2H++SO42-,其具有酸的通性,能与金属单质、碱性氧化物、碱、盐等物质发生反应。
3、浓H2SO4的特性:浓H2SO4中存在的主要是H2SO4分子,因而浓H2SO4具有一些特殊的性质。
(1)吸水性:利用浓H2SO4的吸水性,其常用作干燥剂。
(2)脱水性:浓H2SO4能够将有机物里的氢、氧元素按原子个数2︰1的比例脱去。
(3)强氧化性:
A、常温下,铁、铝遇浓H2SO4发生“钝化”。原因:金属表面形成了致密的氧化物保护层。所以常温下可用铝槽车装运浓硫酸。
B、能氧化不活泼的金属,如与Cu反应的化学方程式为:Cu+2H2SO4=CuSO4+SO2↑+2H2O。
 C、能氧化非金属单质,如与C反应的化学方程式为:C+2H2SO4 CO2↑+2SO2↑+2H2O。
C、能氧化非金属单质,如与C反应的化学方程式为:C+2H2SO4 CO2↑+2SO2↑+2H2O。
 (一)硫酸的制备:接触法制H2SO4是目前工业上采用的主要方法,包含三个步骤:
(一)硫酸的制备:接触法制H2SO4是目前工业上采用的主要方法,包含三个步骤:
1、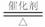 硫磺(或含硫矿石如FeS2)在沸腾炉中燃烧,化学方程式为4FeS2+11O2 2Fe2O3+8SO2。
硫磺(或含硫矿石如FeS2)在沸腾炉中燃烧,化学方程式为4FeS2+11O2 2Fe2O3+8SO2。
2、SO2的催化氧化:2SO2+O2 2SO3。 3、SO3的吸收:SO3+H2O=H2SO4。
20. ____ we are developing new technology at such a high pace ,the true challenge is to find new ways of using it.
A. Although B. After C. As soon as D. Now that
19. you’ve understood all these rules,you’ll have no further difficulty.
A. Unless B. Although C. Until D. Once
18. ______ time, animals have developed many ways to stay away from their enemies.
A. Through B. On C. By D. Over
17. Let me say sorry to her? No way! I would die I apologize to her!
A. after B. before C. until D. while
16.--Why didn’t you tell him about the result of the test?
--He rushed out of the room ______ I could say a word.
A. before B. until C. when D. after
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com