
4.在当代英国,国王、议会和内阁三者之间的关系是
A、内阁由议会产生,国王和内阁对议会负责
B、议会由内阁产生,议会和内阁对国王负责
C、国王、议会和内阁权力相互分立,互不相干
D、内阁对议会负责,国王按内阁的意志行使权力
3.下列对上海合作组织认识正确的有
①是发展国家之间政治、经济、文化等方面交流与合作的纽带
②是争取世界和平与促进经济发展的重要国际组织形式
③是各国公认的调整国家关系的原则和制度的总称
④是一个只有主权国家才能参加的国际组织
A、①②③ B、①②④ C、①③④ D、②③④
2.下列选项中国家结构形式是单一制,政体是共和制的一组是
①中国 ②美国 ③德国 ④意大利 ⑤法国 ⑥日本 ⑦印度
A、①③⑦ B、①④⑤ C、②④⑥ D、①④⑥
1.“国家无非是一个阶级镇压另一个阶级的机器,这一点即便在民主共和制下也丝毫不比君主制下差。”这段话表明
A、国家是阶级矛盾不可调和的产物B、国家是一种社会历史现象
C、国家是全体人民的国家D、国家是阶级专政的工具
(二)化学键的形成及对物质性质的影响
1、由金属元素与非金属元素间形成的化学键不一定是离子键,如氯化铝中共价化合物。
2、由阳离子和阴离子结合生成的化合物不一定是离子化合物,如H++OH-=H2O。
3、有化学键被破坏的变化不一定是化学变化,如HCl溶于水,NaCl熔化等。
4、用化学键强弱可解释物质的化学性质,也可解释物质的物理性质。
[思考感悟](1)形成离子键的静电作用指的是阴、阳离子间的静电吸引吗?(2)形成离子键的元素一定是金属元素和非金属元素吗?
(1)有阴、阳离子间的静电吸引,也有原子核与原子核之间,电子与电子之间的强烈的相互排斥。(2)不一定,如铵盐全是非金属元素形成的。
[基础训练]
1、现有如下各说法:①在水中氢、氧原子间均以化学键相结合;②金属和非金属化合形成离子键;③离子键是阳离子、阴离子的相互吸引;④根据电离方程式:HCl=H++Cl-,可判断HCl分子里存在离子键;⑤H2分子和Cl2分子的反应过程是H2、Cl2分子里共价键发生断裂生成H原子、Cl原子,而后H原子、Cl原子形成离子键的过程。上述各种说法正确的是( B )
A、①②⑤ B、都不正确 C、④ D、②③④⑤
2、下列物质中含有相同的化学键类型的是( C )
A、NaCl、HCl、H2O、NaOH B、Cl2、Na2S、HCl、SO2
C、HBr、CO2、H2O、CS2 D、Na2O2、H2O2、H2O、N2
3、科学家们在探索生命奥秘的过程中,认识到生命细胞的组成和元素周期律有着密切的联系,约占人体总质量99.97%的11种大量元素全部是元素周期表前20号元素,其余0.03%是由10多种人体不可缺少的微量元素组成。现有a-h 8种短周期元素,是除氧、钾、钙外的其他大量元素,它们在元素周期表中的位置如下,请据此回答下列问题:
|
a |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
d |
e |
|
|
|
|
b |
c |
|
|
|
|
|
|
|
|
|
|
|
|
f |
h |
g |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
(1)下列中的元素的原子间反应最容易形成离子键的是B,容易形成共价键的是C。
A、c和f B、b和g
C、d和g D、b和e
(2)下列由a-g形成的各分子中所有原子都满足最外层为8电子结构的是CD。
A、ea3 B、ag
C、fg3 D、dg4
(3)由a、e组成的一种化合物化学式为ea5,其各原子均达到同周期稀有气体原子的稳定结构,
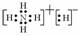
试写出该化合物的电子式 ,该物质属于离子(填“离子”或“共价”)化合物。
(4)均由a、b、h和氧四种元素形成的两种离子化合物,相互反应可生成有刺激性气味的气体。这两种化合物中有一种相对分子质量为120,该化合物熔化时破坏的是离子键(填化学键类型,下同),溶于水时破坏的是离子键和共价键。
[高考模拟]
4、(2007广东高考)下列物质中含离子键的是( C )
A、 Cl2 B、CO2 C、NaCl D、CH4
5、(2007广州模拟)固体A的化学式为NH5,能跟水反应,它的所有原子的电子层结构都跟与该原子同周期的稀有气体原子一样,则下列说法中,不正确的是( A )
A、1molNH5中有5NA个N-H键(NA为阿伏加德罗常数)
B、NH5中既有共价键、又有离子键,是离子晶体
C、NH5跟水的反应是氧化还原反应
D、NH5跟水反应的化学方程式为:NH5+H2O=NH3·H2O+H2↑
(一)物质中化学键的存在规律
1、离子化合物中一定有离子键,可能还有共价键:(1)简单离子组成的离子化合物中只有离子键;(2)复杂离子(原子团)组成的离子化合物中既有离子键,又有共价键。
2、共价化合物中只有共价键,一定没有离子键。
3、在非金属单质中只有共价键。
4、构成稀有气体的单质分子,由于原子已达到稳定结构,是单原子分子,分子中不存在化学键。
5、非金属元素的原子间也可以形成离子键,如氯化铵。
(六)共价化合物:共用电子对写在成键两原子中间(一般形成共价键后,成键原子达到稳定结构),每个原子最外层电子要标出,相同的原子不能合并。
(五)离子化合物:由阴、阳离子的电子式构成,但相同的离子不能合并,且带同类电荷的离子不能相邻。
(四)原子团:不仅要标出各原子最外层电子数,而且还要用“[ ]”括起来,并在右上角标出“n+”或“n-”。
(三)单核阳离子:与离子符号相同。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com