
5.(1)雷霆乍惊,宫车过也; , 。(《阿房宫赋》杜牧)
(2)_________,__________。飞湍瀑流争喧豗,砯崖转石万壑雷。
(3)清风徐来,______。举酒属客,________,歌窈窕之章。
第2套
4、下列句子中,没有语病的一句是
A、“奇瑞·东方之子”是上汽集团奇瑞汽车有限公司2003年推向市场的一款豪华大气、质量上佳、安全可靠、配置极为齐全、做工精细的轿车,在安全性、舒适度、人性化等方面可圈可点。
B、今年3月9日,韩国在野的大国家党和民主党向国会提出了弹劾总统卢武铉。这在韩国宪政史上尚属首次。
C、GDP是世界通用的重要宏观经济指标。单从现在我国GDP每增长一个百分点,就可以拉动80多万人就业来说,我们也必须保持经济快速增长的势头。
D、我们历来主张向外国著名的IT巨头公司借鉴,而且事实上已经这样做了;但我们也历来主张反对盲目照搬,全盘西化——事实证明,这样做极端有害。
3、下列句子中,加横线的词语使用恰当的一项是
A、从新年伊始,中央一再号召各级党组织务真求实,让广大人民的生活安居乐业。
B、在《幻城》和它的作者已经被炒得甚嚣尘上的时候,再来谈论就难免有些狗尾续貂的尴尬。
C、下半场,釜底抽薪的曼城队突然发威,迪斯丁·博斯威尔特和菲利浦斯各进一球,将比分扳平。
D、去年三月,美国悍然发动了军事力量对比悬殊的伊拉克战争,老百姓形象而戏谑地称美国人是“高射炮打蚊子”。
2、依次填入下列各句横线处的词语,最恰当的一组是
①荣耀与羞辱之下,心灵始而防范,继而 ,终至孤单。心灵于是呻吟,同时也在呼唤。
②随着我国证券市场的进一步发展,证券监管机构的某些强制执行 ,亟需加以规范。
③朋友是一把伞, 不能遏制狂风恶浪, 也能撑起一方晴空,让你备感真诚和友谊的难能可贵。
A、疏离 权限 虽然/但 B、疏离 权利 即使/可
C、疏远 权利 虽然/但 D、疏远 权限 即使/可
1、下列词语中加点的字的读音完全正确的一组是
A、粗犷(kuáng) 镌刻(juān) 量体裁衣(liàng) 卷帙浩繁(zhì)
B、埋怨(mán) 载体(zài) 暴殄天物(tiǎn) 戛然而止(jiá)
C、宝藏(zàng) 应届(yìng) 恪守不渝(kè) 擢发难数(zhuó)
D、熨帖(yùn) 熟稔(rěn) 相形见绌(chù) 徇私枉法(xùn)
21.(《物质结构与性质》)
(1)金属镁有许多重要的用途,法国化学家维多克·格利雅因发明了在有机合成方面用途广泛的格利雅试剂而荣获诺贝尔化学奖,格利雅试剂的结构简式可表示为RMgX,它是金属镁和卤代烃反应的产物,简称格氏试剂,它在醚的稀溶液中以单体形式存在,并与二分子醚络合,在浓溶液中以二聚体存在,结构如下图:
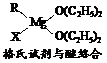
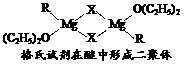
①上述2种结构中均存在配位键,把你认为是配位键的用“→”标出。
②由原子间的成键特点,可以预测中心原子Mg的杂化类型可能为_________;Mg
原子的核外电子排布式可表示为________________________。
③下列比较中正确的是_________________________________
A.金属键的强弱:Mg>Al B.基态原子第一电离能:Mg>Al
C.金属性:Mg>Al D.晶格能:NaCl>MgCl2
|
TiCl4+2Mg=======Ti+2MgCl2
①Ti元素在元素周期表中的位置是 ,钛原子的外围电子排布式为 。
②TiCl4在常温下是无色液体,在水或潮湿空气中易水解而冒白烟。则TiCl4属于 (填“原子”、“分子”或“离子”)晶体。
③二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。有关甲醛、苯、二氧化碳及水说法正确的是 。
A. 苯与B3N3H6互为等电子体
B.甲醛、苯分子中碳原子均采用sp2杂化
C.苯、二氧化碳是非极性分子,水和甲醛是极性分子
D.水的沸点比甲醛高得多,是因为水分子间能形成氢键
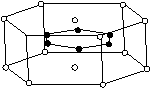 (3)2001年报导的硼和镁形成的化合物刷新了金属化合物超导温度的最高纪录。下图中示意的该化合物的晶体结构单元:镁原子间形成正六棱柱,则棱柱的上下底面还各有一个镁原子,六个硼原子位于棱柱内,则该化合物的化学式可表示为
(3)2001年报导的硼和镁形成的化合物刷新了金属化合物超导温度的最高纪录。下图中示意的该化合物的晶体结构单元:镁原子间形成正六棱柱,则棱柱的上下底面还各有一个镁原子,六个硼原子位于棱柱内,则该化合物的化学式可表示为
A.MgB B.MgB2 C.Mg2B D.Mg3B2
20.(6分)锌铝合金的主要成分有Zn、Al、Cu、Si等元素。实验室测定其中Cu含量的步骤如下:①称取该合金样品1.1g,用HCl和H2O2溶解后,煮沸除去过量H2O2,过滤,滤液定容于250mL容量瓶中。
②用移液管移取50.00mL滤液于250mL碘量瓶中,控制溶液的pH=3-4,加入过量KI溶液(生成CuI和I2)和指示剂,用0.01100mol×L-1Na2S2O3溶液滴定生成的I2至终点(反应:I2 + 2S2O32- = 2I- + S4O62-),消耗Na2S2O3溶液6.45mL。
⑴写出步骤①溶解Cu的离子方程式 。
⑵判断步骤②滴定终点的方法是 。
⑶计算合金中Cu的质量分数。
19.相对分子质量为92的某芳香烃X是一种重要的有机化工原料,研究部门以它为初始原料设计出如下转化关系图(部分产物、合成路线、反应条件略去)。其中A是一氯代物,H是一种功能高分子,链节组成为C7H5NO。
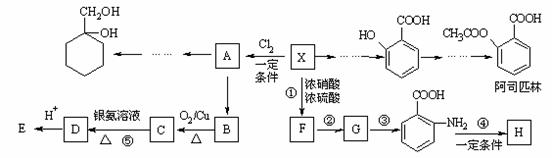
已知:
Ⅰ 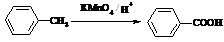
Ⅱ 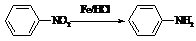 (苯胺,易被氧化)
(苯胺,易被氧化)
请根据所学知识与本题所给信息回答下列问题:
⑴H的结构简式是_______________________________________________;
⑵反应②的类型是 ;
⑶反应⑤的化学方程式是____________________________________________;
⑷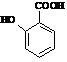 有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有_____种;
有多种同分异构体,其中含有1个醛基和2个羟基的芳香族化合物共有_____种;
⑸请用合成反应流程图表示出由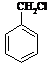 和其他无机物合成
和其他无机物合成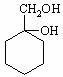 最合理的方案(不超过4步)。
最合理的方案(不超过4步)。
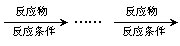 例:
例: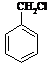

18.(10分)已知Cr(OH)3在碱性较强的溶液中将生成[Cr(OH)4]-,铬的化合物有毒,由于+6价Cr的强氧化性,其毒性是+3价Cr毒性的100倍。因此,必须对含铬的废水进行处理。目前研究和采用的处理方法主要有:
方法一、还原法:在酸性介质中用FeSO4、NaHSO3等将+6价Cr还原成+3价Cr。具体流程如下:

有关离子完全沉淀的p H如下表。
|
|
Fe(OH)2 |
Fe(OH)3 |
Cr(OH)3 |
|
Ksp |
8.0×10-16 |
4.0×10-38 |
6.0×10-31 |
|
完全沉淀的pH |
9.0 |
3.2 |
5.6 |
请回答下列问题:
(1)在②中调节pH的范围至 为最好。(填序号)
A.3-4 B.6-8 C.10-11 D.12-14
(2)若在①使FeSO4适当过量、空气适量,使Fe2+与Fe3+的比例恰当时,可产生具有磁性、组成类似于Fe3O4•xH2O的铁氧体悬浮物,变废为宝。则控制空气适量的目的是 ,使铁氧体分离出来较简便的方法是 。
方法二、电解法:将含+6价Cr的废水放入电解槽内,用铁作阳极,加入适量的氯化钠进行电解:阳极区生成的Fe2+和Cr2O72-发生反应,生成的Fe3+和Cr3十在阴极区与OH一结合生成Fe(OH)3和Cr(OH)3沉淀除去。
(3)写出此阴极反应的电极方程式 。现用上法处理1×104 L含铬(+6价)78 mg / L的废水,电解时阳极物质消耗的质量至少为________kg。
17.(10分)下图是部分常见元素的单质及其化合物的转化关系图(有关反应的条件及生成的部分产物已略去)。
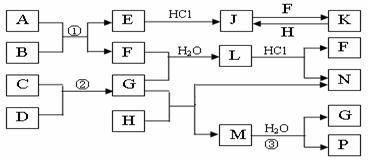
已知:E为红棕色固体,K为浅绿色溶液;反应①、②都是化工生产中的重要反应;B、C、D、H是单质;B、C、D、F、G、H常温下是气态; F、P 和H的水溶液均具有漂白作用,且F是形成酸雨的主要物质之一;N是一种常见的氮肥;化合物G分子构型为三角锥形,化合物M由两种元素组成,分子内共有58个电子。
(1)F的化学式 ;G的水溶液中,最多的阳离子是
(2)写出K与H反应的离子方程式
G与H反应的化学方程式
(3)在实验室中,向饱和H水溶液中加入CaCO3粉末,充分反应后过滤,可制得浓度较大的P的水溶液。用化学平衡移动的原理加以解释 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com