
14Ł®ĎÂÁĐ˵·¨ŐýČ·µÄĘÇ
AŁ®µ±ÇâÔ×Ó´Ón=1µÄ״̬ԾǨµ˝n=3µÄ״̬ʱŁ¬·˘Éäłöąâ×Ó
BŁ®ÄłŇ»ÔŞËصĶŕÖÖͬλËظ÷ľßÓв»Í¬µÄşËµçşÉĘý
CŁ®·ĹÉäĐÔÔŞËصİëËĄĆÚĘÇÖ¸´óÁż¸ĂÔŞËصÄÔ×ÓşËÖĐÓĐ°ëĘý·˘ÉúËĄ±äĐčŇŞµÄʱĽä
DŁ®ÖĐ×ÓÓëÖĘ×Ó˝áşĎłÉ뮺ËʱÎüĘŐÄÜÁż
13Ł®ĎÂÁĐąŘÓÚµç˝âÖĘČÜŇşµÄĹжĎŐýČ·µÄĘÇ
AŁ®ĎŕͬζČĎÂŁ¬ŇŃÖŞHF±ČHCNŇ×µçŔ룬ÔňNaFČÜŇşµÄpHÖµ±ČNaCNČÜŇşµÄpHÖµ´ó
BŁ®ÓöčĐԵ缫µç˝âş¬ÓĐŇ»¶¨Ĺ¨¶ČµÄCuSO4ČÜŇşŁ¬Ň»¶ÎʱĽäşóĐčĽÓČë0.1 mol Cu(OH)2˛ĹżÉŇÔ»Ö¸´ÖÁÔŔ´µÄŨ¶ČşÍĚĺ»ýŁ¬ÔňÔÚµç˝âąýłĚÖĐתŇĆÁË0.4 mol µç×Ó
CŁ®łŁÎÂĎÂŁ¬0.1 mol/LµÄĎÂÁĐČÜŇşŁş˘ŮNH4Al(SO4)2ˇ˘˘ÚNH4Clˇ˘˘ŰNH3ˇ¤H2Oˇ˘˘ÜCH3COONH4ČÜŇşÖĐŁ¬c(NH4+) ÓÉ´óµ˝ĐˇµÄËłĐňĘÇŁş˘Ú > ˘Ů > ˘Ü > ˘Ű
DŁ®łŁÎÂĎÂŁ¬0.4 mol/L HAČÜŇşşÍ0.2 mol/L NaOHČÜŇşµČĚĺ»ý»ěşĎşóČÜŇşµÄpH=3Ł¬ÔňČÜŇşÖĐ΢ÁŁĹ¨¶Č´ćÔÚąŘϵΪŁşc(HA) > c(Na+) > c(A-) > c(H+) > c(OH-)
12Ł®ÄłÎ¶ČĎÂŁ¬ÔÚČÝ»ýąĚ¶¨µÄĂܱŐČÝĆ÷ÖĐ·˘ÉúżÉÄć·´Ó¦ŁşA(g) + 2B(g)  ˇˇ2Q(g)ˇŁĆ˝şâʱŁ¬¸÷ÎďÖʵÄŨ¶Č±ČÎŞŁşc(A)ˇĂc(B)ˇĂc(Q)Ł˝1ˇĂ1ˇĂ2ˇŁ±ŁłÖζȲ»±äŁ¬ŇÔ1ˇĂ1ˇĂ2µÄĚĺ»ý±ČÔŮłäČËAˇ˘Bˇ˘QŁ¬ÔňĎÂÁĐĐđĘöŐýČ·µÄĘÇ
ˇˇ2Q(g)ˇŁĆ˝şâʱŁ¬¸÷ÎďÖʵÄŨ¶Č±ČÎŞŁşc(A)ˇĂc(B)ˇĂc(Q)Ł˝1ˇĂ1ˇĂ2ˇŁ±ŁłÖζȲ»±äŁ¬ŇÔ1ˇĂ1ˇĂ2µÄĚĺ»ý±ČÔŮłäČËAˇ˘Bˇ˘QŁ¬ÔňĎÂÁĐĐđĘöŐýČ·µÄĘÇ
AŁ®¸ŐłäČËʱ·´Ó¦ËŮÂĘŁ¬vŐý ĽőСŁ¬vÄć Ôö´ó
BŁ®´ďµ˝ĐµÄĆ˝şâʱŁ¬·´Ó¦»ěşĎÎďÖĐAˇ˘BµÄÎďÖʵÄÁż·ÖĘýÔöĽÓ
CŁ®´ďµ˝ĐµÄĆ˝şâʱŁ¬c(A)ˇĂc(B)ˇĂc(Q)ČÔÎŞ1ˇĂ1ˇĂ2
DŁ®´ďµ˝ĐµÄĆ˝şâąýłĚÖĐŁ¬ĚĺϵѹǿĎČÔö´óŁ¬şóÖ𽥼őС
11Ł®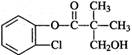 ÄłÓĐ»úÎďAĘÇĹ©Ň©Éú˛úÖеÄŇ»ÖÖÖĐĽäĚ壬Ćä˝áąąĽňĘ˝ČçÍĽËůĘľˇŁąŘÓÚAµÄĐđĘö˛»ŐýČ·µÄĘÇ
ÄłÓĐ»úÎďAĘÇĹ©Ň©Éú˛úÖеÄŇ»ÖÖÖĐĽäĚ壬Ćä˝áąąĽňĘ˝ČçÍĽËůĘľˇŁąŘÓÚAµÄĐđĘö˛»ŐýČ·µÄĘÇ
AŁ®ĘôÓÚ·ĽĎă×廯şĎÎď
BŁ®·Ö×ÓÖĐÖÁÉŮÓĐ12¸öÔ×Ó´¦ÓÚͬһƽĂćÄÚ
CŁ®1 mol A×î¶ŕżÉŇÔşÍ4 mol NaOH·´Ó¦
DŁ®Ň»¶¨ĚőĽţĎ¿ɷ˘ÉúĽÓłÉ·´Ó¦ˇ˘ĎűČĄ·´Ó¦ˇ˘Ë®˝â·´Ó¦
10Ł®ĘŻĂŢĘÇŇ»ŔŕĽŰ¸ńµÍÁ®µÄąčËáŃβÄÁĎŁ¬µ«ÓжľŁ¬ÄÜĘąČË»Ľ·Î°©ˇŁżóÇŕĘŻĂ޵ĻŻŃ§Ę˝ÎŞŁşNa2Fe5Si8O22(OH)2Ł¬ÓĂϡĎőËáČÜŇş´¦Ŕí¸ĂĘŻĂŢʱŁ¬»ąÔ˛úÎďÖ»ÓĐNOŁ¬ĎÂÁĐ˵·¨ŐýČ·µÄĘÇ
AŁ®¸ĂÎďÖĘÖĐFeÔŞËصĻŻşĎĽŰÎŞ+2ĽŰŁ¬ËüĘôÓÚąčËáŃÎ
BŁ®¸ĂÎďÖʵĻŻŃ§×éłÉżÉ±íʾΪŁşNa2Oˇ¤3FeOˇ¤Fe2O3ˇ¤8SiO2ˇ¤H2O
CŁ®1 mol ¸ĂÎďÖĘÄÜşÍ18 mol HNO3·´Ó¦Ł¬Ň˛ÄÜÓë18 mol ŃÎËá·´Ó¦
DŁ®ŐâÖÖĘŻĂŢĘôÓÚĐÂĐÍÎŢ»ú·Ç˝đĘô˛ÄÁĎ
9Ł®ĎÂÁĐŔë×Ó·˝łĚĘ˝ŐýČ·µÄĘÇ
AŁ®×ăÁżµÄCO2ͨČ뱥şÍĚĽËáÄĆČÜŇşÖĐŁşCO2 + CO32- + H2O = 2HCO3-
BŁ®ĎňNH4Al(SO4)2ČÜŇşÖеÎČëBa(OH)2ČÜҺʹSO42-·´Ó¦ÍęČ«Łş
2Ba2+ + 4OH- + Al3+ + 2SO42- = 2BaSO4ˇý+ AlO2- + 2H2O
CŁ®ĎňMg(HCO3)2ČÜŇşÖĐĽÓČëąýÁżµÄNaOHČÜŇşŁş
Mg2+ + 2HCO3- + 4OH- = Mg(OH)2ˇý+ 2CO32- + 2H2O
DŁ®ĎňFe(NO3)2ČÜŇşÖĐĽÓČëϡŃÎË᣺3Fe2+ + 4H+ + 2NO3- = 3Fe3+ + 2NOˇü + 2H2O
8Ł®ąŘÓÚ°˘·üĽÓµÂÂŢłŁĘý(ÓĂNA±íĘľ)µÄĎÂÁĐĐđĘöÍęČ«ŐýČ·µÄĘÇ
AŁ®ÔÚ±ę׼״żöĎÂŁ¬ĂܱŐČÝĆ÷ÖĐ11.2 L NOÓë11.2 L O2»ěşĎşóĆřĚĺ·Ö×ÓĘýÎŞ0.75NA
BŁ®ÓÉ3¸öĚĽÔ×ÓĐγɵÄÄłÓĐ»úÎ1 mol ¸ĂÓĐ»úÎď×î¶ŕş¬ÓеÄC-CµĄĽüĘýÎŞ2NA
CŁ®ÔÚ±ę׼״żöĎÂŁ¬160 g SO3ş¬ŃőÔ×ÓĘýĿΪ6NA
DŁ®±ę׼״żöĎÂŁ¬22.4 L Ë®ÖĐş¬·Ö×ÓĘýÎŞNA
7Ł®ĎÂÁĐĹжϲ»ŐýČ·µÄĘÇ
AŁ®ËáĐÔŁşH2SiO3 < H3PO4 < H2SO4 < HClO4
BŁ®»ąÔĐÔŁşSe2- > S2- > O2-
CŁ®Ëć×űËŘÔ×Ӱ뾶µÄÔö´óŁ¬ĆäÇ⻯ÎďµÄČ۷е㣺HF < HCl < HBr < HI
DŁ®CCl4ˇ˘PCl3ˇ˘SiF4ˇ˘S2Cl2ľůÂú×ă¸÷Ô×Ó×îÍâ˛ă8µç×ӽṹ
6Ł®ąúÇěÁůĘ®ÖÜÄęÍí»áÉϡ°60ˇ±ˇ˘ˇ°Đ¦Áłˇ±µČŃć»đČĂČ«ĘŔ˝çµÄ»ŞČËÎŞÖ®»¶şôˇ˘×ÔşŔˇŁŃć»đµÄÖ÷ŇŞÔÁĎĘÇşÚ»đŇ©Ł¬»ąÓвÝËáÄơ˘ĚĽËáÍ(·˘łöÂĚÉ«µÄąâ)µČ·˘É«ĽÁşÍÂČËáĽŘˇ˘ĂľÂÁ˝đĘô·ŰÄ©µČĚíĽÓĽÁˇŁĎÂÁĐ˵·¨ŐýČ·µÄĘÇ
˘ŮĚĽËáÍŇňÎŞĘÜČČ·Ö˝â˛Ĺ·˘łöÂ̹⡡ ˘ÚĂľÂÁÔÚŃć»đąýłĚÖб»Ńő»Żˇˇ ˘ŰÂČËáĽŘµÄÖ÷ŇŞÓĂÍľĘDzúÉú×ĎÉ«µÄ»đŃć ˇˇ˘ÜşÚ»đŇ©ĘÇŇ»ÖÖ´żľ»µÄ»ŻşĎÎ ˘Ý˛ÝËáÄƵĻŻŃ§Ę˝ÎŞNa2C2O4
AŁ®˘Ú˘Ýˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ BŁ®˘Ů˘Ú˘Üˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ CŁ®˘Ü˘Ýˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇˇ DŁ®˘Ú˘Ű˘Ü
5Ł®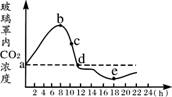 ˝«Ň»Ö˛Îď·ĹÔÚĂܱյIJŁÁ§ŐÖÄÚŁ¬ÖĂÓÚĘŇÍâĹŕŃřŁ¬ĽŮ¶¨ŐÖÄÚÖ˛ÎďÉúŔí״̬Óë×ÔČ»»·ľłÖĐĎŕͬˇŁÓĂCO2Ũ¶Č˛â¶¨ŇDzâµĂŐÖÄÚCO2Ũ¶ČµÄ±ä»ŻÇéżö»ćłöČçĎÂÇúĎßÍĽŁ¬ÓÉÍĽ»ńµĂµÄŐýČ·ĐĹϢĘÇ
˝«Ň»Ö˛Îď·ĹÔÚĂܱյIJŁÁ§ŐÖÄÚŁ¬ÖĂÓÚĘŇÍâĹŕŃřŁ¬ĽŮ¶¨ŐÖÄÚÖ˛ÎďÉúŔí״̬Óë×ÔČ»»·ľłÖĐĎŕͬˇŁÓĂCO2Ũ¶Č˛â¶¨ŇDzâµĂŐÖÄÚCO2Ũ¶ČµÄ±ä»ŻÇéżö»ćłöČçĎÂÇúĎßÍĽŁ¬ÓÉÍĽ»ńµĂµÄŐýČ·ĐĹϢĘÇ
AŁ®eµăʱŐÖÄÚCO2Ũ¶Č×îµÍŁ¬ËµĂ÷´ËʱąâşĎ×÷ÓĂ×îÇż
BŁ®dµăʱֲÎďµÄąâşĎ×÷ÓĂÇż¶ČµČÓÚşôÎü×÷ÓĂÇż¶Č
CŁ®¸ĂÖ˛ÎďµÄąâşĎ×÷ÓĂżŞĘĽÓÚbµăÇ°
DŁ®dµăʱ±ČcµăʱŁ¬Ň¶ÂĚĚĺÖĐC3ÓëC5Ďŕ¶Ôş¬Áż˝Ď¸ßµÄĘÇC3
ąúĽĘѧУÓĹѡ - Á·Ď°˛áÁбí - ĘÔĚâÁбí
şţ±±Ęˇ»ĄÁŞÍřÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨Ć˝Ě¨ | ÍřÉĎÓĐş¦ĐĹϢľŮ±¨×¨Çř | µçĐĹթƾٱ¨×¨Çř | ÉćŔúĘ·ĐéÎŢÖ÷ŇĺÓĐş¦ĐĹϢľŮ±¨×¨Çř | ÉćĆóÇÖȨľŮ±¨×¨Çř
ÎĄ·¨şÍ˛»ÁĽĐĹϢľŮ±¨µç»°Łş027-86699610 ľŮ±¨ÓĘĎ䣺58377363@163.com