
4.下列选项中正确的是 ( )
A.命题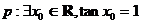 ;命题
;命题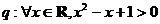 ,则命题“
,则命题“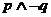 ”
”
是真命题
B.集合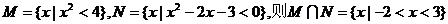
C.命题“若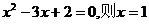 ”的逆否命题为“若
”的逆否命题为“若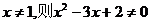 ”
”
D.函数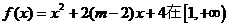 上为增函数,则m的取值范围是
上为增函数,则m的取值范围是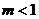
3.函数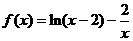 的零点所在的大致区间是 ( )
的零点所在的大致区间是 ( )
A.(1,2) B.(2,3) C.(3,4) D.(4,5)
1
设全集是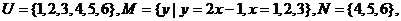 则
则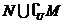 ( )
( )
A.{2} B.{2,4,5,6}
C.{1,2,3,4,6} D.{4,6}
2.若实数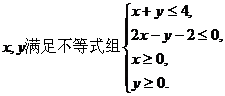 则
则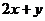 的最大值是 ( )
的最大值是 ( )
A.5 B.6 C.7 D.8
3.根据生成物和反应物的相对稳定性判断。由稳定的物质生成不稳定的物质的反应为吸热反应,反之为放热反应。
2.根据生成物和反应物总能量的相对大小判断。若生成物的总能量大于反应物的总能量,则为吸热反应,反之为放热反应。实际上,反应放热就是因为反应物的总能量大于生成物的总能量;而反应吸热是因为生成物的总能量大于反应物的总能量。
10.下表中的数据是破坏1mol物质中的化学键所消耗能量(KJ)
|
1mol物质 |
Cl2 |
Br2 |
I2 |
HF |
HCI |
HBr |
HI |
H2 |
|
能量(KJ) |
243 |
193 |
151 |
660 |
432 |
366 |
298 |
436 |
(1)根据上表,上述物质本身所具有的能量最低的是_______.
(2)下列氢化物中,最稳定的是_______.
A.HCI B.HBr C.HI D.HF
(3)X2+ H2=2HX(x代表Cl、Br、I)是_______(填“吸热”或“放热”)反应。
(4)相同条件下,X2(x代表CL、Br、I)分别与氢气反应,当消耗等物质的量的氢气时,______(放出或吸收)热量最多的是______.
[课后反思]
常见的放热反应有哪些?①所有的燃烧反应,如碳、氢气、甲烷等在氧气或空气中的燃烧,氢气在氯气中的燃烧等。②酸碱中和反应。③大多数的化合反应。④金属与酸的反应,如镁条和盐酸的反应。
常见的吸热反应有哪些?①大多数的分解反应。②氢氧化钡晶体和氯化铵晶体的反应。③碳和二氧化碳、碳和水的反应等。
9.已知甲烷的燃烧反应:CH4+2O2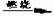 CO2+2H2O是一个放出热量的反应,则说明反应物1molCH4和2molO2所具有的总能量_______(填“大于”、“小于”或“等于”)生成物1mol CO2和2molH2O所具有的总能量。断开1molCH4和2molO2中的化学键需_______(填“吸收”或“放出”,下同)能量,形成CO2中2molC=O和H2O中4molH-O键需________能量。
CO2+2H2O是一个放出热量的反应,则说明反应物1molCH4和2molO2所具有的总能量_______(填“大于”、“小于”或“等于”)生成物1mol CO2和2molH2O所具有的总能量。断开1molCH4和2molO2中的化学键需_______(填“吸收”或“放出”,下同)能量,形成CO2中2molC=O和H2O中4molH-O键需________能量。
8.2C+O2=2CO,2CO+O2=2CO2都是放热反应,据此判断下列说法不正确的是( )
A.12gC所具有的能量一定高于28gCO所具有的能量
B.56gCO和32gO2所具有的总能量大于88gCO2所具有的总能量
C.12gC和32gO2所具有的总能量大于44gCO2所具有的总能量
D.将一定质量的C燃烧,生成CO2比生成CO时放出的热量多
7.下列各图中,能表示反应吸收热量的是( )
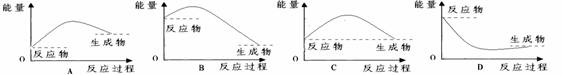
6.下列说法中正确的是( )
A.物质发生化学反应都伴随着能量的变化 B.伴随有能量变化的物质变化都是化学变化
C.在一个确定的化学反应中,反应物的总能量总是低于生成物的总能量。
D.在一个确定的化学反应中,反应物的总能量总是高于生成物的总能量
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com