
溶 液 胶体 浊液
1、分散质大小(nm) <1 1-100 >100
10、物质的量浓度的配制 配制前要检查容量瓶是否漏水
步骤:①. 计算 m=c×v×M ②.称量③. 溶解 ④.转移 (洗涤2---3次 洗涤液转入容量瓶)
⑤.定容⑥.摇匀⑦. 装瓶贴签
9、物质的量浓度与物质的量的关系:公式:CB=
8、物质的量浓度:单位体积溶液中所含溶质B的物质的量。符号CB 单位:mol/l
7、阿伏加德罗定律:同温同压下, 相同体积的任何气体都含有相同的分子数
6、体积与物质的量的关系:公式:n=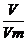 标准状况下
,1mol任何气体的体积都约为22.4l
标准状况下
,1mol任何气体的体积都约为22.4l
5、质量与物质的量的关系:公式:n=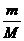
4、摩尔质量:单位物质的量的物质所具有的质量 用M表示 单位:g/mol 数值上等于该物质的式量
3、微粒与物质的量的关系: 公式:n=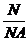
2、阿伏加德罗常数:0.012kgC-12中所含有的碳原子数。用NA表示。 约为6.02x1023
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com