
3.1842年,英国对华输出的货物总值是96.9万英镑,1844年迅速上升到230.5万。导致这一现象的原因是( )
A.鸦片输入减少 B.自然经济解体
C.列强夺取了政治经济特权 D.关税降低
2.两宋时期商品经济发展的影响不包括( )
A.加快了农副产品的商品化
B.城镇经济空前繁荣和发展
C.益州地区的富商开始发行交子
D.商税成为政府重要财源
1.下列有关西周井田制的叙述,正确的是( )
①奴隶社会的土地国有制 ②诸侯臣下只能世代享用 ③土地不得转让和买卖④直接耕种土地者要交纳租税
A.①②③④ B.①②③ C.①③④ D.②③④
26.(5分)在一定条件下发生反应:3A(g)
+ 2B(g)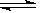 xC(g)
+ 2D(g),在2 L密闭容器中,把4 mol A和2 mol B混合,2
min后达到平衡。此时C的浓度为0.8mol/L,又测得反应速率vB =
0.2 mol /(L · min)。试求算:
xC(g)
+ 2D(g),在2 L密闭容器中,把4 mol A和2 mol B混合,2
min后达到平衡。此时C的浓度为0.8mol/L,又测得反应速率vB =
0.2 mol /(L · min)。试求算:
(1)x的值;
(2)达平衡时A的浓度;
25.(10分)为了探究原电池的电极名称不仅与电极材料有关还与电解质溶液有关,某学生做了如下的实验
|
编号 |
电极材料 |
电解质溶液 |
电子流向 |
|
① |
Mg-Al |
HNO3(浓) |
Mg→Al |
|
② |
Mg-Al |
HCl(aq) |
Mg→Al |
|
③ |
Mg-Al |
NaOH(aq) |
Al→Mg |
|
④ |
Al-Cu |
HNO3(浓) |
Cu→Al |
根据以上表格内容回答:
(1)( 4分)实验1中Mg作___________(填正极或负极),发生__________(氧化反应或还原反应)
实验3中Mg作___________,发生__________(同上)
(2) ( 6分)实验2中Mg电极反应式为__________________。
Al电极上的电极反应式为_________________________,总的电池反应是_______________________________。
24.(6分)一定温度下,某容积为2L的密闭容器内,某一反应中M、N的物质的量随反应时间变化的曲线如图,依图所示:
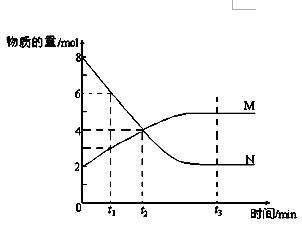
(1)该反应的化学方程式是___________________。
(2)在图上所示的三个时刻中, (填t1、t2或t3)时刻处于平衡状态,此时V正 V逆(填>、<或=);
达到平衡状态后,平均反应速率v(N)﹕v(M)= 。
(3)若反应容器的容积不变,则压强不再改变
(填“能”或“不能”)作为该反应已达到平衡状态的判断依据。
(4)已知M、N均为气体,则下列措施能增大反应速率
A.升高温度 B.降低压强 C.减小M的浓度 D.将反应容器体积缩小
23.(4分)A、B、C为短周期元素,在周期表中所处的位置如图所示,A、C两元素原子核外电子数之和等于B元素原子的质子数。B原子核内的质子数和中子数相等。
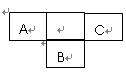
(1)B位于元素周期表中第 周期,第 族。
(2)C的原子结构示意图为 。
(3)用电子式表示B元素氢化物的形成过程:
22.(10分)按要求用合适的化学用语填空
Ⅰ.(8分)在原子序数1-18号元素中:
(1)与水反应最剧烈的金属是_____________。
(2)与水反应最剧烈的非金属单质是_____________。
(3)原子半径最小的元素是_____________。
(4)气态氢化物最稳定的化学式是_____________。
(5)最高价氧化物对应水化物的酸性最强的化学式是_____________。
(6)电子数为10的分子(写5个)
Ⅱ.(2分)下列各分子中,所有原子都满足最外层为8电子结构的是
①. H2O ②. BF3 ③.CF2Cl2 ④. PCl3 ⑤. SO3 ⑥. N2 ⑦. COCl2
21、(5分)有下列四种微粒:①O、② Na、③
Na、③ Mg、④N(填写序号)
Mg、④N(填写序号)
(1)按原子半径由大到小顺序排列的是__________________________.
(2)微粒中质子数小于中子数的是______________________________.
(3)在化合物中呈现的化合价的数值最多的是____________________.
(4)能形成X2Y2型化合物的是___________,能形成X3Y2型化合物的是__________.
20、在容积为1 L的固定真空容器中,加入3.68 g N2O4无色晶体,升温至20℃,晶体逐渐气化成无色气体,并部分离解为红棕色的NO2气体,直至达到化学平衡:
N2O4(g) 2N2O4(g)(正反应为吸热反应),从化学反应刚发生直到化学平衡的全过程中,以下量的变化正确的是(温度不变) ( )。
A. 气体总压强减小 B. 气体平均相对分子质量减小
C. 气体的密度增大 D. 气体的密度减小
第 Ⅱ 卷(非选择题 共40分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com