
1.(07年广东化学·4)许多国家十分重视海水资源的综合利用。不需要化学变化就能够从海水中获得的物质是
A.氯、溴、碘
B.钠、镁、铝
C.烧碱、氢气
D.食盐、淡水
答案:D
解析:考查海水成分,化学与生活、化学与技术内容。题目中A、B、C中物质只能通过化学变化取得。
35. (09年福建理综·23)(15分)
(09年福建理综·23)(15分)

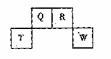 短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中T所处的周期序数与主族序数相等,请回答下列问题:
短周期元素Q、R、T、W在元素周期表中的位置如右图所示,期中T所处的周期序数与主族序数相等,请回答下列问题:
 (1)T的原子结构示意图为 。
(1)T的原子结构示意图为 。
 (2)元素的非金属性为(原子的得电子能力):Q W(填“强于”或“弱于”)。
(2)元素的非金属性为(原子的得电子能力):Q W(填“强于”或“弱于”)。
 (3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为 。
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,其中一种是气体,反应的化学方程式为 。
 (4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是 。
(4)原子序数比R多1的元素是一种氢化物能分解为它的另一种氢化物,此分解反应的化学方程式是 。
 (5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氯气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是 。
(5)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氯气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是 。
 (6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量akJ和bkJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的
(6)在298K下,Q、T的单质各1mol完全燃烧,分别放出热量akJ和bkJ。又知一定条件下,T的单质能将Q从它的最高价氧化物中置换出来,若此置换反应生成3molQ的单质,则该反应在298K下的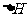 =
(注:题中所设单质均为最稳定单质)。
=
(注:题中所设单质均为最稳定单质)。
答案:(1) (2)弱于
(2)弱于
(3)S+2H2SO4(浓) 3SO2↑+2H2O
3SO2↑+2H2O
(4)2H2O2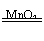
 2H2O+O2↑(或其他合理答案:)
2H2O+O2↑(或其他合理答案:)
(5)NaNO2
(6)(3a – 4b)kJ/mol
解析:本题考查无机物的性质,涉及化学用语、方程式书写、氧化还原反应以及热化学的知识。从给出的表,结合T在周期表的位置与族数相等这一条件 ,不难得出T为Al,Q为C,R为N,W为S。(1)T为Al,13号元素。(2)S、C最高价氧化物对应的酸为硫酸强于碳酸,则可得非金属性S强于C。(3)S与H2SO4发生归中反应,从元素守恒看,肯定有水生成,另外为一气体,从化合价看,只能是SO2。(4)比R质子数多1的元素为O,存在H2O2转化为H2O的反应。(5)N中相对分子质量最小的氧化物为NO,2NO+O2=2NO2,显然NO过量1L,同时生成1L的NO2,再用NaOH吸收,从氧化还原角度看,+2价N的NO与+4价N的NO2,应归中生成+3N的化合物NaNO2。(6)C +O2 CO2△H=-a kJ/mol①,4Al+3O2=2Al2O3△H= -4bkJ/mol②。Al与CO2的置换反应,写出反应方程式为:4Al+3CO2
CO2△H=-a kJ/mol①,4Al+3O2=2Al2O3△H= -4bkJ/mol②。Al与CO2的置换反应,写出反应方程式为:4Al+3CO2 3C+2Al2O3,此反应的△H为可由②-①×3得,△H=-4b-(-3a)=(3a-4b)kJ/mol。
3C+2Al2O3,此反应的△H为可由②-①×3得,△H=-4b-(-3a)=(3a-4b)kJ/mol。
36 .(09年天津理综·7)(14分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
.(09年天津理综·7)(14分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族 周期 周期 |
IA |
|
0 |
|||||
|
1 |
① |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
|
2 |
|
|
|
② |
③ |
④ |
|
|
|
3 |
⑤ |
|
⑥ |
⑦ |
|
|
⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序为 。
 (2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是
。
 (3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:
。
 (4)由表中两种元素的原子按1︰1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)
_。
(4)由表中两种元素的原子按1︰1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号)
_。
 a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
 (5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:

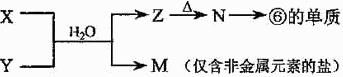
 X溶液与Y溶液反应的离子方程式为
,
X溶液与Y溶液反应的离子方程式为
, N→⑥的单质的化学方程式为
。
N→⑥的单质的化学方程式为
。
 常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至
。
常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至
。
答案:(1)Na>Al>O (2)HNO3>H2CO3>H2SiO3 (3)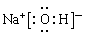 或
或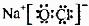 (4)a b
(4)a b
(5)Al3++3NH3·H2O=Al(OH)3↓+3NH4+ 2Al2O3(熔融)
 4Al+3O2↑ 溶液的pH等于7
4Al+3O2↑ 溶液的pH等于7
解析:本题以周期表为题材,考查原子半径比较,酸性强弱,电子式,离子方程式以及盐类水解等知识。(1)⑤⑥位于同一周期,且⑤排在⑥的前面,原子半径大,而④在上一周期,比⑤、⑥少一个电子层,故半径最小。(2)②⑦位于同一主族,上面的非金属性强,最高价含氧酸酸性强,②③位于同一周期,且③在后,非金属性强,对应的酸性强。(3)四种元素分别为氢、氧、钠和氯,离子键显然必须是钠盐,极性共价键则应有两种非金属组成。(4)液态H2O2可以在MnO2、FeCl3等催化剂作用下发生分解反应。(5)⑥为Al,可推断Z为Al(OH)3,受热分解可产物Al2O3,再电解即可得单质铝。M仅含非金属的盐,显然铵盐,所以X与Y应为AlCl3与NH3·H2O的反应,生成NH4Cl。由于NH4+ 水解,故要使其浓度与Cl-相等,则要补充NH3·H2O。由电荷守恒知:c(NH4+ )+ c(H+) c(Cl-)+c(OH-),若c(NH4+ )
c(Cl-)+c(OH-),若c(NH4+ ) c(Cl-),则c(H+)= c(OH-),即pH=7。
c(Cl-),则c(H+)= c(OH-),即pH=7。
14.(8分)(1)7 在K2O、K2O2、KO2、KO3中任选2个 (2)He、Ne、Ar
(3)C、H (4)Na (5)NH3 SiH4
解析:本题考查了元素周期表和元素周期律的知识,侧重考查学生运用所学知识解决问题的能力。(1)1-20号的金属元素有:Li、Be、Na、Mg、Al、K、Ca。(3)有机物的种类在化合物中占的比例最大,且C、H还能组成无机物。(5)由同一周期从左到右非金属性逐渐增强可知非金属性:N>C,由同一主族从上到下非金属性逐渐减弱可知非金属性:C>Si,所以非金属性:N>Si。又由非金属性越强其氢化物的稳定性也越强可知稳定性:NH3>SiH4。
34.(8分)(08年海南化学·14)根据元素周期表1-20号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有________种,金属性最强的元素与氧反应生成的化合物有___________(填两种化合物的化学式)。
(2)属于稀有气体的是___________(填元素符号,下同)。
(3)形成化合物种类最多的两种元素是____________________。
(4)第三周期中,原子半径最大的是(稀有气体除外)______________。
(5)推测Si、N最简单氢化物的稳定性_________大于_________(填化学式)。
33.(10分)(2007海南·13)下表为元素周期表的一部分,请回答有关问题:
|
|
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
|
|
|
|
① |
|
② |
|
|
3 |
|
③ |
④ |
⑤ |
|
⑥ |
⑦ |
⑧ |
|
4 |
⑨ |
|
|
|
|
|
⑩ |
|
(1)⑤和⑧的元素符号是 和 ;
(2)表中最活泼的金属是 ,非金属最强的元素是 ;
(填写元素符号)
(3)表中能形成两性氢氧化物的元素是 ,分别写出该元素的氢氧化物与⑥、⑨最高价氧化物的水化物反应的化学方程式:
, ;
(4)请设计一个实验方案,比较⑦、⑩单质氧化性的强弱:
。
答案:(1)Si Ar(2)K F
(3)铝(或Al)2Al(OH)3 + 3H2SO4=Al2(SO4)3 + 6H2O
Al(OH)3 + KOH=KAlO2 +2H2O
(4)在NaBr溶液中通入氯气(或加入氯水),溶液变红棕色(或橙色)
考点:本题考查了元素周期表的应用以及常见元素的性质。
解析:(1)根据元素周期表,可确定①、②、③、④、⑤、⑥、⑦、⑧、⑨、⑩元素分别为:N、F、Mg、Al、Si、S、Cl、Ar、K、Br。(2)又知金属性:同周期从左到右越来越小,同主族从上到下越来越大;而非金属性:同周期从左到右越来越大,同主族从上到下越来越小。(3)氢氧化铝为两性化合物,既能与酸反应,又能与碱反应。(4)利用“在氧化还原反应中,氧化剂氧化性大于氧化产物”原理,设计反应Cl2 + 2NaBr=2NaCl+Br2。
31.(09年海南化学·2)同一短周期的元素W、X、Y、Z的原子序数依次增加,下列叙述正确的是:
A.单质的化学活泼性:W<X<Y<Z B.原子最外层电子数:W<X<Y<Z
C.单质的氧化能力:W<X<Y<Z D.元素的最高化合价:W<X<Y<Z
答案:B
解析:本题中元素为同一周期,从左至右最外层电子数依次增加。而单质的活泼性分金属与非金属性,氧化能力随着单质晶体形态及分子内的化学键不同有变化,最高化合价随原子序数的递增有特例(O、F无正价)。
32 .(09年海南化学·10)门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是:
.(09年海南化学·10)门捷列夫在描述元素周期表时,许多元素尚未发现,但他为第四周期的三种元素留下了空位,并对它们的一些性质做了预测,X是其中的一种“类硅”元素,后来被德国化学家文克勒发现,并证实门捷列夫当时的预测相当准确。根据元素周期律,下列有关X性质的描述中错误的是:
 A.X单质不易与水反应 B.XO2可被碳或氢还原为X
A.X单质不易与水反应 B.XO2可被碳或氢还原为X
 C.XCl4的沸点比SiCl4的高 D.XH4的稳定性比SiH4的高
C.XCl4的沸点比SiCl4的高 D.XH4的稳定性比SiH4的高
答案:D
解析:根据元素周期律,同族元素随着原子序数的递增,非金属性减弱,气态氢化物的稳定性减弱。故D选项有明显错误。其他选项可由硅的性质进行类推。
30.(09年广东文基·62)碘单质及其化合物具有重要应用。下列说法正确的是
A.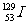 与
与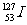 互为同位素
互为同位素
B.加碘食盐能使淀粉溶液变蓝
C.从海带中提取I2的过程只发生物理变化
D.I和Cl是同族元素,HI比HCl稳定
答案:A
解析: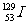 与
与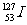 是I元素的不同核素,互为同位素,A选项正确;加碘食盐的碘是化合态的,不能使淀粉变蓝色,只有游离态的单质碘才能使淀粉变蓝色,故B选项错误;海带中的碘是化合态的,因此从海带中提取I2时要把化合态的转变为游离态的,价态发生变化,发生氧化还原反应,故C选项错误;I和Cl是同族元素,由于I的核电荷数比Cl多,因此Cl的非金属性比I强,所以HCl比HI稳定,故D选项错误。
是I元素的不同核素,互为同位素,A选项正确;加碘食盐的碘是化合态的,不能使淀粉变蓝色,只有游离态的单质碘才能使淀粉变蓝色,故B选项错误;海带中的碘是化合态的,因此从海带中提取I2时要把化合态的转变为游离态的,价态发生变化,发生氧化还原反应,故C选项错误;I和Cl是同族元素,由于I的核电荷数比Cl多,因此Cl的非金属性比I强,所以HCl比HI稳定,故D选项错误。
[考点分析]元素及其化合物性质;元素周期律的应用
29.(09年山东理综·11)元素在周围表中的位置,反映素的原子结构和性质,下列说法正确的是
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期和的元素,最外层电子数,化学性质完全相同
D.同一主族的原子,最外层的化学原子相同
答案:B
解析:本题比较全面的考查了元素周期律的核心知识-“元素的结构”、“元素在周期表的位置”“、元素的性质”三者之间的关系。周期表中位于金属和非金属分界线的元素既有金属性又有非金属性,碳元素在遇到不同的物质反应时,既可表现为得到电子,也可能表现为失去电子;第三周期的元素从Na到Cl从正一价到正七价符合这一说法;H元素、Li元素形成离子后不能达到8电子稳定结构;同一主族的元素的原子,最外层电子数是相同的,但化学性质只能是相似,如第VIIA族的所有元素最外层都为7个电子,在化学反应中常表现为得电子,但的电子能力也是不一样的。再比如第IA族的所有元素最外层都为1个电子,但是H元素与Na元素性质差异很大。
28.(09年山东理综·10)下列关于氯的说法正确的是
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.若35 17Cl、37 17若Cl为不同的核素,有不同的化学性质 学科
学科
C.实验室制备Cl2,可用排放和食盐水集气法收集
D.1.12LCl2含有1.7NA个质子(NA 表示阿伏伽德罗常数)
答案:C
解析:本题以氯元素为载体,从氧化还原、原子结构、收集方法不同角度进行考查,体现了山东理综化学选择题的命题模式。氯气与水的反应既是氧化剂也是还原剂;同一元素的不同核素化学性质几乎完全相同而物理性质不同;D中提Cl2的体积未指明是标准状况。实验室制备Cl2,可用排饱和食盐水集气法收集也可用瓶口向上排空气法收集,故C正确。
26.(09年江苏化学·2) 下列有关化学用语使用正确的是
下列有关化学用语使用正确的是
A.硫原子的原子结构示意图:
B.NH4Cl的电子式: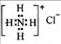
C.原子核内有10个中子的氧原子:
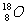
 D.对氯甲苯的结构简式:
D.对氯甲苯的结构简式: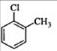
 答案:C
答案:C
 解析:A项,硫原子的原子结构示意图应为
解析:A项,硫原子的原子结构示意图应为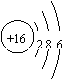
 ,
, 所以A项错误。B项,NH4Cl是由MH4+和Cl-离子构成,由于Cl-是阴离子,必须写出电子式,
所以A项错误。B项,NH4Cl是由MH4+和Cl-离子构成,由于Cl-是阴离子,必须写出电子式, 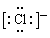 。
。
 C项,
C项,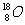 表示质量数为18,质子数为8的氧原子,所以该原子核内有10个中子。
表示质量数为18,质子数为8的氧原子,所以该原子核内有10个中子。
 D项,该结构简式是邻氯甲苯,因为氯原子和甲基的位置在相邻的碳原子上。对氯甲苯中的氯原子和甲基的位置应该处于相对位置。
D项,该结构简式是邻氯甲苯,因为氯原子和甲基的位置在相邻的碳原子上。对氯甲苯中的氯原子和甲基的位置应该处于相对位置。
 [考点分析]
[考点分析]
 ①熟记1-20号原子的原子结构结构示意图,常见阴离子、阳离子的结构示意图;
①熟记1-20号原子的原子结构结构示意图,常见阴离子、阳离子的结构示意图;
 ③质量数、质子数、中子数之间的关系;、
③质量数、质子数、中子数之间的关系;、
 ④常见有机物的命名。
④常见有机物的命名。
27 .(09年江苏化学·8)X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
.(09年江苏化学·8)X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是
 A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
A.元素Y、Z、W具有相同电子层结构的离子,其半径依次增大
 B.元素X不能与元素Y形成化合物X2Y2
B.元素X不能与元素Y形成化合物X2Y2
 C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
C.元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR
 D.元素W、R的最高价氧化物的水化物都是强酸
D.元素W、R的最高价氧化物的水化物都是强酸
 答案:C
答案:C
 解析:从题目所给的条件可以看出X是H元素,Y是O元素,Z是Na元素,W是Mg元素,R是S元素。所以,A项,Y、Z、W具有相同电子层结构的离子(O2-、Na+、Mg2+),其半径依次减小(判断依据:核外电子排布相同的微粒,半径随着核电荷数的增加而减小);B项,X和Y元素能形成2种化合物,X2Y(H2O)和X2Y2(H2O2);C项,元素Y、R分别与元素X形成的化合物是氢化物,因为Y(O元素)和R(S元素)的非金属性强弱:Y>R,所以对应的氢化物的稳定性:XmY>XmR;W元素最高价氧化物的水化物是Mg(OH)2,是中强碱,而R元素最高价氧化物的水化物是H2SO4,是强酸。
解析:从题目所给的条件可以看出X是H元素,Y是O元素,Z是Na元素,W是Mg元素,R是S元素。所以,A项,Y、Z、W具有相同电子层结构的离子(O2-、Na+、Mg2+),其半径依次减小(判断依据:核外电子排布相同的微粒,半径随着核电荷数的增加而减小);B项,X和Y元素能形成2种化合物,X2Y(H2O)和X2Y2(H2O2);C项,元素Y、R分别与元素X形成的化合物是氢化物,因为Y(O元素)和R(S元素)的非金属性强弱:Y>R,所以对应的氢化物的稳定性:XmY>XmR;W元素最高价氧化物的水化物是Mg(OH)2,是中强碱,而R元素最高价氧化物的水化物是H2SO4,是强酸。
 [考点分析]元素周期律的运用
[考点分析]元素周期律的运用
 ①同周期、同主族内元素性质(核外电子排布、原子半径、金属性、非金属性、酸碱性、气态氢化物的热稳定性等)变化规律。
①同周期、同主族内元素性质(核外电子排布、原子半径、金属性、非金属性、酸碱性、气态氢化物的热稳定性等)变化规律。
 ②元素之间化合所形成化合物的化学式的书写。
②元素之间化合所形成化合物的化学式的书写。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com