
3. NA代表阿伏加德罗常数,下列说法正确的是 ( )
A. 16g氧气所含的氧原子数为2NA
B. 18g水所含的电子数为NA
C. 2.4g金属镁与盐酸(足量)反应失去的电子数为0.1NA
D. 17g氨气所含电子数目为10NA
2. 下列情况中含微粒数目最多的是 ( )
A.
1mol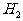 中的H原子 B. 0.5mol
中的H原子 B. 0.5mol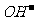 中的电子
中的电子
C.
0.6mol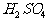 中的O原子 D.
1mol
中的O原子 D.
1mol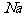 完全反应后失去的电子
完全反应后失去的电子
1. 与12.8g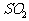 所含有原子数相等的NO的质量为
( )
所含有原子数相等的NO的质量为
( )
A. 3.0g B. 6.0g C. 9.0g D. 18.0g
10. (09年上海化学·31)烟气中NOx是NO和NO2的混合物(不含N2O4)。
 (1)根据废气排放标准,1m3烟气最高允许含400mgNOx。若NOx中NO质量分数为0.85,则1m3烟气中最高允许含NO
L(标准状况,保留2位小数)。
(1)根据废气排放标准,1m3烟气最高允许含400mgNOx。若NOx中NO质量分数为0.85,则1m3烟气中最高允许含NO
L(标准状况,保留2位小数)。
 (2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度1.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为
mol/L(保留2位小数)。
(2)工业上通常用溶质质量分数为0.150的Na2CO3水溶液(密度1.16g/mL)作为NOx吸收剂,该碳酸钠溶液物质的量浓度为
mol/L(保留2位小数)。
 (3)已知:NO+NO2+Na2CO3=2NaNO2+CO2 ①
(3)已知:NO+NO2+Na2CO3=2NaNO2+CO2 ①
 2NO2+Na2CO3=NaNO2+NaNO3+CO2 ②
2NO2+Na2CO3=NaNO2+NaNO3+CO2 ②
1m3 含2000mgNOx的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,吸收后的烟气
排放标准(填“符合”或“不符合”),理由:
。
含2000mgNOx的烟气用质量分数为0.150的碳酸钠溶液吸收。若吸收率为80%,吸收后的烟气
排放标准(填“符合”或“不符合”),理由:
。
 (4)加入硝酸可改变烟气中NO和NO2的比,反应为:
(4)加入硝酸可改变烟气中NO和NO2的比,反应为: NO+2HNO3=3NO2+H2O
NO+2HNO3=3NO2+H2O
 当烟气中n(NO)︰n(NO2)=2︰3时,吸收率最高
当烟气中n(NO)︰n(NO2)=2︰3时,吸收率最高
 1m3烟气含2000mgNOx,其中n(NO)︰n(NO2)=9︰1。
1m3烟气含2000mgNOx,其中n(NO)︰n(NO2)=9︰1。
 计算:(i)为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)。
计算:(i)为了达到最高吸收率,1m3烟气需用硝酸的物质的量(保留3位小数)。
 (ii)1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量(假设上述吸收反应中,反应①比反应②迅速。计算结果保留1位小数)
(ii)1m3烟气达到最高吸收率90%时,吸收后生成NaNO2的质量(假设上述吸收反应中,反应①比反应②迅速。计算结果保留1位小数)
答案:
 (1)0.25i
(1)0.25i
 (2)1.64
(2)1.64
 (3)不符合 因吸收后烟气总体积减小,NOx含量仍超过
(3)不符合 因吸收后烟气总体积减小,NOx含量仍超过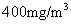
 (4)(i)
(4)(i)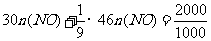 n(NO)=0.057mol
n(NO)=0.057mol
 NO+2HNO3=3NO2+H2O
NO+2HNO3=3NO2+H2O

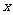
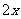
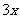

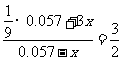
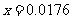 n(HNO3)=2x=0.035mol
n(HNO3)=2x=0.035mol
 (ii)
(ii)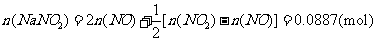

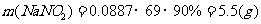

9. (09年广东化学·6)设NA 代表阿伏加德罗常数(NA )的数值,下列说法正确的是
A.1 mol 硫酸钾中阴离子所带电荷数为NA
B.乙烯和环丙烷(C3H6 )组成的28g混合气体中含有3NA 个氢原子
C.标准状况下,22.4L氯气与足量氢氧化钠溶液反应转移的电子数为NA
D.将0.1mol氯化铁溶于1L水中,所得溶液含有0.1NA Fe3+
答案:C
解析: K2SO4中阴离子为硫酸根,1mol硫酸根所带电荷为2mol,A错误。乙烯和C3H6的最简式相同均为CH2,28g混合气有2molCH2,所以含4molH原子,B错误。Fe3+在溶液中发生水解,0.1molFeCl3溶液中,Fe3+的物质的量要小于0.1mol,D错误。
8. (09年江苏化学·4)用NA表示阿伏加德罗常数的值。下列叙述正确的是
 A.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA
A.25℃时,pH=13的1.0L Ba(OH)2溶液中含有的OH-数目为0.2NA
 B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
B.标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
 C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
 D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
D.标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
 答案:C
答案:C
 解析:A项,pH=13也就是意味着c(H+)=1×10-13mol·L-1,则c(OH-)=1×10-1mol·L-1,所以n(OH-)=n(OH-)×V=1×10-1mol·L-1×1L=0.1mol,所以N(OH-)=0.1NA;B项,发生的化学反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O(该反应为歧化反应),n(Cl2)=0.1mol,那么转移电子的数目应该为0.1NA;C项,乙烯和丁烯的最简式都是CH2,则n(CH2)=
解析:A项,pH=13也就是意味着c(H+)=1×10-13mol·L-1,则c(OH-)=1×10-1mol·L-1,所以n(OH-)=n(OH-)×V=1×10-1mol·L-1×1L=0.1mol,所以N(OH-)=0.1NA;B项,发生的化学反应方程式为Cl2+2NaOH=NaCl+NaClO+H2O(该反应为歧化反应),n(Cl2)=0.1mol,那么转移电子的数目应该为0.1NA;C项,乙烯和丁烯的最简式都是CH2,则n(CH2)=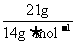 =1.5mol,所以n(C)=01.5mol,N(C)=1.5NA;D项,标准状况下,甲醇为液态,那么甲醇的物质的量就不是1mol,则所含有的氧原子个数也不为NA。
=1.5mol,所以n(C)=01.5mol,N(C)=1.5NA;D项,标准状况下,甲醇为液态,那么甲醇的物质的量就不是1mol,则所含有的氧原子个数也不为NA。
 [考点分析]以阿伏伽德罗常数为载体考察如下知识点①考查22.4L/mol的正确使用;②考查在氧化还原反应中得失电子数的计算;③正确表示一定物质的量的某物质微粒所含某种微粒的个数;④考查在标准状况下一定体积的气体分子所含的分子数和原子数。
[考点分析]以阿伏伽德罗常数为载体考察如下知识点①考查22.4L/mol的正确使用;②考查在氧化还原反应中得失电子数的计算;③正确表示一定物质的量的某物质微粒所含某种微粒的个数;④考查在标准状况下一定体积的气体分子所含的分子数和原子数。
7. (09年海南化学·8)下列叙述正确的是(用NA代表阿伏加德罗常数的值)
 A.2.4g金属镁变为镁离子时失去的电子数为0.1NA
A.2.4g金属镁变为镁离子时失去的电子数为0.1NA
 B.1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等
B.1molHCl气体中的粒子数与0.5 mo1/L盐酸中溶质粒子数相等
 C.在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 NA
C.在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 NA
 D.CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等
D.CO和N2为等电子体,22.4L的CO气体与lmol N2所含的电子数相等
答案:C
解析:A中镁为0.1mol,失去的电子数为0.2 NA;B中盐酸无体积,不能计算出粒子数;D选项中使用气体摩尔体积不是在标准状况下
6.(09年山东理综·10)下列关于氯的说法正确的是
A.Cl2具有很强的氧化性,在化学反应中只能作氧化剂
B.若35 17Cl、37 17若Cl为不同的核素,有不同的化学性质 学科
学科
C.实验室制备Cl2,可用排放和食盐水集气法收集
D.1.12LCl2含有1.7NA个质子(NA 表示阿伏伽德罗常数)
答案:C
 解析:本题以氯元素为载体,从氧化还原、原子结构、收集方法不同角度进行考查,体现了山东理综化学选择题的命题模式。氯气与水的反应既是氧化剂也是还原剂;同一元素的不同核素化学性质几乎完全相同而物理性质不同;D中提Cl2的体积未指明是标准状况。实验室制备Cl2,可用排饱和食盐水集气法收集也可用瓶口向上排空气法收集,故C正确。
解析:本题以氯元素为载体,从氧化还原、原子结构、收集方法不同角度进行考查,体现了山东理综化学选择题的命题模式。氯气与水的反应既是氧化剂也是还原剂;同一元素的不同核素化学性质几乎完全相同而物理性质不同;D中提Cl2的体积未指明是标准状况。实验室制备Cl2,可用排饱和食盐水集气法收集也可用瓶口向上排空气法收集,故C正确。
5.(08年山东理综·13)NA代表阿伏伽德罗常数,下列叙述错误的是A
A.10 mL质量分数为98%的H2SO4,用水稀释至100 mL,H2SO4的质量分数为9.8%
B.在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2 NA个电子
C.标准状况下,分子数为NA的CO、C2H4混合气体体积约为22.4 L,质量为28 g
D.一定温度下,1 L 0.50 mol·L-1NH4Cl溶液与2 L0.25mol·L-1NH4Cl溶液含NH4+物质的量不同
答案:A
解析:选项A中根据稀释前后溶质的质量不变得:10mL×ρ(前)×98%=100mL×ρ(后)×ω(后),所以ω(后)=,由于反应前后溶液的密度不能确定,所以其质量分数也不能确定;选项B中n(O2)=1mol,O元素的化合价从-1价变为0价,所以每个O原子失去1个电子,故反应中转移的电子数为2NA;选项C中分子数为NA的CO和C2H4其物质的量为1mol,则在标准状况下所占的体积为22.4L,由于它们的摩尔质量都是28g·mol-1,即平均摩尔质量也为28g·mol-1,所以其质量为28g;选项D中由于NH4++H2O NH3·H2O+OH-,浓度越小,水解程度越大,所以溶液中所含NH4+的物质的量不同。
NH3·H2O+OH-,浓度越小,水解程度越大,所以溶液中所含NH4+的物质的量不同。
4.(08年江苏化学·3)用NA表示阿伏加德罗常数的值。下列叙述正确的是C
A.常温常压下的33.6 L氯气与27 g铝充分反应,转移电子数为3NA
B.标准状况下,22.4 L己烷中共价键数目为19NA
C.由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA
D.1 L浓度为1 mol·L-1的Na2CO3溶液中含有NA个CO32-
答案:C
解析:选项A中n(Al)=1mol,Cl2的物质的量不能确定,当Cl2的物质的量小于1.5mol时,转移的电子数小于3NA,当Cl2的物质的量等于或大于1.5mol时,转移的电子数为1.5mol;己烷在标准状况下为液体,所以其物质的量不能用n=来确定;选项C中含有NA个分子的CO2和O2,其物质的量为1mol,而不管是CO2还是O2
1mol中均含有2mol的O,NA个CO2和O2的混合气体所含的O数为1mol;选项D中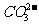 为弱酸根离子,水解后使得
为弱酸根离子,水解后使得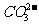 -的物质的量小于1mol,
-的物质的量小于1mol,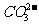 的个数小于NA。
的个数小于NA。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com