
16. M(NO3)2热分解化学方程式为:2 M(NO3)2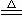 2MO+4NO2↑+O2↑。加热29.6g M(NO3)2使其完全分解,在标准状况下收集11200mL的气体,那么M的摩尔质量是
2MO+4NO2↑+O2↑。加热29.6g M(NO3)2使其完全分解,在标准状况下收集11200mL的气体,那么M的摩尔质量是
A.24g/mol B.40g/mol C.64g/mol D.65g/mol

15、在两种短周期元素组成的化合物中,它们的原子个数比为1:2,设两种元素的原子序数分别为a和b,则下列对a和b可能的关系概括得最完全的是
( )
①a+b=15 ②a=b+15 ③a=b-5 ④a+b=22
A. ①④
B. ①③④
C. ①②③④
D. ①②④

14、对下列事实的解释错误的是( )
A.在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
B.浓硝酸在光照下颜色变黄,说明浓硝酸不稳定
C.常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应
D.已知反应CuSO4 + H2S→CuS↓+ H2SO4能进行,这说明硫化铜既不溶于水也不溶于稀硫酸

13.目前人类已发现的非金属元素除稀有气体外,共有16种,下列对这16种元素的相关判断:①都是主族元素,最外层电子数都大于4;②单质在反应中都只能作氧化剂;③氢化物常温下都是气态,所以又都叫气态氢化物;④氧化物常温下都可以与水反应生成酸( )
A.只有①②正确 B.只有①③正确 C.只有③④正确
D.①②③④均不正确

12.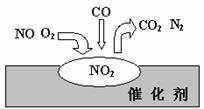 在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法错误的是( )
在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如图所示。下列说法错误的是( )
A.NO2是该过程的中间产物
B.NO和O2必须在催化剂表面才能反应
C.汽车尾气的主要污染成分包括CO和NO
D.催化转化总反应为:2NO+O2+4CO  4CO2+N2
4CO2+N2

11、如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )
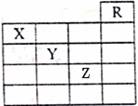 ①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐
①X的气态氢化物与Y的最高价氧化物对应的水化物能发生反应生成盐
②Y的氢化物沸点比它上一周期同族元素的氢化物沸点低 
③Z的单质在常温下是液体
④Z的原子序数比Y大19 
⑤Z所在的周期中含有32种元素
A.①②③④ B.①②③④⑤ C.只有③ D.只有①④

10.在给定条件下,下列加点的物质在化学反应中能被完全消耗的是( )

A、用浓硫酸与足量Cu反应

B、标准状况下,将1g铝片投入到20mL18mo1/L的硫酸中

C、向100mL 3mo1/L的硝酸中加入5.6g铁

D、在5×107Pa、500℃和铁触媒催化的条件下,用氮气和足量氢气合成氨 


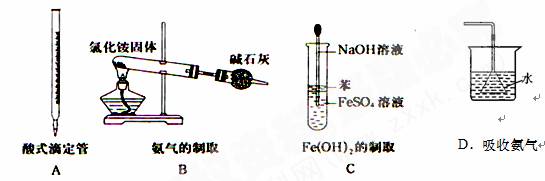
9、下图所示对实验仪器名称的标注或实验操作正确的是
|

8.砷(As)的原子结构为则下列叙述中正确的是
A.在AsCl3分子中,As的最外电子为8个 
B.As的氢化物为AsH3,是一种强氧化剂
C.As的相对原子质量为74.92,由此可知As中子数为42
D.H3AsO4是强酸

7.下列变化中,属于物理变化的是
( )
①加热氨水可得到氨气 
②氯化铵晶体受热后由试管底部移到试管上部 
③固体碘受热变成紫红色气体 
④液氨气化 
⑤浓硝酸从无色液体变成黄色液体
A.①③④ B.③④ C.②③④ D.③④⑤

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com