
20.
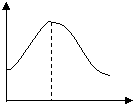 把镁条投入盛有盐酸的敞口容器中,产生氢气速率变化
把镁条投入盛有盐酸的敞口容器中,产生氢气速率变化
如图所示。下列因素中,影响反应速率的因素是( )
①盐酸的浓度 ②镁条的表面积 ③溶液的温度
④Cl-的浓度
A.①④ B.③④
C.①②③ D.②③ t
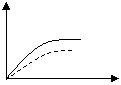
19.将ag块状碳酸钙跟足量的盐酸反应,反应物损失的质量随时间的变化曲线如图中的实线所示,在相同条件下,将bg(a>b)粉末状碳酸钙与同浓度的盐酸反应,则相应的曲线如图中的
虚线所示。其中正确的是( )







0 t 0 t 0 t O t
A B C D
18.下列各组反应(表中物质均为反应物):刚开始时,放出H2的速率最大的是( )
|
编号 |
金属(粉末状) |
物质的量(mol) |
酸的浓度 |
酸的体积 |
反应温度 |
|
A |
Mg |
0.1 |
6mol/LHNO3 |
10mL |
60℃ |
|
B |
Mg |
0.1 |
3mol/LHCl |
10mL |
60℃ |
|
C |
Fe |
0.1 |
3mol/LHCl |
10mL |
60℃ |
|
D |
Mg |
0.1 |
3mol/LHCl |
10mL |
60℃ |
17.已知中和热的数值是57.3KJ/mol。下列反应物混合时,产生的热量等于57.3KJ的是( )
A.1mol/L稀HCl(aq)和1mol/L稀NaOH(aq)
B.500mL2.0mol/L的HCl(aq)和500mL2.0mol/L的NaOH(aq)
C.500mL2.0mol/L的CH3COOH(aq)和500mL2.0mol/L的NaOH(aq)
D.1mol/L稀CH3COOH(aq)和1mol/L稀NaOH(aq)
16.可逆反应H2(g)+I2(g)==I2(g)达到平衡时的标志是( )
A、混合气体密度恒定不变 B、混合气体的颜色不再改变
C、H2、I2、HI的浓度相等 D、I2在混合气体中体积分数不变
15.理论上不能设计为原电池的化学反应是,注:△H<0 为放热反应( )
A.CH4(g)+2O2(g)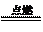 CO2(g)+2H2O(l);△H<0
CO2(g)+2H2O(l);△H<0
B.HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(aq);△H<0
C.2H2(g)+O2(g)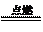 2H2O(g);△H<0
2H2O(g);△H<0
D.2FeCl3(l)+Fe(s)==3FeCl2(l);△H<0
14.铁制自来水管与下列材料作成的自来水龙头连接,自来水管锈蚀最快的是( )
A.铁水龙头 B.铜水龙头 C.塑料水龙头 D.陶瓷水龙头
13.已知空气-锌电池的电极反应为:锌片:Zn+2OH--2e-=ZnO;碳棒: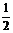 O2+H2O+2e-=2OH-,据此判断,锌片是( )
O2+H2O+2e-=2OH-,据此判断,锌片是( )
A.正极并被还原 B.正极并被氧化 C.负极并被还原 D.负极并被氧化
12.下图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )
A. a电极是负极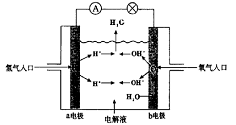
B. b电极的电极反应为:4OH--4e-=2H2O +O2↑
C. 氢氧燃料电池是一种具有应用前景的绿色电源
D. 氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
11.纯锌跟稀H2SO4反应速率很小,为了加快锌的溶解和放出H2的速率,并且使产生H2的量不变,当稀H2SO4过量时,可向其中加少量( )
A.CuSO4溶液 B.ZnSO4 C.铜 D.镁条
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com