
5. ( )向100 mL 2 mol·L-的AlCl3溶液中,逐滴加入NaOH溶液100 mL产生沉淀为7.8 g,则加入NaOH溶液的物质的量浓度是
A.1 mol·L- B.1.5 mol·L- C.3 mol·L- D.7 mol·L-
4. ( )将镁、铝、硅的混合物分为等质量的两份,一份跟足量的NaOH溶液反应,另一份跟足量的盐酸反应,最终产生的H2一样多,则镁与硅物质的量之比为
A.2∶1 B.4∶1 C.1∶1 D.3∶1
3.( )下列各组物质中的每一种均既能与NaOH溶液反应,又能与稀H2SO4反应的是
A. NaHCO3 Al2O3 Al(OH)3 B.NH4NO3 AgNO3 [Ag(NH3)2]OH
C. NaHSO4 NaHSO3 NaHS D. Al AlCl3 KAlO2
2.( )在托盘天平右盘上放一个盛有100 mL 3 mol/LNaOH溶液的烧杯,左盘上放一个盛有100 mL 3 mol/L盐酸的烧杯,调节天平至平衡,然后在两烧杯中各加入等质量的铝片,反应完全后,则天平可能出现的情况是 A.左盘下沉 B.右盘下沉 C.仍保持平衡 D.无法判断
1. ( )下列各组反应中,最后得到Al(OH)3沉淀的是
A.将Al2O3固体粉末加到沸水中 B .将CO2气体通入NaAlO2溶液中
C.将过量金属钠投入到NaAlO2溶液中 D.向200毫升1mol/LNaOH溶液中加入50ml 1mol/L的AlCl3溶液
下列各图中的纵坐标表示沉淀的物质的量,横坐标表示加入x的物质的量,请将各图一一对应的反应的代号填入每图下方的括号内。


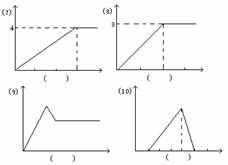 A、Ca3(PO4)2悬浊液中滴入H3PO4 B、NaAlO2溶液中通入HCl
C、Ba(OH)2溶液中通入SO2 D、石灰水中通入CO2 E、AlCl3溶液中滴入氨水
F、AlCl3溶液中滴入NaAlO2溶液 G、SO2溶液中通入H2S气体
H、稀硫酸中滴入Ba(OH)2溶液 I、AlCl3、MgSO4的混合溶液中加入过量NaOH溶液
J、在盐酸酸化的AlCl3溶液中,滴入KOH溶液 K、AlCl3溶液中滴入NaOH溶液
A、Ca3(PO4)2悬浊液中滴入H3PO4 B、NaAlO2溶液中通入HCl
C、Ba(OH)2溶液中通入SO2 D、石灰水中通入CO2 E、AlCl3溶液中滴入氨水
F、AlCl3溶液中滴入NaAlO2溶液 G、SO2溶液中通入H2S气体
H、稀硫酸中滴入Ba(OH)2溶液 I、AlCl3、MgSO4的混合溶液中加入过量NaOH溶液
J、在盐酸酸化的AlCl3溶液中,滴入KOH溶液 K、AlCl3溶液中滴入NaOH溶液
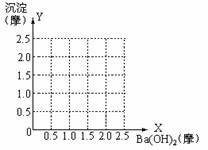
[思考]有Al2(SO4)3和MgSO4的混合物,用适量的水将混合物完全溶解
再加入KOH溶液,析出沉淀的质量随加入KOH溶液体积变化,如图
则混和物中Al2(SO4)3和MgSO4的物质的量之比是 。
①Al3+不能与下列离子大量共存:OH-、CO32-、HCO3-、S2-、HS-、AlO2-等
②AlO2-不能与下列离子大量共存:H+、HCO3-、NH4+、Al3+等
3.明矾(化学式 )
 是____色晶体,易溶于水,在水中的电离方程式_______________________________;明矾能够净水其离子方程式为__________________________________。
是____色晶体,易溶于水,在水中的电离方程式_______________________________;明矾能够净水其离子方程式为__________________________________。
[例题]向明矾[KAl(SO4)2·12H2O]溶液中逐滴加入Ba(OH)2溶液至过量。 (1)当明矾为1mol时,试在图中画出生成的每种沉淀物质的量随
Ba(OH)2物质的量变化的曲线(表明化学式) (2)当向体积为1L 1mol/L的明矾溶液中滴加
aL 0.5mol/L的Ba(OH)2溶液时,用含a的代数式表示:
①当a满足 时,沉淀的总物质量最大
②当a满足 时,沉淀的总质量最大



 四、Al与其化合物的转化关系(铝三角) Al
四、Al与其化合物的转化关系(铝三角) Al
 AlCl3 NaAlO2
AlCl3 NaAlO2


Al(OH)3
2.氢氧化镁和氢氧化铝
Mg(OH)2的电离方程式:
Al(OH)3:_________色______状物,是典型的_____。氢氧化铝的电离方程式:_________;当向 Al(OH)3中加入强酸时,平衡向____移动;当向 Al(OH)3中加入强碱时,平衡向____移动。典型的 性氢氧化物:①Al(OH)3+H+ ②Al(OH)3+OH-
②Al(OH)3+OH- 实验室制备 Al(OH)3时,选用铝盐和氨水作用而不选氢氧化钠溶液的原因是____________。写出实验室制备氢氧化铝的离子方程式________________________________________。
实验室制备 Al(OH)3时,选用铝盐和氨水作用而不选氢氧化钠溶液的原因是____________。写出实验室制备氢氧化铝的离子方程式________________________________________。
受热能分解: Al(OH)3
1. 氧化镁和氧化铝
MgO、 Al2O3是白色的难熔物质,较好的耐火材料。MgO是典型的 性氧化物,Al2O3是典型的 性氧化物:既能溶于强酸,又能溶于强碱
Al2O3+ H+ Al2O3+OH-
Al2O3+OH-
电解制备铝单质: Al2O3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com