
| 实验操作 | 实验现象 | 实验结论 |
| 操作一:取天然碱样品少量溶于足量水后,加入过量的CaCl2稀溶液(如果操作一有沉淀,则进行操作二) | 无沉淀出现 | 假设一成立 |
| 操作二:待操作一中反应充分后过滤,并在滤液中加入过量的Ca(OH)2溶液,观察. | 无沉淀出现 | 假设二成立 |
| 产生白色沉淀 | 假设三成立 |
分析 Ⅰ.(1)碳酸钠和碳酸氢钠中阴离子对应的酸都是碳酸;
(2)碳酸氢钠能和胃酸中的稀盐酸反应生成氯化钠、水和二氧化碳;
Ⅱ.碳酸氢钠受热分解生成碳酸钠、水和二氧化碳;
二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水;
【假设猜想】
天然碱成分可能是碳酸氢钠,也可能是碳酸钠,或碳酸氢钠和碳酸钠;
【实验方案】
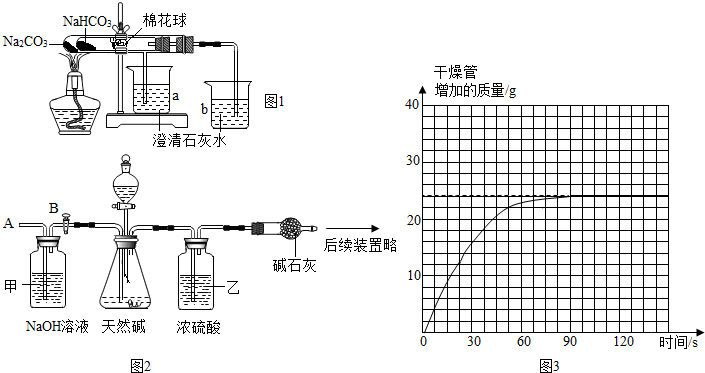
如果澄清石灰水不能变浑浊,说明是碳酸钠,如果澄清石灰水变浑浊,说明是碳酸氢钠,或碳酸氢钠和碳酸钠;
为了防止实验装置漏气影响实验结果,应该检查装置的气密性;
稀硫酸不具有挥发性;
氢氧化钠溶液能够吸收二氧化碳;
浓硫酸具有吸水性,可以用来干燥二氧化碳气体;
根据提供的数据可以计算试样中碳酸氢钠的质量分数.
解答 解:Ⅰ.(1)碳酸钠和碳酸氢钠中阴离子对应的酸都是H2CO3;
(2)碳酸氢钠在医疗上用作治疗胃酸过多,反应的化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑.
故填:H2CO3;NaHCO3+HCl=NaCl+H2O+CO2↑.
Ⅱ.①结论:碳酸氢钠受热分解出水和CO2等物质;
②b烧杯中,二氧化碳和氢氧化钙反应生成碳酸钙和水,发生反应的化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O.
故填:碳酸氢钠;CO2+Ca(OH)2═CaCO3↓+H2O.
【假设猜想】
天然碱成分可能是碳酸氢钠,也可能是碳酸钠,或碳酸氢钠和碳酸钠.
故填:碳酸氢钠和碳酸钠.
【实验方案】
方案一:这种方案不合理,理由是:如果澄清石灰水不能变浑浊,说明是碳酸钠,如果澄清石灰水变浑浊,说明是碳酸氢钠,或碳酸氢钠和碳酸钠,即只能得出是否含有碳酸氢钠或碳酸钠,不能判断是否同时含有碳酸氢钠和碳酸钠.
故填:否;只能得出是否含有碳酸氢钠或碳酸钠,不能判断是否同时含有碳酸氢钠和碳酸钠.
方案二:操作一:取天然碱样品少量溶于足量水后,加入过量的 CaCl2稀溶液,无沉淀出现,假设一成立;
操作二:待操作一中反应充分后过滤,并在滤液中加入过量的 Ca(OH)2溶液,如果不产生沉淀,说明假设二成立;
如果产生白色沉淀,说明假设三成立.
故填:CaCl2稀溶液;Ca(OH)2溶液;无沉淀出现;产生白色沉淀.
Ⅲ.①步骤(1)加入样品前还应检查装置的气密性,所加的酸溶液最好是稀硫酸.
故填:检查装置的气密性;稀硫酸.
②装置甲的作用是吸收空气中的二氧化碳;
装置乙的作用是吸收二氧化碳中混有的水蒸气;
第(4)步再次从导管A处缓缓鼓入一定量的空气的作用是使反应生成的二氧化碳全部被碱石灰吸收.
故填:吸收空气中的二氧化碳;吸收二氧化碳中混有的水蒸气;使反应生成的二氧化碳全部被碱石灰吸收.
③设碳酸氢钠的质量为x,反应生成二氧化碳的质量为y,
由图中数据可知,反应生成二氧化碳的质量为22g,
NaHCO3+HCl═NaCl+H2O+CO2↑,Na2CO3+2HCl═2NaCl+H2O+CO2↑,
84 44 106 44
x y 52.5g-x 22g-y
$\frac{84}{44}$=$\frac{x}{y}$,$\frac{106}{44}$=$\frac{52.5g-x}{22g-y}$,
x=1.9g,
则碳酸氢钠的质量分数为:$\frac{1.9g}{52.5g}$×100%=3.6%,
答:试样中碳酸氢钠的质量分数是3.6%.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
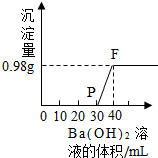 已知某混合液由HCl、K2CO3、H2SO4、CuCl2、NaCl溶液中的几种混合而成,向该混合液中加Ba(OH)2溶液,产生沉淀量与加的Ba(OH)2溶液体积关系如图.则下列说法正确的是( )
已知某混合液由HCl、K2CO3、H2SO4、CuCl2、NaCl溶液中的几种混合而成,向该混合液中加Ba(OH)2溶液,产生沉淀量与加的Ba(OH)2溶液体积关系如图.则下列说法正确的是( )| A. | 混合液一定是HCl和CuCl2混合而成 | B. | 混合液中一定没有K2CO3和H2SO4 | ||
| C. | F点溶液中的溶质肯定只有一种 | D. | 沉淀完全时,消耗Ba(OH)26.84g |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 现象 | 有关反应的化学方程式 |
| 要少量固体B,滴加 稀盐酸 | 有气泡产生 | Zn+2HCl═ZnCl2+H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com