
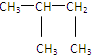 ⑩
⑩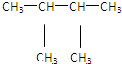 ⑪${\;}_{17}^{35}$Cl⑫
⑪${\;}_{17}^{35}$Cl⑫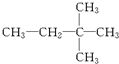
分析 同系物指结构相似、通式相同,组成上相差1个或者若干个CH2原子团,具有相同官能团的化合物;
具有相同分子式而结构不同的化合物互为同分异构体;
同种元素形成的不同单质互为同素异形体;
质子数相同质量数(或中子数)不同的原子互称同位素;
组成和结构都相同的物质为同一物质,同一物质组成、结构、性质都相同,结构式的形状及物质的聚集状态可能不同.
解答 解:②CH3-CH-CH3⑨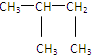 ;⑥CH3-CH2-CH2-CH3⑩
;⑥CH3-CH2-CH2-CH3⑩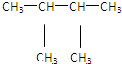 都是烷烃,组成上相差1个CH2原子团,互为同系物;
都是烷烃,组成上相差1个CH2原子团,互为同系物;
⑩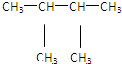 ⑫
⑫ 具有相同分子式而结构不同,互为同分异构体;
具有相同分子式而结构不同,互为同分异构体;
③白磷⑦红磷是同种元素形成的不同单质,互为同素异形体;
⑧${\;}_{17}^{37}$Cl⑪${\;}_{17}^{35}$Cl质子数相同中子数不同,互称同位素;
①液氯④氯气都是氯气,是同一物质;
故答案为:②(或⑨)和⑥⑩;③和⑦;⑧和⑪;①和④.
点评 本题考查“五同”比较,题目难度不大,侧重考查学生的辨别能力,选项多,要细心排查.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
 金属镍及其化合物在合金材料以及催化剂等方面应用广泛.根据要求回答下列问题.
金属镍及其化合物在合金材料以及催化剂等方面应用广泛.根据要求回答下列问题. )作用生成腥红色配合物沉淀A.
)作用生成腥红色配合物沉淀A.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 0 | 2 | 4 | 6 | 8 | 10 |
| V(O2)/mL | 0.0 | 9.6 | 16.8 | 22.4 | 26.5 | 29.9 |
| A. | 2 min时H2O2的浓度c(H2O2)=0.314 mol/L | |
| B. | 0~4 min的平均反应速率v(H2O2)=3.75×10-2 mol/(L•min) | |
| C. | 0~10 min内,过氧化氢的分解速率逐渐加快 | |
| D. | 反应到6 min时,H2O2分解了50% |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 25℃时,用浓度为0.1000mol•L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol•L-1的三种酸HX、HY、HZ滴定曲线如图所示.下列说法正确的是( )
25℃时,用浓度为0.1000mol•L-1的NaOH溶液滴定20.00mL浓度均为0.1000mol•L-1的三种酸HX、HY、HZ滴定曲线如图所示.下列说法正确的是( )| A. | 根据滴定曲线,可得Ka(HY)≈10-9 | |
| B. | 在相同温度下,同浓度的三种酸溶液的导电能力顺序:HZ<HY<HX | |
| C. | HY与HZ混合,达到平衡时:c(H+)=$\frac{Ka(HY)•c(HY)}{c({Y}^{-})}$+c(Z-)+c(OH-) | |
| D. | 将上述HX、HY溶液等体积混合后,用NaOH溶液滴定至HX恰好完全反应时:c(Na+)>c(Y-)>c(X-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢硫酸显弱酸性:H2S?2H++S2- | |
| B. | Na2CO3水溶液显弱碱性:CO32-+2H2O?H2CO3+2OH- | |
| C. | 用铜电极电解饱和NaCl溶液:阳极反应式是:2Cl--2e-=Cl2↑ | |
| D. | 用稀硝酸洗去试管中的银镜:3Ag+NO3-+4H+=3Ag++NO↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗下层液体从下口放出,上层液体从上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 碘的四氯化碳溶液可用萃取的方法分离出四氯化碳 | |
| D. | 配制稀硫酸时,先向烧杯中注入适量蒸馏水,再缓慢注入浓硫酸,并用玻璃棒不断搅拌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com