
 ��1�����dz��ô�����ѡ��Ӧ���еķ�����ͼ��ʾΪһ��������1mol CH3OH��O2������Ӧʱ������CO��CO2��HCHO�������仯ͼ[��Ӧ��O2��g����������H2O��g����ȥ]��
��1�����dz��ô�����ѡ��Ӧ���еķ�����ͼ��ʾΪһ��������1mol CH3OH��O2������Ӧʱ������CO��CO2��HCHO�������仯ͼ[��Ӧ��O2��g����������H2O��g����ȥ]��| �¶ȣ��棩 | 250 | 300 | 350 |
| K | 2.041 | 0.270 | 0.012 |
| ʱ�䣨min�� | 5 | 10 | 15 | 20 | 25 | 30 |
| ѹǿ�ȣ�P��/Pǰ�� | 0.98 | 0.90 | 0.80 | 0.70 | 0.70 | 0.70 |
| n��SO32-����n��HSO3-�� | 91��9 | 1��1 | 1��91 |
| pH | 8.2 | 7.2 | 6.2 |
���� ��1����ʹ�ô������Խ��ͷ�Ӧ�Ļ�ܣ����Խ�ͣ���ͨ����Խ����ת���ɻ���ӣ���ӦԽ���ף���Ӧ����Խ�죻
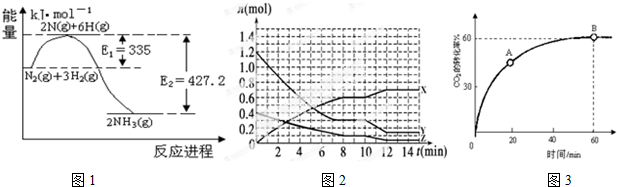
����ͼ����֪2HCHO��g��+O2��g���T2CO��g��+2H2O��g���з�Ӧ�������ߣ������������ͣ��ʸ÷�ӦΪ���ȷ�Ӧ����ͼ��֪1mol��ȩ��Ӧ�ų�����Ϊ��676-158-283��kJ��
���Ȼ����м��백ˮ��������Ϸ�Ӧ��������������ӣ�
��2���ټ���Ũ���̣��뻯ѧƽ�ⳣ����Դ�Сȷ����Ӧ�������Qc=K������ƽ��״̬��Qc��K����Ӧ������Ӧ���У�Qc��K����Ӧ���淴Ӧ���У�
���¶ȡ��������Ŀ��淴Ӧ�У������ѹǿ֮�ȵ��������ʵ���֮�ȣ��ݴ˼��㷴Ӧ��������������ʵ������Ӷ�����������Ӧ�����ʵ������ٸ���v=$\frac{\frac{��n}{V}}{��t}$���㷴Ӧ���ʣ�
20min����ƽ�⣬����ƽ��ʱ�����ʵ����������ò���������μӷ�ӦCO���ʵ�������������COת���ʣ�
��3�����ɱ����е����ݿ�֪��HSO3-Խ�࣬����Խǿ����������������ӣ�
��a��������������ӵ���̶ȴ���ˮ��̶ȣ���Һ�����ԣ��������ˮ��̶ȶ���С��ˮ������������ӣ�
b�����������غ��c��Na+��=c��SO32-��+c��HSO3-��+c��H2SO3����������������ӵ���̶ȴ���ˮ��̶ȣ�����c��SO32-����c��H2SO3����
c����Һ�д��ڵ���غ�c��Na+��+c��H+��=2c��SO32-��+c��HSO3-��+c��OH-���������غ�c��Na+��=c��SO32-��+c��HSO3-��+c��H2SO3����
d�����ݵ���غ��c��Na+��+c��H+��=2c��SO32-��+c��HSO3-��+c��OH-����
��� �⣺��1���ٸ���ͼ����Կ���ת���ɼ�ȩʱ�����ͣ�ʹ�ô���ʱ��Ҫ����ΪHCHO��
2HCHO��g��+O2��g���T2CO��g��+2H2O��g���÷�ӦΪ���ȷ�Ӧ����H=-2��676-158-283��=-470KJ•mol-1��
�ʴ�Ϊ��HCHO��-470KJ•mol-1��
���Ȼ����백ˮ������Ϸ�Ӧ�����ӷ���ʽ��AgCl+2NH3•H2O=Ag��NH3��2++Cl-+2H2O����AgCl+2NH3=Ag��NH3��2++Cl-��
�ʴ�Ϊ��AgCl+2NH3•H2O=Ag��NH3��2++Cl-+2H2O��AgCl+2NH3=Ag��NH3��2++Cl-��
��2����Ũ����Qc=$\frac{0.8}{0.4��0��{4}^{2}}$=12.5��2.041����ƽ�����淴Ӧ�����ƶ������Է�Ӧ����v����v����
�ʴ�Ϊ������
���¶ȡ��������Ŀ��淴Ӧ�У������ѹǿ֮�ȵ��������ʵ���֮�ȣ�15minѹǿ�ȣ�P��/Pǰ��=0.80����Ӧ����������ʵ���=3mol��0.80=2.40mol��������ٵ����ʵ���=3mol-2.4mol=0.6mol��CO��g��+2H2��g��?CH3OH��g���и���������ٵ����ʵ���������֮��Ĺ�ϵʽ֪���μӷ�Ӧ�����������ʵ���0.6mol���������ķ�Ӧ����=$\frac{\frac{0.6mol}{2L}}{15min}$=0.02 mol•�� L•min��-1��
20min����ƽ��״̬����ʱ������������ʵ���Ϊ3mol��0.7=2.1mol����������ٵ����ʵ���=3mol-2.1mol=0.9mol������1molCO��Ӧ�����ʵ�����С2mol����μӷ�Ӧ��CO�����ʵ���=$\frac{0.9mol}{2}$=0.45mo����CO��ת����=$\frac{0.45mol}{1mol}$=45%��
�ʴ�Ϊ��0.02 mol•�� L•min��-1��45%��
��3�����ɱ����е����ݿ�֪��HSO3-Խ�࣬����Խǿ����������������ӣ����뷽��ʽΪHSO3-?H++SO32-����������������������ˮ�⣬
�ʴ�Ϊ���
��a��������������ӵ���̶ȴ���ˮ��̶ȣ���Һ�����ԣ��������ˮ��̶ȶ���С��ˮ������������ӣ����Ը���Һ������Ũ�ȴ�С˳����c��Na+����c��HSO3-����c��H+����c��SO32-����c��OH-������a��ȷ��
b�����������غ��c��Na+��=c��SO32-��+c��HSO3-��+c��H2SO3����������������ӵ���̶ȴ���ˮ��̶ȣ�����c��SO32-����c��H2SO3��������c��Na+����2c��SO32-��+c��HSO3-������b����
c����Һ�д��ڵ���غ�c��Na+��+c��H+��=2c��SO32-��+c��HSO3-��+c��OH-���������غ�c��Na+��=c��SO32-��+c��HSO3-��+c��H2SO3�������Ե�c��H2SO3��+c��H+��=c��SO32-��+��OH-������c��ȷ��
d�����ݵ���غ��c��Na+��+c��H+��=2c��SO32-��+c��HSO3-��+c��OH-������d����
��ѡ��ac��
���� ���⿼�黯ѧƽ����㡢ƽ�ⳣ��Ӧ�á���Ӧ�ȼ��㡢����Ũ�ȴ�С�Ƚϵȣ��Ƕ�ѧ���ۺ������Ŀ��飬��Ҫѧ���߱���ʵ�Ļ��������������������Ŀ�Ѷ��еȣ�


 ��ĩ�����ϵ�д�
��ĩ�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| ѡ�� | X | Y | Z | M |
| A | O2 | CO2 | CO | C |
| B | HNO3 | Fe��NO3��3 | Fe��NO3��2 | Fe |
| C | NaOH | NaHCO3 | Na2CO3 | CO2 |
| D | NH3 | NO | NO2 | O2 |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

 C6H5COOCH3+H2O��
C6H5COOCH3+H2O��
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

| ������ | ������ | ���������� | ������ | |
| �ܶ�/��g/cm3�� | 0.810 | 1.049 | 0.882 | 0.7689 |
| �е�/�� | 118.0 | 118.1 | 126.1 | 142 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��������һ����Ҫ���л�����ԭ�ϣ���е�Ϊ38.4�森�Ʊ��������һ�ַ������Ҵ��������ᷴӦ��
��������һ����Ҫ���л�����ԭ�ϣ���е�Ϊ38.4�森�Ʊ��������һ�ַ������Ҵ��������ᷴӦ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ȩ��֬��phenolic resin��������ϳɵĵ�һ�ָ߷��Ӳ��ϣ������Ա��㷺ʹ�ã�ijУ��ѧ��ȤС���ͬѧͨ�����з�����ʵ�����Ʊ���ȩ��֬��
��ȩ��֬��phenolic resin��������ϳɵĵ�һ�ָ߷��Ӳ��ϣ������Ա��㷺ʹ�ã�ijУ��ѧ��ȤС���ͬѧͨ�����з�����ʵ�����Ʊ���ȩ��֬�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 3s23p63d2 | B�� | 2d10 | C�� | 3s23p64s2 | D�� | 3s23p33d5 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ˮԽ����������Խ���� | |
| B�� | ��ζ����Ӫ�����ӵ�Խ��Խ�� | |
| C�� | ����������������Դ�������ã������������к��������ɻ������� | |
| D�� | Ϊ������ȱ��֢���������涨������ʳ���мӵⵥ�� |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com