
题目列表(包括答案和解析)
1.下列有关微生物的叙述中,错误的是( )
A.无机氮源不可能为微生物提供能量
B.组成酶是微生物细胞内一直存在的酶,它们的合成只受遗传物质的控制
C.改变微生物的遗传特性,可实现对微生物代谢的人工控制
D.微生物的连续培养有助于延长稳定期,提高代谢产物的产量,并缩短培养周期
31.(16分)小麦是自花传粉植物。在种植白色粒小麦的田间偶然发现有一株小麦所结籽粒为红色。研究表时红色籽粒小麦是由种皮中色素所引起的。第二年将该小麦的800多颗红色籽粒播种后,有600多株以育成熟,其中有160多株结白色籽粒,其余仍结红色籽粒。(答题中基因型用A表示显性基因,a表示隐性基因。)
(1)最初产生结红色籽粒植株的原因很可能是由于 ;红色籽粒中胚的基因型是 。
(2)若采用单倍体育种的方法尽快获得稳定遗传的红色籽粒小麦品种。具体步骤是:
①将最初得到的红色籽粒播种后,最好培养至 (传粉前/传粉后),取
进行离体培养;
②待得到 时,用秋水仙素处理使其 后,培养至成熟;得到的植株基因型为 。
③待 时,选红色籽粒留种。
30.I.(14分)下图甲表示春季晴天某密闭大棚内一昼夜CO2浓度的变化。乙图曲线表示某种植物在20℃、CO2浓度为0.03%的环境中随着光强度的变化光合速率的变化;在B点时改变某种环境条件,结果发生了如曲线b的变化。请分析回答。

(1)甲图中,一昼夜中CO2浓度最高和最低的时间点分别是a时和b时,在这两个时点,植物光合作用强度 (大于、等于、小于)呼吸作用强度。
(2)分析乙图在B点时改变的某种条件可能是(列举两种情况):
可能①: ,理由: 。
|
(3)乙图中A点与C点相比较,C点时刻叶绿体中C3的含量 、NADPH的含量 。
II.(12分)为比较两种形态和习性上很接近的原生动物在相同条件下的繁殖速度,某学校研究性学习小组进行了以下实验:
第一步:各取1个原生动物A和B,以同一种杆菌为饲料,分别放在两个大小不同的容器中,在相同且适宜的条件下单独培养;
第二步:定期统计两个容器中的原生动物种群数量,记录在表格中。
(1)上述实验步骤中有两处不妥之处,请分虽指出:
① ;②
 (2)若修改后进行实验,记录结果如下表:(单位:个)
(2)若修改后进行实验,记录结果如下表:(单位:个)
天数 个数 个数种类 |
2 |
4 |
6 |
8 |
10 |
12 |
14 |
16 |
|
A |
15 |
60 |
80 |
81 |
80 |
82 |
81 |
80 |
|
B |
12 |
35 |
50 |
60 |
61 |
62 |
60 |
62 |
请分析回答下列问题:
①原生动物A单独培养6天后,种群数量趋于稳定、生态学上称此数量为 。
②由实验数据可以看出,单独培养时,A、B种群增长都属于 型增长。
③如果将A、B放在同一个容器中混合培养,能够在生存中占优势的是A《判断的理由是 。但当它达到稳定状态时,种群数量比单独培养时要 (填“多”或“少”)
29.(13分)已知烯烃通过臭氧化并经锌和水处理发生如下变化,其中(I)和(II)均能被H2还原为醇。
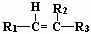
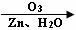
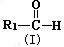 +
+ 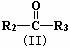 (R1、R2、R3均为烷基)
(R1、R2、R3均为烷基)
(1)上述反应的生成物(I)中含有官能团的名称是
(2)某一氯代烃A分子式为C6H13Cl,它可以发生如下转化:

试回答:
①A→B的反应类型为 。
②若化合物B的某种同分异构体通过臭氧化并经锌和水处理,只得到一种产物且为醛,则上述转化后得到化合物G的结构简式为 。
③若化合物B的某种同分异构体通过臭氧化并经锌和水处理得到甲醛和另一种醛,符合该条件的B的结构有4种,结构简式分别为:CH2=CH-CH2-CH2-CH2-CH3、
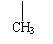
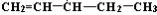 、
、
。
、
、
。
④若经过结构分析表明,化合物B通过加氢反应后分子中生成2个“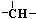 ”(次甲基),则化合物D的结构简式为
,反应E→G的化学方程式为
。
”(次甲基),则化合物D的结构简式为
,反应E→G的化学方程式为
。
28.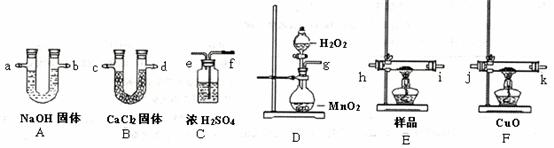 (18分)2008年9月,中国的三聚氰胺污染牛奶事件,在社会上造成了很坏的影响。牛奶和奶粉中添加三聚氰胺,主要是因为它能冒充蛋白质。已知三聚氰胺中含有碳、氢、氮三种元素,其相对分子质量为126,为测定三聚氰胺的组成,用下列各仪器装置,在过量的氧气流中将2.52g三聚氰胺样品氧化成CO2、H2O和N2。回答下列问题:
(18分)2008年9月,中国的三聚氰胺污染牛奶事件,在社会上造成了很坏的影响。牛奶和奶粉中添加三聚氰胺,主要是因为它能冒充蛋白质。已知三聚氰胺中含有碳、氢、氮三种元素,其相对分子质量为126,为测定三聚氰胺的组成,用下列各仪器装置,在过量的氧气流中将2.52g三聚氰胺样品氧化成CO2、H2O和N2。回答下列问题:
(1)产生的氧气按从左向右流向,所选装置各导管的连接顺序是:g接 、 接
、 接 、 接 、 接 。
(2)装置C的作用是 ;装置F中CuO的作用是 ;
装置D中发生反应的化学方程式是 。
(3)实验前后称得A、B两装置的质量分别增加2.64g和1.08g,则三聚氰胺分子中碳、氢、氮的原子个数比为 。
(4)目前较多采用以尿素为原料,在0.1MPa下,390℃左右时,以硅胶做催化剂合成三聚氰胺。反应过程中,除生成CO2外,还生成一种使湿润的红色石蕊试纸变蓝的气体,试写出制备三聚氰胺的化学方程式(有机物可用分子式表示) 。
(5)按(1)的连接方法,此实验装置存在的缺点是 ,原因是
27.(15分)A、B、D、X、Y是由短周期元素组成的化合物,其中X是常见的强酸、Y是
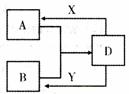 常见的强碱,它们的相互转化关系如右图(部分生成物和水略去)
常见的强碱,它们的相互转化关系如右图(部分生成物和水略去)
(1)若A、B均为气体,在水溶液中反应生成D,其中A具有漂
白性,则A的化学式为 ,B发生催化氧化的化学方程式
为 。
(2)若A、B、D含有相同的金属元素,工业用电解熔融氧化物的
方法制取该金属单质。则此金属元素在周期表中的位置为
。现将X滴入B的溶液中至过量,观察到
的现象是 。
(3)若A为非极性分子,灼烧B、D、Y时火焰均为黄色。写出D+Y→B的离子方程式 。现将标准状况下1.12 L的A通入60 mL l mol/L的B溶液中,则反应后溶液中含有的溶质的物质的量之比(不考虑水解,自定比例顺序) 。
(4)现用右图装置电解某浓度Y的水溶液,则下列叙述中不正确的是(填序号) 。
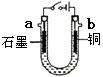 ①电解过程中,阴极区溶液pH增大
①电解过程中,阴极区溶液pH增大
②电解一段时间后U型管内将有蓝色沉淀产生
③当电路中转移0.02 mol 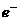 时,阳极质量减小0.64g
时,阳极质量减小0.64g
④a口产生的是氢气,b口产生的是氧气
26.(14分)X、Y、Z为原子序数由小到大排列的三种短周期元素。已知X、Y的氢化物分子具有相同的电子数;Y与Z同主族。XY2是非极性分子,其晶体可用作人工降雨。请回答:
(1)①Z的最高价氧化物对应的水化物W是重要的化工原料,W的化学式为 ;
②在101kPa时,3.2gZ的固体单质完全燃烧可放出29.7KJ的热量,写出能够表示该固体单质燃烧热的热化学方程式 ;
③工业上由ZY2合成ZY3时,结合工业实际,应选用的温度和压强是 (选择字母填空)。
A.400℃一500℃,0.1 Mpa B.400℃-500℃,1Mpa
C.500℃一600℃,10Mpa D.400℃-500℃,100Mpa
|
①写出X单质与W的浓溶液反应的化学方程式 ;
②11.2L ZY2(标准状况)在加热和催化剂作用下与足量的XY发生化学反应,反应中有2mol电子转移,则该反应的化学方程式为 ;
③Z与Fe可组成FeZ2的化合物,是工业制备W的重要原料,假定由FeZ2生成W的每一步原料利用率均为90.0%,请求出用含FeZ2 1.20 t的矿石制备浓度为80.0%的W溶液的质量。(要求写出详细计算过程,结果保留3位有效数字)
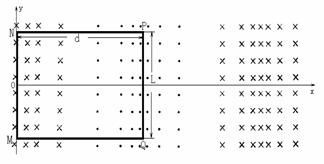
25.(22分)(16分)磁悬浮列车是一种高速运载工具。它具有两个重要系统:一是悬浮系统,利用磁力使车体在导轨上悬浮起来;另一是驱动系统,在沿轨道上安装的三相绕组中,通上三相交流电,产生随时间和空间做周期性变化的磁场,磁场与固连在车体下端的感应金属板相互作用,使车体获得牵引力。
设图中 平面代表轨道平面,
平面代表轨道平面,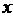 轴与轨道平行,现有一与轨道平面垂直的磁场正以速度
轴与轨道平行,现有一与轨道平面垂直的磁场正以速度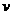 向
向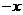 方向匀速运动,设在
方向匀速运动,设在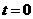 时,该磁场的磁感应强度B的大小随空间位置x的变化规律为
时,该磁场的磁感应强度B的大小随空间位置x的变化规律为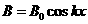 (式中B0、k为已知常量),且在y轴处,该磁场垂直
(式中B0、k为已知常量),且在y轴处,该磁场垂直 平面指向纸里。与轨道平面平行的一金属矩形框MNPQ处在该磁场中,已知该金属框的MN边与轨道垂直,长度为L,固定在y轴上,MQ边与轨道平行,长度为d=
平面指向纸里。与轨道平面平行的一金属矩形框MNPQ处在该磁场中,已知该金属框的MN边与轨道垂直,长度为L,固定在y轴上,MQ边与轨道平行,长度为d=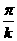 ,金属框的电阻为R,忽略金属框的电感的影响。求:
,金属框的电阻为R,忽略金属框的电感的影响。求:
(1) t=0时刻,金属框中的感应电流大小和方向;
(2) 金属框中感应电流瞬时值的表达式;
(3) 经过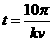 时间,金属框产生的热量;
时间,金属框产生的热量;
(4) 
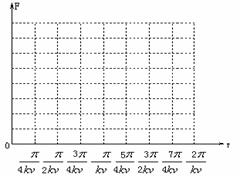 画出金属框受安培力F随时间变化的图象。
画出金属框受安培力F随时间变化的图象。
24.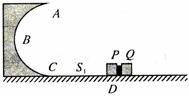 (18分)如图所示,ABC是竖直固定的半圆形光滑圆弧槽,底端与水平地面相切于C点,半径R=0.1m.P、Q是两个可视为质点的物体,
(18分)如图所示,ABC是竖直固定的半圆形光滑圆弧槽,底端与水平地面相切于C点,半径R=0.1m.P、Q是两个可视为质点的物体,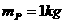 、
、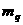 =5kg,其间放有一压缩弹簧,且P开始静止于D处.P、Q与水平地面的摩擦因素均为μ=0.5,某时刻弹簧将P、Q瞬间水平推开(不考虑推开过程中摩擦力的影响),有E=15J的弹性势能转化为P、Q的动能.(g取10m/s2)求:
=5kg,其间放有一压缩弹簧,且P开始静止于D处.P、Q与水平地面的摩擦因素均为μ=0.5,某时刻弹簧将P、Q瞬间水平推开(不考虑推开过程中摩擦力的影响),有E=15J的弹性势能转化为P、Q的动能.(g取10m/s2)求:
(1)P、Q被推开瞬间各自速度的大小?
(2)当CD间距离S1满足什么条件时,P物体可到达槽最高点A。
23. (14分) 如图,长为L=75cm的平底玻璃管,底部放置一可视为质点的小球,现让玻璃管从静止开始以a=16m/s2的加速度竖直向下运动,经过一段时间后小球运动到玻璃管口,此时让玻璃管立即停止运动,不计一切阻力(g取10m/s2,可能用到的数据:
(14分) 如图,长为L=75cm的平底玻璃管,底部放置一可视为质点的小球,现让玻璃管从静止开始以a=16m/s2的加速度竖直向下运动,经过一段时间后小球运动到玻璃管口,此时让玻璃管立即停止运动,不计一切阻力(g取10m/s2,可能用到的数据: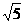 =2.24).求
=2.24).求
(1)小球到达玻璃管口时的速度;
(2)从玻璃管开始运动到小球再次回到玻璃管底所用的时间(结果保留两位有效数字).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com