
题目列表(包括答案和解析)
33. (8分)[化学-有机化学基础]
化合物A、B、C和D互为同分异构体,已知化合物A的结构简式为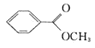 。实验表明:化合物A、B、C和D均是一取代芳香化合物,其中A、C和D的苯环侧链上只含一个官能团。4个化合物在碱性条件下可以进行如下反应,且A、B、C的第二步反应酸化后均生成两种有机物。
。实验表明:化合物A、B、C和D均是一取代芳香化合物,其中A、C和D的苯环侧链上只含一个官能团。4个化合物在碱性条件下可以进行如下反应,且A、B、C的第二步反应酸化后均生成两种有机物。
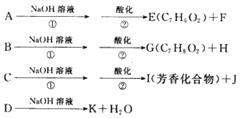
(1) 写出A、B、C和D共同的分子式。
(2) 写出B的结构简式。
(3) A在NaOH溶液中发生的反应类型为 ,H分子中含有官能团的名称为 。
(4) D在NaOH溶液中发生反应的化学方程式为 。
32. (8分)[化学-物质结构与性质]
下表为元素周期表前三周期的一部分。
|
|
|
||
|
X |
|
Z |
|
|
W |
Y |
|
R |
(1) X的氢化物的沸点与W的氢化物的沸点比较: > (填化学式),原因是 。
(2) W元素基态原子的价电子排布式为 ;在X元素形成的单质分子中,X元素原子之间存在着个 σ键和 个π键。
(3) 以上五种元素中,原子结构最稳定的元素是 (填元素符号)。
(4) 由以上某种元素与氢元素组成的三角锥形分子E和由以上某种元素组成的直线形分子G反应,生成两种直线形分子L和M(组成E、G、L、M分子的元素原子序数均小于10),反应如下图中所示,则下列判断错误的是 (填编号)。

A. 分子M的化学性质比同主族相邻元素单质的化学性质活泼
B. L是极性分子
C. E的中心原子杂化轨道类型为sp3杂化
D. G是活泼的非金属单质
31. (8分)[化学--化学与技术]
亚氯酸钠(NaClO2)是一种重要的含氯消毒剂,主要用于水的消毒以及砂糖、油脂的漂白与杀菌。以下是过氧化氢法生产亚氯酸钠的工艺流程图:
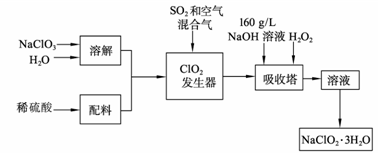
已知:
① NaClO2的溶解度随温度升高而增大,适当条件下可结晶析出NaClO2的结晶水合物;
② 纯ClO2易分解爆炸,一般用稀有气体或空气稀释到10%以下。
(1) 发生器中鼓入空气的作用可能是 ;鼓入SO2 的作用可能是 ;
(2) 吸收塔内发生反应的化学方程式为 ;
(3) 吸收塔中原料加入时,可能采取的一种工艺是 ;
(4) 从溶液中得到NaClO2·3H2O粗晶体的实验操作依次是 。
30. (16分)X、Y、Z、M均为短周期非金属元素,其原子序数按由小到大排列。X可分别与Y、Z、M组成10电子共价化合物。X、Z、M三种元素可形成离子化合物。
(1) 写出元素的名称:X. ,Z. 。
(2) 已知有反应2ZX3+3CuO=Z2+3Cu+3X2O,利用下图所示装置和必要的用品,可以进行制取ZX3并证明ZX3具有还原性的实验。
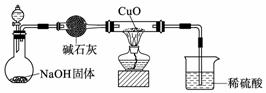
① 分夜漏斗中的溶液可能是 或 (填写名称)。
② 证明ZX3具有还原性的实验现象是 。
 ③ 上述装置有一不当之处,请在下面方框中画出改进部分的装置图。
③ 上述装置有一不当之处,请在下面方框中画出改进部分的装置图。
 (3) 某化学课外活动小组进行了一系列“带火星的木炭复燃”的实验,实验装置如下图。
(3) 某化学课外活动小组进行了一系列“带火星的木炭复燃”的实验,实验装置如下图。
某同学探究“使带火星木炭复燃时M2的体积分数的极限”。将M2和空气(假定空气中M2的体积分数为20%)按不同的体积比混合得100 mL气体A进行实验,实验记录如下:
|
编号 |
I |
II |
III |
IV |
V |
|
V(M2)/mL |
60 |
40 |
20 |
12 |
10 |
|
V(空气)/mL |
40 |
60 |
80 |
88 |
90 |
|
现象 |
木条复燃 |
木条复燃 |
木条复燃 |
木条有时燃烧,有时不燃烧 |
木条不复燃 |
回答问题:
① 使带火星木条复燃的M2的体积分数最小(第Ⅳ组数据)约为 。
② 用带火星木条检验集气瓶里是否集满M2,若木条复燃,能否认为集气瓶里的气体一定是纯净的M2?答: (填“能”或“否”)。
③ 若按照3∶2的比例混合M2和CO2气体,该混合气体能否使带火星的木条复燃
(填“能”“否”或“不一定”)。
(4) 物质的检验和分离,是化学实验的基本操作。
① X与Z元素可共同组成一种常见的阳离子,写出检验该离子的实验操作及现象。
实验操作: ;
现象: 。
② 下列混合物的分离和提纯方法:① 渗析② 蒸馏③ 过滤④ 分液,其中基本原理相近的是下列的 (填序号)。
A. ①和② B. ③和④ C. ①和③ D. ②和④
[选做部分]
共8个小题,考生从中选择2个物理题、1个化学题和1个生物题作答。
29. (13分)化学科学可以让人们在分子水平上了解疾病的原理,寻求有效的防治措施。
(1) NO在医学上因其在治疗心脏病方面的特殊作用而被称为“明星分子”。工业上可利用如下反应制备NO:
4NH3(g)+5O2(g)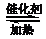 4NO(g)+6H2O(g)ΔH<0
4NO(g)+6H2O(g)ΔH<0
① 写出该反应的平衡常数表达式:K= 。
② 在一定体积的密闭容器中,为使该反应的反应速率增大,且平衡向正反应方向移动,下列措施中可采用的是 。
a. 增大压强b. 适当升高温度c. 增大O2的浓度d. 选择高效催化剂
(2) 痛风是关节炎反复发作及产生结石为特征的一类疾病,关节炎的原因归结于在关节滑液中形成了尿酸钠(NaUr)晶体,有关平衡如下:
Ⅰ. HUr(尿酸,aq) 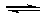 Ur-(尿酸根,aq)+H+(aq)
Ur-(尿酸根,aq)+H+(aq)
(37℃时,Ka=4.0×10-6mol·L-1)
Ⅱ. NaUr(s) 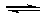 Ur-(aq)+Na+(aq)
Ur-(aq)+Na+(aq)
① 关节炎发作大都在脚趾和手指的关节处,这说明温度降低时,反应Ⅱ的Ksp(填“增大”、“减小”或“不变”)。生成尿酸钠晶体的反应是 (填“放热”或“吸热”)反应。
② 人体内关节滑液的pH (填“越大”、或“越小”),越易形成关节炎。
(3) 碳不完燃烧生成的CO可与人体血红蛋白结合而使人中毒。己知:
CO(g)+1/2O2(g)= CO2(g);ΔH=-283.0 kJ·mo1-1
H2(g)+12O2(g)= H2O(g);ΔH=-241.8 kJ·mo1-1
C(s)+12O2(g)= CO(g);ΔH=-110.5 kJ·mo1-1
若将12 g 碳先与水蒸气反应完全转化为水煤气(主要成分是CO、H2),然后水煤气再完全燃烧,整个过程放出kJ的热量。
28. (13分)近年来,我国储氢纳米碳管研究获重大进展,电弧法合成的碳纳米管,常伴有大量碳纳米颗粒生成。这种碳纳米颗粒可用氧化汽化法提纯。其反应的化学方程式为:
3C
+2K2Cr2O7 + 8H2SO4(稀) 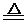 3CO2 ↑+ 2K2SO4+
2Cr2(SO4)3+ 8H2O
3CO2 ↑+ 2K2SO4+
2Cr2(SO4)3+ 8H2O
(1) 此反应中的氧化剂是 ,氧化产物是 。
(2) H2SO4在上述反应中表现出来的性质有 (填选项编号)。
A. 酸性 B. 氧化性 C. 吸水性 D. 脱水性
在下列四个标签中,保存K2Cr2O7的试剂瓶上最适合贴上的一个标签是 (填序号);
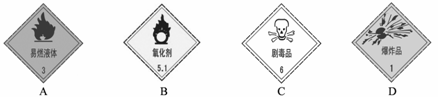
(3) 电解法处理含Cr2O72-离子的废水(pH=4-6)的一种方法是:往废水中加入适量NaCl,以铁为电极进行电解,同时鼓入空气,经过一段时间后,废水中的铬元素含量降到可排放标准。试写出电解过程中阳极的电极反应式 。试写出在酸性条件下阳极产物与Cr2O72-在溶液中反应的离子方程式 (已知Cr2O72-转化为Cr3+离子,方程式不必配平)。
(4) 实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是 (填序号)。
A. C(s)+H2O(g)===CO(g)+H2(g) ΔH>0
B. NaOH(aq)+HCl(aq)===Nacl(aq)+H2O(l)ΔH<0
C. 2H2(g)+O2(g)===2H2O(l)ΔH<0
以KOH溶液为电解质溶液,依据所选反应设计一个原电池,写出其负极的反应式:
。
27. (17分)金鱼是重要的观赏鱼,品种众多,可观赏的性状多种多样。请利用遗传学和生物进化知识回答下列问题。
(1) 实验证明,任何品种的金鱼都能与野生鲫鱼杂交,并产生可育后代。这说明金鱼与野生鲫鱼之间不存在 现象。众多金鱼品种的形成是长期的 结果。
(2) 研究表明,金鱼的性别由性染色体决定,属于XY型。金鱼培育专家培育的珍贵品种--“蓝剑”,其性染色体组成为XYY。该金鱼所以珍贵,其原因之一是“蓝剑”不能直接产生后代,最根本的原因是 ;“蓝剑”的产生可能是亲本中 个体在减数分裂第 次分裂时遗传物质分配异常所造成的。
(3) 基因Aa和Bb是位于非同源染色体上的两对基因。两只金鱼杂交,若子代中出现A:aa=3∶1,B :bb=1∶1,则亲本的基因型为 ;若子代中雌鱼全部表现为B控制的性状,雄鱼既有B控制性状又有表现为b控制性状,则亲本的基因型应为 。
(4) 若已知金鱼眼睛的性状甲和乙是一对相对性状,并且由位于X染色体上的一对等位基因控制。但实验室只有从自然界捕获的、有繁殖能力的甲性状雌、雄金鱼各一条和乙性状雌、雄金鱼各一条,某同学想通过一次杂交试验确定这对相对性状中的显性性状。
他应选择的亲本是 。
预测子代可能出现的性状,并作出相应的结论。
① 。
② 。
③ 。
26. (16分)人体内环境稳态是生命活动正常进行的必要条件。请回答下列有关内环境稳态及人体生命活动调节的有关问题:
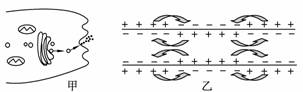
上图甲、乙可以表示同一细胞的不同部分,也可以表示不同细胞的不同部分。
(1) 如果甲和乙所表示的是同一细胞的不同部分,则该细胞一定是 细胞;若甲分泌的是维持人体水分平衡的重要物质,则该细胞是 细胞。
(2) 若甲和乙表示不同细胞的不同部分,并且甲释放的物质被乙接受并引起乙发生如图的变化,则甲释放的物质是 ,甲、乙共同构成的结构称为 。
(3) 若甲和乙表示不同细胞的不同部分,环境温度降低时,由于乙的作用导致甲的分泌活动加强,则甲表示的是 细胞或 细胞。
(4) 若甲的分泌物质可以与侵入人体的病原体特异性结合,发挥免疫效应,则甲细胞应是 ;当同种病原体第二次侵入时,甲细胞主要由 增殖分化形成。
25. (17分)如图所示,在直角坐标系的第Ⅱ象限和第Ⅳ象限中的直角三角形区域内,分布着磁感应强度均为B=5.0×10-2T的匀强磁场,方向分别垂直纸面向外和向里。质量为m=6.64×10-27kg、电荷量为q=+3.2×10-19C的α粒子(不计α粒子重力),由静止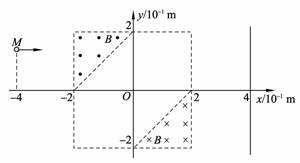 开始经加速电压为U=1 205 V的电场(图中未画出)加速后,从坐标点M(-4,2)处平行于x轴向右运动,并先后通过匀强磁场区域。
开始经加速电压为U=1 205 V的电场(图中未画出)加速后,从坐标点M(-4,2)处平行于x轴向右运动,并先后通过匀强磁场区域。
(1) 请你求出α粒子在磁场中的运动半径
(2) 请你在图中画出α粒子从直线x=-4到直线x=4之间的运动轨迹,并在图中标明轨迹与直线x=4交点的坐标
(3) 求出α粒子在两个磁场区域偏转所用的总时间
24.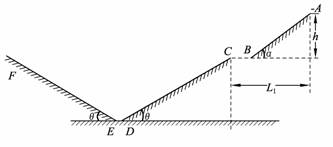 (16分)高台滑雪以其惊险刺激而闻名,运动员在空中的飞跃姿势具有很强的观赏性。某滑雪轨道的完整结构可以简化成如图所示的示意图。其中AB段是助滑雪道,倾角α=30°,BC段是水平起跳台,CD段是着陆雪道,AB段与BC段圆滑相连,DE段是一小段圆弧(其长度可忽略),在D、E两点分别与CD、EF相切,EF是减速雪道,倾角θ=37°。轨道各部分与滑雪板间的动摩擦因数均为μ=0.25,图中轨道最高点A处的起滑台距起跳台BC的竖直高度h=10 m。A点与C点的水平距离L1=20 m,C点与D点的距离为32.625
m。 运动员连同滑雪板的质量m=60 kg,滑雪运动员从A点由静止开始起滑,通过起跳台从C点水平飞出,在落到着陆雪道上时,运动员靠改变姿势进行缓冲使自己只保留沿着陆雪道的分速度而不弹起。除缓冲外运动员均可视为质点,设运动员在全过程中不使用雪杖助滑,忽略空气阻力的影响,取重力加速度g=10 m/s2,sin37°=0.6,cos37°=0.8。求:
(16分)高台滑雪以其惊险刺激而闻名,运动员在空中的飞跃姿势具有很强的观赏性。某滑雪轨道的完整结构可以简化成如图所示的示意图。其中AB段是助滑雪道,倾角α=30°,BC段是水平起跳台,CD段是着陆雪道,AB段与BC段圆滑相连,DE段是一小段圆弧(其长度可忽略),在D、E两点分别与CD、EF相切,EF是减速雪道,倾角θ=37°。轨道各部分与滑雪板间的动摩擦因数均为μ=0.25,图中轨道最高点A处的起滑台距起跳台BC的竖直高度h=10 m。A点与C点的水平距离L1=20 m,C点与D点的距离为32.625
m。 运动员连同滑雪板的质量m=60 kg,滑雪运动员从A点由静止开始起滑,通过起跳台从C点水平飞出,在落到着陆雪道上时,运动员靠改变姿势进行缓冲使自己只保留沿着陆雪道的分速度而不弹起。除缓冲外运动员均可视为质点,设运动员在全过程中不使用雪杖助滑,忽略空气阻力的影响,取重力加速度g=10 m/s2,sin37°=0.6,cos37°=0.8。求:
(1) 运动员在C点水平飞出时速度的大小
(2) 运动员在着陆雪道CD上的着陆位置与C点的距离
(3) 运动员滑过D点时的速度大小
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com