
题目列表(包括答案和解析)
25.(6分) A、B、X、Y均为中学阶段的常见物质,它们之间的转化关系如下图所示,
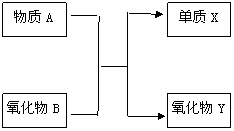 试写出符合下列条件的化学方程式:
试写出符合下列条件的化学方程式:
(1)若物质A为氧化物 ▲ ;
(2)若A为金属单质,B为非金属单质 ▲ ;
(3)若A和X均为非金属单质 ▲ 。
24.(8分)海水占地球总储水量的97.2%。若把海水淡化和化工生产结合起来,既可以解决淡水资源缺乏的问题,又可以充分利用海洋资源。
(1)海水中含有大量的氯化钠。请写出氯原子的原子结构示意图 ▲ ;
(2)目前国际上实用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸汽,蒸汽经过冷却而得高纯度淡水,由此可判断蒸馏法是 ▲ (填物理变化、化学变化);
(3)工业上利用电解饱和食盐水可制得重要化工产品,又称为“氯碱工业”。电解饱和食盐水的化学方程式为 ▲ ;
(4)近年来有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法,该方法的流程如下:
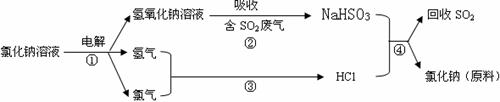
试写出④的化学反应方程式 ▲ 。
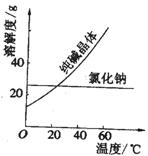
21.21.(5分)下图是一种用于显示事物异同点的信息处理方法。图1中两个圆分别代表碳酸钠和碳酸氢钠的有关信息,两圆重叠区域表它们的共同特点(相似点),重叠区域以外的部分表示它们独有的特征(不同点)。请你在图下的空格内填写适当内容。(每处只要求填一点)
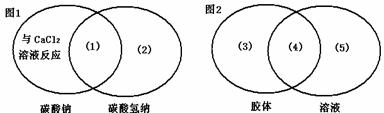
(1) ▲ ;(2) ▲ ;(3) ▲ ;(4) ▲ ;(5) ▲ 。
|
|

|
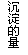
 (已知:2Na2O2+2H2O=4NaOH+O2↑)
(已知:2Na2O2+2H2O=4NaOH+O2↑)
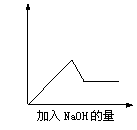
第③个实验中,生成白色沉淀的量与加入NaOH的量有右图
所示的相互关系。据此可知:
(1)在原溶液中一定不存在的离子有 ▲ ;
(2)为满足该溶液中一定存在的离子的要求,一般可溶解两种常见
 物质为(写化学式) ▲ 和 ▲ ;
物质为(写化学式) ▲ 和 ▲ ;
(3)写出第③个实验中发生反应的离子方程式 ▲ 。
20.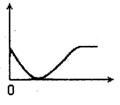 下列实验过程中产生的现象与右边坐标图形相符合的是
下列实验过程中产生的现象与右边坐标图形相符合的是
A.稀盐酸滴加到一定量NaHCO3,溶液中(横坐标是稀盐酸的体积,纵坐标为气体体积)
B.NaOH溶液滴入Ba(HCO3)2溶液中(横坐标是NaOH溶液的体积,纵坐标为沉淀质量)
C.稀硫酸滴加到Ba(OH)2溶液中(横坐标是稀硫酸的体积,纵坐标为溶液的导电能力)
D.稀盐酸滴加到AgNO3溶液中(横坐标是稀盐酸的体积,纵坐标为溶液的导电能力)
第II卷(非选择题,共60分)
19.类推是化学学习与研究中常用的方法,下列类推的结论正确的是
A.钠与氧气、水等反应时钠均作还原剂,则金属单质参与反应时金属单质均作还原剂
B.铁能从硫酸铜溶液中置换出铜,则钠也能从硫酸铜溶液中置换出铜
C.碳在少量氧气中燃烧生成CO、在过量氧气中燃烧生成CO2,则硫在少量氧气中燃烧生成SO2、在过量氧气中燃烧生成SO3
D.铝粉在氧气中燃烧生成Al2O3,则铁丝在氧气中燃烧生成Fe2O3
18.下列物质除杂(括号内物质为杂质)的方法及试剂都正确的是
|
|
物 质 |
方 法 |
试 剂 |
|
A |
CO2(SO2) |
洗气 |
氢氧化钠溶液 |
|
B |
AlCl3(MgCl2) |
过滤 |
过量氢氧化钠溶液 |
|
C |
乙醇(水) |
萃取、分液 |
汽油 |
|
D |
Cl2(HCl) |
洗气 |
饱和食盐水、浓硫酸 |
17.配制一定物质的量浓度的NaOH溶液时,造成所配溶液浓度偏高的原因是
A.所用NaOH已吸潮 B.定容前溶液未冷却
C.称量时砝码位置放错 D.向容量瓶加水时眼睛一直仰视液面
16.已知一些金属单质的发现与其金属活动性存在着某种必然的联系,你认为下无事件发生在铁器时代之前的是
①金属铝的冶炼 ②青铜器时代 ③金银的使用 ④戴维发现金属钠
⑤15世纪中国使用锌铸币
A.②③⑤ B.②③ C.①②③ D.①④⑤
15.下列有关工业生产的说法错误的是
A.高炉炼铁、生产普通硅酸盐水泥和普通玻璃都要用到的原料是石灰石
B.从海水中提取镁的过程中,不涉及到的反应类型是置换反应
C.从铝土矿中提取Al2O3的操作:用过量NaOH溶液溶解、过滤即可
D.接触法生产硫酸的主要设备有沸腾炉、接触室和吸收塔
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com