
题目列表(包括答案和解析)
27.国务院强调,调水必须坚持“三先三后”即“先节水后调水、先治污后通水、先环保后用水”的原则。在调水工程中,沿途污水的任意排放是造成水质恶化的最大隐患。检测某工厂废液中,含有大量的Mg2+、Al3+、Cu2+、Ag+。试分析回答下列问题:
(1)该废液中可能大量存在的一种阴离子是(填序号)·········· ( )
A.SO42― B.NO3― C.Cl― D.CO32―
(2)为检测废液中铝元素的含量,需要将其从废水样品中分离出来,可以用一种试剂即可以将上述污水中的其它离子与Al3+分开,所用的试剂可以是(填化学式)___________,铝元素发生变化的离子方程式是_____________________________。
(3)为了回收废液中的金属银,某同学设计了如右图的方案:
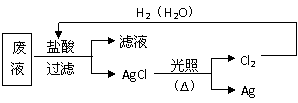
若依该方案获得108 g Ag,为保证不污染环境和Cl2的循环利用,理论上应提供标准状况下的氢气_____________ L。
26.实验室配制并保存硫酸亚铁溶液时,为防止Fe2+被氧化成Fe3+,可以加入的试剂是_____,原理是_____________________________(用离子方程式表示);在配制氯化铁溶液时,为防止Fe3+的水解,常加入的试剂是________________。用不含Fe3+的FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备_______色的Fe(OH)2沉淀,在操作上要注意防Fe(OH)2被氧化,Fe(OH)2在空气中被氧化最终将变为________色,反应的化学方程式是_____________________________________。工业上常在用铜板制作印刷线路时,用到氯化铁溶液来溶解铜,其反应的化学方程式是_________________________________。
25.铝粉与氧化铁(及其它一些金属氧化物)的混合物常称为铝热剂。由于该混合物发生反应时会放出大量的热,使得到的金属熔化,反应的化学方程式是________________________,常称该反应为__________反应。该反应实际上是体现了金属铝较强的_________(填“氧化”或“还原”)性,工业上利用该反应来进行野外焊接,或利用该反应来冶炼某些_________的金属。
24.红宝石和蓝宝石是含少量杂质的优质刚玉,是制作名贵首饰的材料,刚玉是较纯的氧化铝。其实,氧化铝晶体的结构较复杂,主要有两种晶体型态,一种属于α型,这种氧化铝很难与酸或碱反应,刚玉就属于这种;另一种属于γ型,通常的氧化铝主要是该型,这种氧化铝是一种_______性氧化物,可以与NaOH溶液反应,工业上常利用这一反应来除去铝表面的氧化膜。该反应的化学方程式是
_______________________________________,氧化铝的熔点很高,常用作_______________材料。
23.下表是元素周期表的一部分:
 族 族周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
|
一 |
a |
|
|
|
|
|
|
|
|
二 |
|
|
|
d |
e |
|
h |
|
|
三 |
b |
|
c |
|
f |
|
g |
|
根据a-h各元素的性质,选择相应的化学符号、化学式或化学方程式填空:(不得用a~h字母回答)
① 其中单质氧化性最强的是__________,金属性最强的是_____________。
② 最高价氧化物对应的水化物中,碱性最强的是___________、酸性最强的是____________。
③ 其中原子半径最大的元素是___________。
④ f、g和h的气态氢化物的稳定性由强到弱的顺序是____________________。
⑤ b和c两者的最高价氧化物对应的水化物间反应的离子方程式是
_____________________,C和e两者的最高价氧化物对应的水化物间反应的离子方程式 是______________________。
⑥ 写出a元素和g元素形成化合物的电子式__________________。
22.1-20号元素中(用元素符号、化学式填写)
(1) 与水反应最剧烈的金属元素是______
(2) 位于2周期ⅡA族的元素是______
(3) 有三个电子层,最外层上有5个电子的元素是______。
(4) 除稀有气体外,原子半径最大的元素为______
(5) 最高价氧化物对应的水化物酸性最强的是____________(化学式)
(6) 第三周期常见简单离子中, 离子半径最大的是__________(离子符号)
21.元素周期表中共有7个周期;其中1、2、3周期中包含的元素数目较少,叫做______周期;4、5、6周期中所含的元素数目较多,叫做______周期;第7周期叫做不完全周期。第4周期共有_________(填数字)种元素。
元素周期表中共有______(填数字)个族,其中有______(填数字)个主族,______(填数字)个副族,还有一个Ⅷ族一个0族。
20.往20ml 1mol/L的AlCl3溶液中滴加0.2mol/L的NaOH溶液,最后有1.17克沉淀生成,则加入NaOH溶液的体积是
A.125 mL B.275 mL
C.325 mL D.450 mL
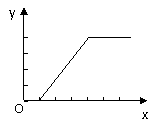
19.向1 mol/L甲溶液中逐滴滴入1 mol/L乙溶液,产生Al(OH)3沉淀的量(用y轴表示)与所加入乙溶液的体积(用x轴表示)的关系如下图所示,符合图中关系的甲、乙溶液是下列各组中的
|
|
甲 |
 乙 乙 |
|
A |
氯化铝溶液 |
氢氧化钠溶液 |
|
B |
盐酸溶液 |
偏铝酸钠溶液 |
|
C |
氢氧化钠溶液 |
氯化铝溶液 |
|
D |
偏铝酸钠溶液 |
盐酸溶液 |
18.某两种金属粉末的温合物20 g,投入足量的稀盐酸中,产生的氢气在标准状态下体积为11.2升,则该温合物可能是
A.Mg、Na B.Al、Mg
C.Fe、Cu D.Fe、Zn
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com