
题目列表(包括答案和解析)
22.(8分)有X、Y、Z三种元素。其中X原子的价电子构型为2s22p2,Y原子的L电子层中有三个未成对电子,且无空轨道;Z的+1价离子是一个质子。
试回答下列问题:
(1)ZXY分子中的三个原子除Z原子外均为8电子构型,写出该分子的结构式 ,根据电子云重叠方式的不同,分子里共价键的类型有 ;
(2)常温下,YZ3呈气态,但易被液化,且极易溶于水,其原因是 ;
(3)液态的YZ3是一种重要的溶剂,其性质与H2O相似,可以与活泼金属反应,写出Na与液态YZ3反应的化学方程式 。
21.(6分)今有A、B、C、D四种元素。其中A元素单质是一种红棕色液体,有刺鼻的臭味。B、C、D的原子电子层排布均不超过3个电子层。C 、D同主族,D原子核内的质子数正好等于C原子核内质子数的2倍。D原子的最内电子层上电子数是B原子核外电子数的2倍。四种元素的名称分别为:A 、B 、C 、D ,由上述某元素的单质与另两种元素形成的化合物反应生成两种酸的化学方程式是: 。
23.(10分)著名化学家侯德榜改革国外的纯碱生产工艺,发明的新生产流程可简要表示如下:
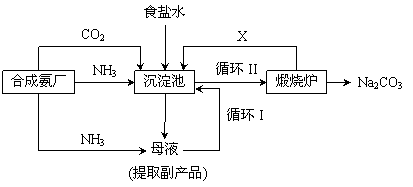
(1) 上述生产纯碱的方法称 ,副产品的一种用途为 ;
(2) 沉淀池中发生的化学反应方程式是 ;
(3) 写出上述流程中X物质的分子式 ;
(4) 此流程能使原料氯化钠的利用率达到90%以上,主要是因为设计了循环
(填上述流程中的编号);
(5)从沉淀池中分离出沉淀的操作是 ;
(6)为检验产品碳酸钠中是否含有氯化钠,可取少量试样溶于水后,再滴加 。
物质结构与性质(选修模块)(共24分)
22.(8分)用离子交换膜电解槽电解饱和食盐水制氯气,阴极产物是 ,阳极产物是 。反应的离子方程式是 。若去掉离子交换膜电解食盐水,可得到一种消毒液,其主要成分是 ,反应的化学方程式是 。
21.(6分) 下图为某饮用水厂从天然水制备纯净水(去离子水)的工艺流程示意图,请回答:
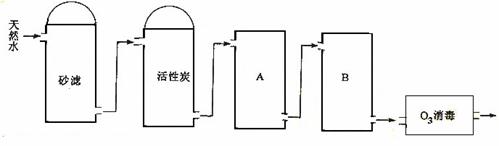
活性炭的作用是 ;
O3消毒的优点是 ;
A中所放物质的名称是 。
23.(10分)氮化硅是一种高温结构陶瓷材料,它的硬度大,熔点高,化学性质稳定,工业上曾普遍采用高纯硅与氮气在1300℃反应获得。
(1)根据其性质,试推测氮化硅陶瓷的用途有下列的 (填序号);
A.制有色玻璃 B.作刀具 C.制造陶瓷发动机
(2)写出氮化硅的化学式 ;
(3)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不跟其它无机酸反应。试推断该陶瓷被氢氟酸腐蚀的化学方程式 ;
(4)用SiC14和N2在H2气氛中加强热使其发生反应,可制取较高纯度的氮化硅,反应的化学方程式为 。
[化学与技术](选修模块,共24分)
22.(8分)人体中胃酸的主要成分是盐酸。胃酸可帮助消化食物,但胃酸过多会使人感到不适,服用适量的小苏打可使症状明显减轻。
(1)写出小苏打和盐酸反应的离子方程式: ;
(2)Mg(OH)2也是一种胃酸中和剂,写出Mg(OH)2中和胃酸的离子方程式: ;
(3)如果你是内科医生,给胃酸过多的胃溃疡病人(其症状之一是胃壁受损伤而变薄)开药方时,最好选用小苏打和氢氧化镁中的 ,理由是 。
21.(6分) 酸雨给人类带来种种危害,严重威胁着生态环境。结合所学的化学知识,回答下列问题:
酸雨给人类带来种种危害,严重威胁着生态环境。结合所学的化学知识,回答下列问题:
(1)称为酸雨的水溶液的pH范围是______ ___;
A. pH<7 B. pH<5.6 C. pH>5.6 D. pH<0
(2)下列气体过量排放,不会形成酸雨的是______;
A.二氧化碳 B.二氧化硫 C.二氧化氮 D.氯化氢
(3)请举出两例酸雨的危害 。
23.(10分)现有下列可逆反应:A(g)+B(g) xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
xC(g),在不同条件下生成物C在反应混合物中的质量分数(C%)和反应时间(t)的关系如下图:
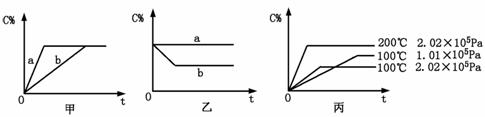
请根据图象回答下列问题:
(1)若甲图中两条曲线分别表示有催化剂和无催化剂的情况,则 曲线表示无催化剂时的情况(填字母,下同);
(2)若乙图表示反应达到平衡后分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入惰性气体后的情况,则 曲线表示恒温恒容的情况;
(3)根据丙图可以判断该可逆反应的正反应是 热反应(填“吸”或“放”);
(4)化学计量数x的值 (填取值范围);判断的依据是 。
化学与生活(选修模块)(共24分)
22.(8分)Ⅰ.(1)事实证明,原电池中发生的反应通常是放热反应。利用下列化学反应可以设计成原电池的是 ;
A.C(s)+H2O(g)=CO(g)+H2(g) △H>0
B.NaOH(aq)+HC1(aq)=NaC1(aq)+H2O(1) △H<0
C.2H2(g)+O2(g)=2H2O(1) △H<0
(2)以KOH溶液为电解质溶液,依据所选反应设计一个原电池,其负极反应式为 ;
Ⅱ.电解原理在化学工业中有着广泛的应用。如图所示电解池,其中a为CuSO4溶液,X和Y是两块惰性 电极板,则电解时的化学方程式为
;通电一段时间后如果转移了0.4mole-,若想使电解质溶液恰好恢复到电解前的浓度和pH,则需加入 g (填化学式)。
电极板,则电解时的化学方程式为
;通电一段时间后如果转移了0.4mole-,若想使电解质溶液恰好恢复到电解前的浓度和pH,则需加入 g (填化学式)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com