
题目列表(包括答案和解析)
1.下列说法正确的是
A.MgO、Al2O3的熔点很高,可作耐高温材料,工业上用热还原法冶炼对应的金属
B.氢氧化钠、碳酸氢钠、氢氧化铝都可用作抗酸药
C.甲醛的水溶液具有杀菌、防腐的作用,可用于海产品保鲜
D.糖类、油脂、蛋白质、维生素、无机盐和水是人体所需的六大营养素
22(1)环形玻璃搅拌棒;保温、隔热,减少实验过程中的热最损失
(2)偏小
(3)不相等; 因为酸、碱发生中和反应放出的热量与酸、碱的用量有关; 相等 中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量,它与酸、碱的用量无关
21.(1)活化能,反应热;(2)放热,<0;ww.k@s@5@ 高#考#资#源#网
20.(1)N2H4(l)+2H2O2(l)=N2(g)+4H2O (g); △H=-641.63 KJ/mol
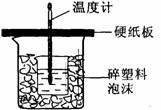
22.中和热是指酸跟碱发生中和反应生成lmol H2O所放出的热量。某学生想通过测定反应过程中所放出的热量来计算中和热。他将50mL0.5mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应。请回答下列问题:
(1) 从实验装置上看,图中尚缺少的一种玻璃用品是__________________,烧杯间填满碎塑料泡沫的作用是_________________________________。
(2) 大烧杯上如不盖硬纸板,则求得的中和热数值_________(填“偏大”、“偏小’、“无影响”)
(3) 实验中改用60 mL 0.50 mol/L的盐酸跟50mL 0.55 mol/L的NaOH溶液进行反应,与上
述实验相比,所放出的热量________(填“相等”或“不相等”),理由是__________________
___________________________________;所求中和热的数值会________(填“相等”或
“不相等”),理由是________________________________________________________。
ww.k@s@5@ 高#考#资#源#网
《化学反应与能量的变化》答案
21.
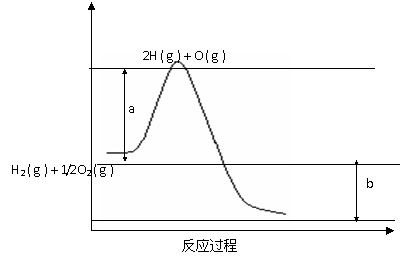 (8分)已知H2 ( g ) + 1/2O2 ( g ) = 2H2O ( g )
,反应过程中能量变化如下图:
(8分)已知H2 ( g ) + 1/2O2 ( g ) = 2H2O ( g )
,反应过程中能量变化如下图:
请回答下列问题:
(1)图中a,b分别代表什么意义?
a. ;
b. 。
(2)该反应是 反应(填“吸热”或“放热”),
△H (填“< 0”或“> 0”)。
20.火箭推进器中盛有强还原剂液态肼(N2H4)和强氧化剂液态双氧水。当它们混合反应时,即产生大量氮气和水蒸气,并放出大量的热。已知0.4mol液态肼与足量的液态双氧水反应,生成氮气和水蒸气,放出256.652KJ的热量。反应的热化学方程式为 __________________ 。
19. 在298K,1.01×105pa时,2molH2(g)燃烧生成水蒸气放出热量484KJ的热量,写出热化学反应方程式。
(1)_____________________________________________________
18.依据事实,写出下列的热化学反应方程式: 1molN2(g)与适量H2(g)起反应,生成NH3(g),放出92.2kj热量。
(1)_____________________________________________________
17. 250C (1.01×105)Pa下,4g CO在氧气中燃烧生成CO2,放出 9. 6kJ热量,写出CO燃烧的(1)反应方程式 (2)热化学反应方程式。
(1)_____________________________________________________
(2)_____________________________________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com