
题目列表(包括答案和解析)
7. 常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两项实验:(N2O4
常温常压下,在带有相同质量活塞的容积相等的甲、乙两容器里,分别充有二氧化氮和空气,现分别进行下列两项实验:(N2O4 2NO2 △H > 0)
2NO2 △H > 0)
|
|
(b)在活塞上都加2 kg的砝码
在以上两情况下,甲和乙容器的体积大小的比较,正确的是
A.(a)甲>乙,(b)甲>乙 B.(a)甲>乙,(b)甲=乙
C.(a)甲<乙,(b)甲>乙 D.(a)甲>乙,(b)甲<乙
6.下列关于判断过程的方向的说法正确的是
A.所有自发进行的化学反应都是放热反应 B.高温高压下可以使石墨转化为金刚石是自发的化学反应
C.由能量判据和熵判据组合而成的复合判据,将更适合于所有的过程
D.同一物质的固、液、气三种状态的熵值相同
5.下列叙述中,不能用平衡移动原理解释的是
A.红棕色的NO2,加压后颜色先变深后变浅
B.高压比常压有利于合成SO3的反应
C.由H2、I2(g)、HI(g)气体组成的平衡体系加压后颜色变深
D.黄绿色的氯水光照后颜色变浅
4. 在一个不传热的固定容积的密闭容器中发生可逆反应 mA(g) + nB(g) pC(g) + qD(g),当m、n、p、q为任意整数(不为零)时,不能说明达到平衡状态的标志是
A.体系的压强不再改变
在一个不传热的固定容积的密闭容器中发生可逆反应 mA(g) + nB(g) pC(g) + qD(g),当m、n、p、q为任意整数(不为零)时,不能说明达到平衡状态的标志是
A.体系的压强不再改变
B.各组分的浓度不再改变
C.反应速率υA : υB : υC : υD = m : n : p : q D.单位时间内m mol A断键发生反应,同时p mol C也断键发生反应
3.下列情况下,反应速率相同的是
A.等体积0.1 mol/L HCl和0.05 mol/L H2SO4分别与0.2 mol/L NaOH溶液反应
B.等质量锌粒和锌粉分别与等量1 mol/L HCl反应
C.等体积等浓度HCl和HNO3分别与等质量的Na2CO3粉末反应
D.等体积0.2 mol/L HCl和0.1 mol/L H2SO4与等量等表面积等品质石灰石反应
2.用3g块状大理石与30mL3mol/L盐酸反应制取CO2气体,若要增大反应速率,可采取的措施是: ①再加入30mL3mol/L盐酸 ②改用30mL6mol/L盐酸 ③改用3g粉末状大理石 ④适当升高温度
A.①②④ B.②③④
C.①③④ D.①②③
1.下列说法中有明显错误的是
A.对有气体参加的化学反应,增大压强体系体积减小,可使单位体积内活化
分子数增加,因而反应速率增大
B.升高温度,一般可使活化分子的百分数增大,因而反应速率增大
C.活化分子之间发生的碰撞一定为有效碰撞
D.加入适宜的催化剂,可使活化分子的百分数大大增加,从而成千上万倍地
增大化学反应的速率
31.(6分) 0.2mol有机物和0.4molO2在密闭容器中恰好完全反应,产物为CO2、CO、H2O(气),产物经过浓H2SO4后,浓H2SO4质量增加10.8克,再通过灼热的氧化铜充分反应后,氧化铜质量减轻3.2克,最后气体再通过碱石灰被完全吸收,质量增加17.6克。试通过计算确定该有机物的分子式。
30.(4分)某含氧有机化合物,它的相对分子质量为88.0,含C的质量分数为68.2%,含H的质量分数为13.6%,经红外光谱测定含有一个羟基,核磁共振氢谱显示该分子中有3个甲基。请写出其结构简式
28.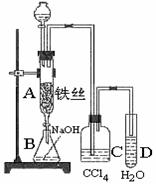 (12分)某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(12分)某化学课外小组用右图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A(A下端活塞关闭)中。
(1)写出A中生成溴苯的化学反应方程式:
(2)观察到A中的现象是 。
(3)实验结束时,打开A下端的活塞,让反应液流入B中,充分振荡,目的是 。
(4)C中盛放CCl4的作用是 。
(5)能证明苯和液溴发生的是取代反应,而不是加成反应,可向试管D中加入AgNO3溶液,若产生淡黄色沉淀,则能证明。另一种验证的方法是向试管D中加入 ,现象是 。
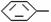
29(4分) .烷基取代苯 R可以被KMnO4的酸性溶液氧化生成
R可以被KMnO4的酸性溶液氧化生成 COOH,但若烷基R中直接与苯环连接的碳原子上没有C一H键,则不容易被氧化得到
COOH,但若烷基R中直接与苯环连接的碳原子上没有C一H键,则不容易被氧化得到
 COOH。现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成
COOH。现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成
为 COOH的异构体共有7种,其中的3种是
COOH的异构体共有7种,其中的3种是 CH2CH2CH2CH2CH3,
CH2CH2CH2CH2CH3,
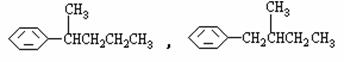
请写出其他4种的结构简式:___________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com