
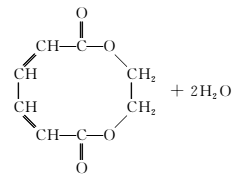
3.已知:—CHO+(C6H5)3P===CH—R―→—CH===CH—R+(C6H5)3P===O,R代表原子或原子团。W是一种有机合成中间体,结构简式为:
HOOC—CH===CH—CH===CH—COOH,其合成方法如图所示:
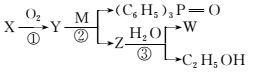
其中,M、X、Y、Z分别代表一种有机物,合成过程中的其它产物和反应条件已略去。X与W在一定条件下反应可以生成酯N,N的相对分子质量为168。
请回答下列问题:
(1)W能发生反应的类型有________。(填写字母编号)
A.取代反应 B.水解反应
C.氧化反应 D.加成反应
(2)已知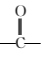 为平面结构,则W分子中最多有________个原子在同一平面内。
为平面结构,则W分子中最多有________个原子在同一平面内。
(3)写出X与W在一定条件下反应生成N的化学方程式:
________________________________________________________________________。
(4)写出含有3个碳原子且不含甲基的X的同系物的结构简式:________________________________________________________________________。
(5)写出第②步反应的化学方程式:________________________________________________________________________
________________________________________________________________________。
解析:采用逆推法,由Z发生水解生成W与C2H5OH的逆反应——酯化反应,可得Z的结构简式为
H5C2OOC—CH===CH—CH===CH—COOC2H5,根据题目所给信息可以判断Y为OHC—CHO,X为HOCH2—CH2OH,再根据X与W在一定条件下反应可以生成相对分子质量为168的酯N,验证所判断的X为HOCH2—CH2OH正确。(1)W中含有碳碳双键和羧基两种官能团,可以发生取代反应、氧化反应、加成反应,不能发生水解反应。(2)由题中信息可知与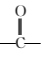 直接相连的原子在同一平面内,又知与
直接相连的原子在同一平面内,又知与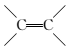 直接相连的原子在同一平面内,而且碳碳单键可以旋转,因此W分子中所有原子有可能都处在同一平面内,即最多有16个原子在同一平面内。(3)X中含有2个羟基,W中含有2个羧基,1分子X与1分子W可以发生酯化反应消去2分子H2O,而生成环状酯N。(4)丙二醇有2种同分异构体,其中HOCH2CH2CH2OH符合题意。
直接相连的原子在同一平面内,而且碳碳单键可以旋转,因此W分子中所有原子有可能都处在同一平面内,即最多有16个原子在同一平面内。(3)X中含有2个羟基,W中含有2个羧基,1分子X与1分子W可以发生酯化反应消去2分子H2O,而生成环状酯N。(4)丙二醇有2种同分异构体,其中HOCH2CH2CH2OH符合题意。
答案:(1)A、C、D (2)16
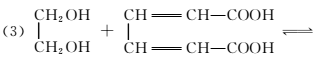
 (4)HOCH2CH2CH2OH(5)OHC—CHO+2(C6H5)3P===CHCOOC2H5―→
(4)HOCH2CH2CH2OH(5)OHC—CHO+2(C6H5)3P===CHCOOC2H5―→
2(C6H5)3P===O+H5C2OOCCH===CH—CH===CHCOOC2H5
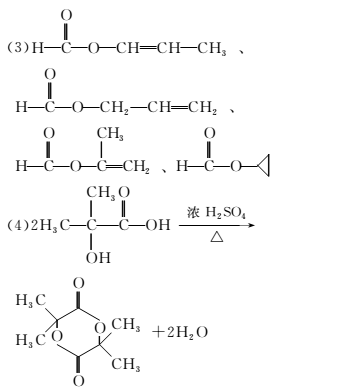
2.化合物X是一种环境激素,存在如图转化关系:
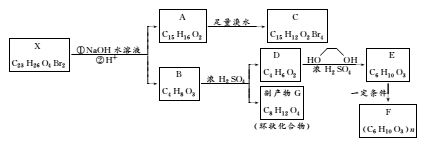
化合物A能与FeCl3溶液发生显色反应,分子中含有两个化学环境完全相同的甲基,其苯环上的一硝基取代物只有两种。核磁共振氢谱显示化合物G的所有氢原子化学环境相同。F是一种可用于制备隐形眼镜的高聚物。
根据以上信息回答下列问题:
(1)下列叙述正确的是________。
a.化合物A分子中含有联苯结构单元
b.化合物A可以和NaHCO3溶液反应,放出CO2气体
c.X与NaOH溶液反应,理论上1 mol X最多消耗6 mol NaOH
d.化合物D能与Br2发生加成反应
(2)化合物C的结构简式是__________,A→C的反应类型是________。
(3)写出同时满足下列条件的D的所有同分异构体的结构简式(不考虑立体异构)________________________________________________________________________。
a.属于酯类 b.能发生银镜反应
(4)写出B→G反应的化学方程式________________________________________________________________________
________________________________________________________________________。
(5)写出E→F反应的化学方程式________________________________________________________________________
________________________________________________________________________。
解析:比较A与C的分子式可发现C比A多了4个Br,少了4个H,说明发生了取代反应,可初步推断在A的结构中含有2个酚的结构单元,且其对位可能被占据;再分析A、B与X之间的关系,可推测X中具有酯的结构,是A中的2个羟基与B中的羧基脱水形成的酯,而X中的Br原子水解得到的羟基会在B分子中,即B中既含有羧基,又含有羟基,所以B在浓硫酸存在的条件下通过分子内消去脱水可得主要产物D,通过分子间酯化脱水得副产物G,D中含有碳碳双键,G中含有环酯结构;D与HOCH2CH2OH发生酯化反应,得到含有双键结构的酯E,酯E则能通过加聚反应得到高分子化合物F。经以上分析可得
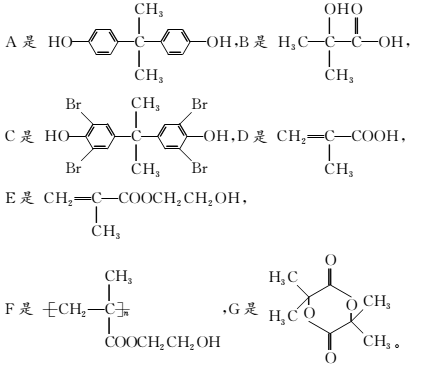
(1)分析化合物A、D、X的结构简式可知,a、b项错误;X中有两个酯基结构,且水解后得到酚类物质,可以消耗4 mol NaOH,另外2个溴原子水解也可消耗2 mol NaOH,故1 mol X最多消耗6 mol NaOH,c项正确;化合物D中含有碳碳双键,可与Br2发生加成反应,d项正确。(2)A转变为C的反应是取代反应。(3)有酯基结构且具有醛基的物质应该是甲酸酯,因此可得D的同分异构体有:
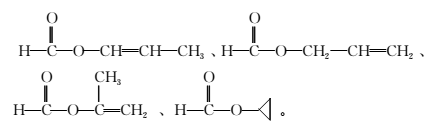
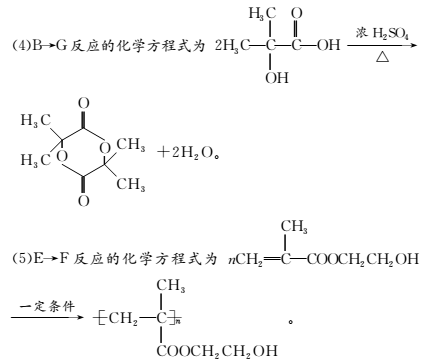
答案:(1)c、d
(2) 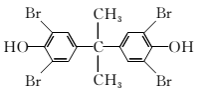 取代反应
取代反应
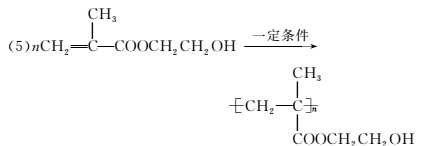
1.科学家对人造血液和人造器官的研制及应用已取得了很大的进步。下列物质就可以作为人工心脏、人工血管等人造器官高分子生物材料:
?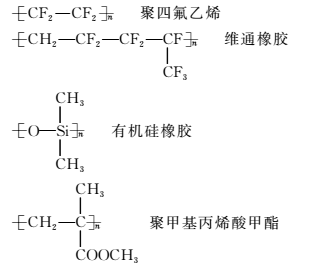
下列关于上述高分子生物材料的说法中正确的是( )
A.用于合成维通橡胶的单体是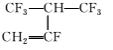
B.用于合成有机硅橡胶的单体是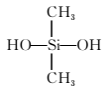
C.聚四氟乙烯、有机硅橡胶均可看做加聚反应的产物
D.有机硅橡胶、聚甲基丙烯酸甲酯均可通过缩聚反应制得
解析:选B 合成维通橡胶的单体是CH2===CF2和CF2===CF—CF3,聚甲基丙烯酸甲酯是由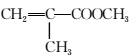 经加聚反应制得的;有机硅橡胶是由
经加聚反应制得的;有机硅橡胶是由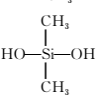 经缩聚反应制得的。
经缩聚反应制得的。
11.环己烯常用于有机合成。现通过图示流程,以环己烯为原料合成环醚、聚酯、橡胶,其中F可以作内燃机的抗冻剂,J分子中无饱和碳原子。已知:
R1—CH===CH—R2O3,Zn/H2O R1—CHO+R2—CHO
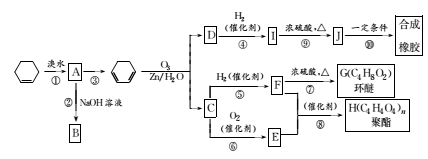
(1)③的反应条件是____________。
(2)H的名称是________________。
(3)有机物B和I的关系为________(填序号)。
A.同系物 B.同分异构体
C.都属于醇类 D.都属于烃
(4)①~⑦中属于取代反应的有:________________________________________________________________________。
(5)写出反应⑩的化学方程式:
________________________________________________________________________。
(6)写出两种D的属于酯类的链状同分异构体的结构简式:________________________________________________________________________。
解析:根据题中信息结合已学知识可知流程图中的各步反
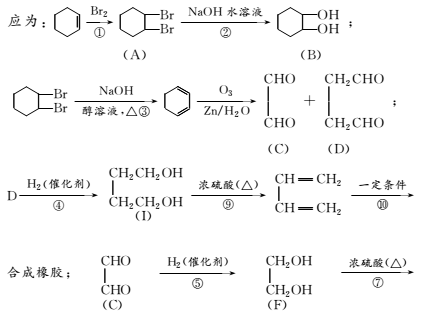
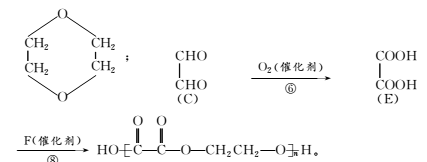
答案:(1)NaOH醇溶液、加热 (2)聚乙二酸乙二酯 (3)C (4)②、⑦ (5)nCH2===CH—CH===CH2一定条件?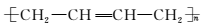 ?
?
(6)CH2===CHCOOCH3、HCOOCH2CH===CH2(其他合理答案也可)

9.(2014·宁波质检)奶油中有一种只含C、H、O的化合物A。A可用作香料,其相对分子质量为88,分子中C、H、O原子个数比为2∶4∶1。
已知:①ROH+HBr(氢溴酸)△RBr+H2O;
②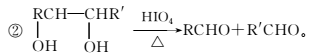
A中含有碳氧双键,与A相关的反应如下:
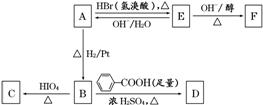
(1)A的分子式为______________。
(2)写出A→E、E→F的反应类型:A→E_________________________________________、
E→F________________。
(3)写出A、C、F的结构简式:A__________________________________________,
C________________,F________________。
(4)写出B→D反应的化学方程式:________________________________________________________________________
________________________________________________________________________。
(5)在空气中长时间搅拌奶油,A可转化为相对分子质量为86的化合物G,G的一氯代物只有一种,写出G的结构简式:______________________________。A→G的反应类型为________。
解析:由题中给出的M(A)=88,N(C)∶N(H)∶N(O)=2∶4∶1,可求得A的分子式为C4H8O2。因A中含碳氧双键且能与HBr取代,故A可能为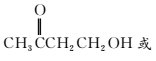
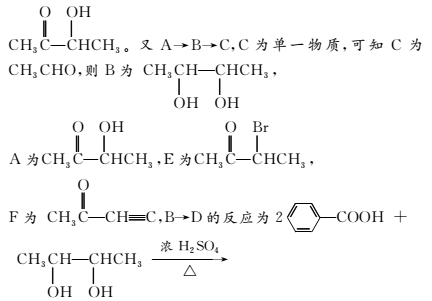
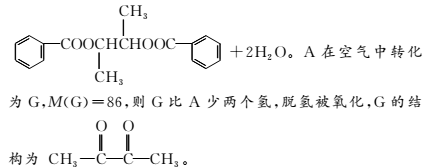
答案:(1)C4H8O2 (2)取代反应 消去反应
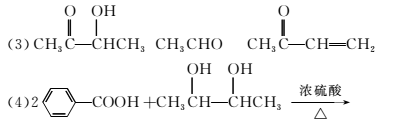
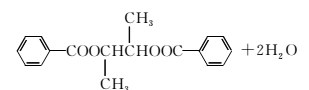
(5) 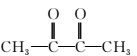 氧化反应
氧化反应
5.已知废旧干电池中的填充物主要有MnO2、ZnCl2、NH4Cl、Mn2O3、ZnO、FeO、炭黑、淀粉糊及汞的化合物等。某实验小组的同学拟回收废旧电池中的成分,主要操作流程如图:
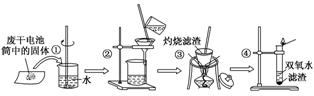
试回答下列问题。
(1)步骤①用玻璃棒搅拌的目的是________________________________________________________________________;
步骤②过滤后,滤液中的主要溶质有____________(填化学式);步骤③中灼烧的目的是________________________________________________________________________。
(2)经过步骤③得到的是粗制二氧化锰,要得到精制的二氧化锰还需将粗制二氧化锰用稀硝酸洗涤和蒸馏水洗涤,稀硝酸的作用是___________________________________。
(3)写出步骤④中发生反应的化学方程式:_________________________;
经过步骤②得到的固体干燥后,用氯酸钾与之混合加热的实验________(填“能”或“不能”)代替实验④。
(4)已知NH4Cl和ZnCl2的溶解度(g/100 g水)如表所示:
|
温度(℃) |
20 |
30 |
40 |
60 |
80 |
|
NH4Cl |
37.2 |
31.4 |
45.8 |
65.6 |
77.3 |
|
ZnCl2 |
396 |
437 |
452 |
541 |
614 |
从滤液中分离NH4Cl和ZnCl2的方法是_________________________________。
(5)从有害物质必须特殊处理的角度考虑,上述设计不合理的地方是________________________________________________________________________。
解析:(1)溶解时用玻璃棒搅拌的主要目的是加速其中的电解质溶解于水;废干电池中的氯化铵和氯化锌可溶于水;灼烧的目的是除去滤渣中的炭黑和淀粉糊等有机物。(2)Mn2O3及其中的其他金属氧化物能溶于稀硝酸,MnO2不溶于稀HNO3从而分离。(3)二氧化锰能催化过氧化氢分解放出氧气,从而间接检验二氧化锰;直接用含有机物的不纯二氧化锰与氯酸钾作用会引起爆炸。(4)由溶解度数据知,两者溶解度相差很大,先蒸发溶剂然后冷却结晶就可得较纯净的氯化铵晶体。
答案:(1)促进废干电池筒中的可溶性物质溶解
ZnCl2、NH4Cl 除去其中的炭黑和有机物
(2)除去其中的低价锰的氧化物和其他金属化合物
(3)2H2O22H2O+O2↑ 不能 (4)结晶(重结晶)
(5)没有回收有害物质汞,在实验过程中会产生汞蒸气污染
4.实验室需要纯净的NaCl溶液,但现有的NaCl晶体混有少量Na2SO4和(NH4)2CO3,请设计实验除去杂质,并回答下列问题:
(1)除去(NH4)2CO3用直接加热好还是加强碱后再加热好?
你认为____________,其理由是_________________________________________
______________________________;
判断(NH4)2CO3是否除尽的方法是_____________________________________。
(2)除去SO的方法是________________________;
判断SO是否除尽的方法是_______________________________________。
解析:比较NaCl和(NH4)2CO3的性质差异结合除杂的基本原则,不难得出直接加热好。判断(NH4)2CO3是否被除尽时,要注意的是只能用盐酸,否则会引入杂质。除去SO是使用过量的BaCl2溶液,接着又要用过量的Na2CO3溶液来除去过量的BaCl2(二者不能颠倒),最后用适量的盐酸除去过量的Na2CO3。
答案:(1)直接加热好 直接加热操作简单节省试剂,且不引入新的杂质 将残留物溶于水后加盐酸,看是否有气泡产生
(2)先加入过量BaCl2溶液,再加入过量Na2CO3溶液,过滤后,滤液中加入适量的盐酸 取加入BaCl2溶液后的上层清液,再滴入少量BaCl2溶液,看是否有白色沉淀生成
3.下列实验过程中出现异常情况,其可能原因分析错误的是( )
|
选项 |
异常情况 |
可能原因分析 |
|
A |
蒸发结晶:蒸发皿破裂 |
将溶液蒸干或酒精灯灯芯碰到热的蒸发皿底部 |
|
B |
分液:分液漏斗中的液体难以滴下 |
没有打开分液漏斗活塞,或玻璃塞上凹槽与漏斗口侧面的小孔没有对齐 |
|
C |
萃取:液体静置不分层 |
加入萃取剂的量较多 |
|
D |
检验Fe2+:加入KSCN溶液,溶液呈红色 |
Fe2+已部分被氧化成Fe3+ |
解析:选C 液体静置不分层一定是萃取剂选得不对,不是萃取剂量多量少的问题,C错误。
2.能鉴别MgI2、AgNO3、Na2CO3、NaAlO2四种溶液的试剂是( )
A.HNO3 B.KOH C.BaCl2 D.NaClO
解析:选A 本题考查物质的鉴别。HNO3氧化I-生成棕色的碘,与Na2CO3产生无色的CO2气体,与NaAlO2反应先生成白色沉淀然后溶解,现象均不同。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com