
7.(5分)有关诚信食品的调查:某些不法商贩,为牟取暴利,常在味精中掺入大量食盐,以次充好,欺骗顾客。我们综合实践活动小组进行“诚信食品”研究,借助大学化学实验室,运用所学知识,探究标签所列成分含量与实际是否相符。我随机取出某种“骏马味精”(成分说明见下图),准确称取3 g溶于水,加入足量AgNO3溶液,再加入稀HNO3少许(目的是防止杂质干扰)。经过滤、洗涤、干燥得白色沉淀AgCl l.435 g,试通过计算回答,该商标是否与实际相符。
|
骏马味精 配料: 谷氨酸钠(C5H7NO4Na2)80% 氯化钠(NaCl)<20% 净重:400g |
6.(7分)甲同学为了探究铝、铁和铜三种金属的活动性,他用铜丝、铁丝、铝丝和稀盐酸四种试剂,设计了以下只用一支试管,取一次盐酸的探究方案。
⑴请你帮助甲同学完善下表中的探究方案
|
实验步骤 |
观察到的现象 |
|
①在试管中取少量盐酸,插入铁丝,充分作用 |
________________ |
|
②在①所得溶液中,插入________,充分作用 |
无明显现象 |
|
③在②所得溶液中,插入________,充分作用 |
________________ |
结论:金属活动性Al>Fe>Cu
将铝丝插入溶液前应进行的操作是_________________________________________。
⑵乙同学看到甲同学的方案后,认为只要再补充一个实验,还能得出活动性Al>Fe>H>Cu的结论,乙同学要补充的实验是____________。
⑶丙同学认为要得到活动性Al>Fe>H>Cu的结论,不必补做实验,只需将甲同学方案中插入金属的顺序调整即可,调整后的金属插入顺序为____________________。
5.(5分)小明在学习金属活动性顺序时,对课本上“活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”这句话产生了好奇。为什么用“一般”这个词呢?难道还有例外吗?
[查阅资料]Na性质活泼,常温下,与氧气反应,也可以与水反应放出氢气。
[实验与分析]①在实验室中,金属钠保存在煤油中;②用镊子从煤油中取出金属钠,放在滤纸上,用小刀切下一小块,投人蒸馏水中,发现钠块立刻熔化成银白色小球,在水面上到处游动,滴入酚酞试液后溶液变成红色;③往硫酸铜溶液中,投入一小块钠,又出现蓝色沉淀,但没有红色物质析出。
⑴金属钠保存在煤油中的原因_________________________。
⑵从实验②中,你能得出哪些信息?(任写二条)。 、
。
⑶写出钠与硫酸铜溶液反应的化学方程式________________________________、
。
[结论]活动性较强的金属不一定将位于其后面的金属从它们的盐溶液中置换出来。
4.(4分)A、B、C、D是常见的化合物,A中含有钾元素。它们之间反应关系如下:
①2A+B=C+2H2O ②C+D=BaSO4↓+2A ③D+CuSO4=BaSO4↓+Cu(OH)2↓
根据以上信息,推断A、B两物质化学式:
A: B: 写出反应②的化学方程式: 。
3.(3分)人体所需的元素从食物中摄取不足时,可通过食品添加剂和保健药剂以补充。如制成补钙、补锌的保健药剂或制成加碘食盐等,来增加对这些元素的摄入量。
⑴氟是人体必需的一种微量元素,在牙釉质表面有一层坚硬的氟磷灰石,它的化学式为 Ca5(PO4)3F,在氟磷灰石中氟元素的化合价是 价。
⑵为了提高补钙效果,服用补钙剂时常需配合服用维生素D,据此可推知维生素D的功能是_____________。维生素D属于六大类营养素中的_____________。
2.(3分)苯甲酸是一种食品防腐剂,它是一种片状晶体,在水中的溶解度如下表:
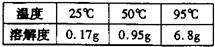
某同学为了提纯某一苯甲酸样品(其中含泥沙等难溶于水的杂质),进行了如下实验:
⑴取样品约1g放入烧杯中,加入50mL蒸馏水充分搅拌,发现样品几乎没溶解,原因是 。
⑵将烧杯放在石棉网上加热,将样品充分溶解后,在加入少量蒸馏水,然后趁热过滤。趁热过滤的目的是 。
⑶将所得滤液 ,使苯甲酸以晶体形式析出,然后过滤得到较纯净的苯甲酸晶体。
1.(3分)我国制碱工业的先驱侯德榜发明了侯氏制碱法,为我国制碱工业的发展做出了极大的贡献。纯碱(化学式为Na2CO3)是常见的工业用碱,也是许多化工产品的生产原料,在生活和生产中得到广泛应用。
⑴纯碱不是碱,在化学物质分类中属于________类物质;
⑵石灰石、大理石的主要成分是碳酸钙,在组成上与纯碱具有相同的组成部分,因而,它们都能与盐酸反应产生(填具体物质)__________气体;
⑶纯碱溶液与石灰水反应可制得少量NaOH溶液,在反应基本类型中,该反应属于_____________反应。
33.(7分)我国化工专家侯德榜的“侯氏制碱法”为世界制碱工业做出了突出的贡献。工业上用侯氏制碱法制得的纯碱中含有一定量的氯化钠杂质。现称取只含氯化钠杂质的纯碱样品11g,全部溶解在50g水中,当加入稀盐酸64.4g时,恰好完全反应,所得溶液的质量为121g。试求:
(1)该纯碱样品的纯度(计算结果精确到0.1%)。
(2)所得溶液中溶质的质量分数。
32.(3分)“禽流感”是一种由病毒引起的传染病,从禽类发病到人类染病引起了全世界的关注。预防这类病毒的方法是消毒,其中NaOH溶液因消毒效果好且廉价易得被广泛使用。某工业烧碱中氢氧化钠的质量分数为80%,一养殖户需配制2000g2%的氢氧化钠溶液对禽舍进行杀菌消毒,需这种工业烧碱_______g。
31.(8分)纯碱(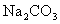 )产品中常含有少量氯化钠。某厂生产的纯碱包装袋上标有“
)产品中常含有少量氯化钠。某厂生产的纯碱包装袋上标有“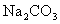 含量≥95%”字样。为判断该产品中
含量≥95%”字样。为判断该产品中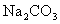 的含量是否达到要求,称取5.0g样品进行检验,可供选取的装置如下图。其中,丙装置中装足量浓氢氧化钠溶液,丁装置中装浓硫酸,戊装置中装水。(提示:浓硫酸具有吸水性,不挥发,不与二氧化碳反应,碳酸钠受热不分解。)
的含量是否达到要求,称取5.0g样品进行检验,可供选取的装置如下图。其中,丙装置中装足量浓氢氧化钠溶液,丁装置中装浓硫酸,戊装置中装水。(提示:浓硫酸具有吸水性,不挥发,不与二氧化碳反应,碳酸钠受热不分解。)
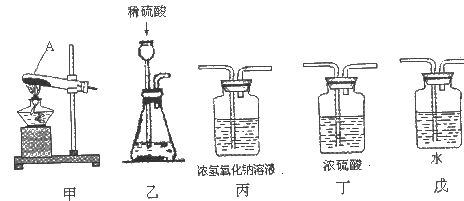
(1)写出上图仪器A的一种常见用途___________。
(2)你选择的实验装置从左到右组装排列为(填编号)___________。请说出你选择或排列装置的一点理由_________。
(3)假设每步都反应完全,生成的二氧化碳全部被吸收,不考虑空气中二氧化碳的影响。较准确地计算“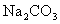 含量≥95%”是否真实,该实验除称取样品质量外,还要用天平量得到的实验数据是
_________。
含量≥95%”是否真实,该实验除称取样品质量外,还要用天平量得到的实验数据是
_________。
(4)若乙装置中加入浓盐酸(有挥发性),对测量结果会产生影响。原因是浓盐酸挥发出的氯化氢气体__________。
(5)若实验装置连接正确,实验过程中看到丙装置出现的气泡比丁少得多,一种可能的原_____________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com