
31、(4分)实验室有一瓶未开封的浓盐酸,部分标签如右图所
示。这瓶浓盐酸中溶液的质量为 g.若用这瓶浓盐
酸来配制200g溶质质量分数为10%的稀盐酸,需量取浓盐酸
的体积是 mL,水的体积是 mL。
28.(7分)小明参观某养鱼池时,好奇的发现农民向养鱼池中撒一种叫过氧化钙的淡黄色固体,用来增加鱼池中的含氧量。小明刚学完氧气的实验室制法,于是他想可否用过氧化钙来制取氧气。
[提出问题]过氧化钙可否用于制取氧气?
[查阅资料]部分内容如下:过氧化钙(CaO2)室温下稳定,在300℃时分解生成氧气,可作增氧剂、杀菌剂等。
[猜想与验证]
⑴小明依据 ,提出猜想Ⅰ。
猜想Ⅰ:加热过氧化钙可制取氧气。
|
实验装置 |
实验主要过程 |
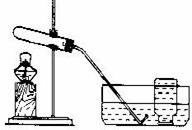 |
①检查装置气密性。操作如下:先将导管伸入液面下,用手紧握试管,观察到
,松开手后,有液体进入导管。 ②加入过氧化钙,加热,导管口有大量气泡昌出。 ③收集满一瓶气体。 ④停止加热。熄灭酒精灯前,应 。 ⑤检验气体,方法是 。 |
实验结论:加热过氧化钙可制取氧气。
⑵分析与反思:
①虽然没有快速收集到大量氧气,由此实验现象,小明认为农民用过氧化钙作增氧剂的主要原因是 。
②小明希望对此实验进行改进,使该反应加快,你能帮他提出建议吗?
你的合理建议是 。
以上建议是否可行,还需进一步通过实验验证。
27.(8分)下表列出了空气、氧气、二氧化碳、氨气在标准状况下的密度和溶解性。
|
物质 |
空气 |
氧气 |
二氧化碳 |
氨气 |
|
密度(g/L) |
1.293 |
1.429 |
1.977 |
0.771 |
|
溶解性 |
/ |
不易溶 |
 能溶 能溶 |
极易溶 |
已知实验室可用下列反应制取氨气:2NH4C1(固)+Ca(OH)2(固) CaCl2+2NH3↑+2H2O。
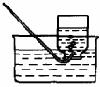
⑴根据上述信息,选择实验室制取和收集氧气、氨气的装置,请在相关空格处√。
|
|
 |
 |
 |
 |
 |
|
氧气 |
|
|
|
|
|
|
氨气 |
|
|
|
|
|
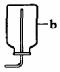
⑵写出图中有标号仪器的名称:a ;b 。
26. (6分)用双氧水和二氧化锰制氧气的反应方程式为:2H2O2 2H2O + O2 ↑。某同学做了该实验后,展开了下列思考与探究:
(6分)用双氧水和二氧化锰制氧气的反应方程式为:2H2O2 2H2O + O2 ↑。某同学做了该实验后,展开了下列思考与探究:
⑴催化剂MnO2的用量对反应速率有没有影响呢?
他做了这样一组实验:每次均用30mL10%的H202溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
|
实验次序 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
MnO2粉末用量(克) |
0.1 |
0.2 |
0.3 |
0.4 |
0.5 |
0.6 |
0.7 |
0.8 |
0.9 |
1.0 |
|
所用时间(秒) |
17 |
8 |
7 |
5 |
4 |
3 |
2 |
2 |
2 |
2 |
请分析表中数据回答:MnO2的用量对反应速率有没有影响呢?如果有,是怎样影响的呢?
。
⑵H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验。记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
|
实验次序 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
H2O2溶液溶质质量分数 |
1% |
3% |
5% |
10% |
15% |
20% |
25% |
30% |
|
MnO2粉末用量(克) |
0.2 |
0.2 |
0.2 |
0.2 |
0.2 |
0.2 |
0.2 |
0.2 |
|
收集到540mL气体时所用时间(秒) |
660 |
220 |
205 |
80 |
25 |
9 |
4 |
3 |
|
反应后液体温度(℃) |
24 |
34 |
39 |
56 |
65 |
67 |
69 |
70 |
请分析表中数据回答:H2O2溶液的溶质质量分数对反应速率有没有影响呢?如果有,是怎样影响的呢?
。
由表中数据还可看出,该反应是个 反应(填“放热”或“吸热”)。
⑶还有哪些因素可能影响该反应的速率呢?请说出你的一个猜想: 。
25.(7分)右图是费俊龙和聂海胜在“神舟”六号飞船中的照片,请你从化学的视角对神六飞船的有关信息进行思考并作答。
⑴航天员在太空中每人每天大约需要0.9kg氧气、2.5 L水、0.6 kg食物,排出1.0 kg二氧化碳、1.8kg水蒸气等。上述的物质中,属于单质的是____________,属于化合物的是
___________,属于混合物的是___________。 ⑵为了处理人体排出的CO2,飞船上采用了与氢氧化钠化学性质相似的氢氧化锂(LiOH)作为吸收剂。LiOH中锂元素的化合价是______。
⑶随着原始大气中O2缓慢地增加,CH4、NH3、CO等气体逐渐被氧化而缓慢地减少,使大气的成分逐渐演化成现代大气。原始大气中NH3可转化为现代大气中的 。
⑷在神六飞船中有篮球大小的储氧瓶6个,储氮瓶2个,它们是航天员的生命之源。舱内空气一天一换。宇航员说:“舱内的空气比地面还好。”请你设计:怎样使得舱内气体成分大致和地面保持一致?
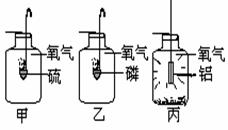
24.(6分)甲、乙、丙是三个实验的示意图,根据图中所发生的化学反应现象及化学反应原理,进行总结归纳并回答下列问题:
 ⑴所发生的三个反应有多
⑴所发生的三个反应有多
个共同的特点,分别是﹕
① ;
② ;
③ ;
④
⑵甲实验进行时,燃烧匙中硫的状态是 。
 ⑶任选上述三个实验中的一个,写出反应的化学方程式:
。
⑶任选上述三个实验中的一个,写出反应的化学方程式:
。
23.(6分)人类发明并使用氟里昂(主要用作致冷剂)若干年后,科学家发现氟里昂在紫外线的照射下能分解出氯原子破坏臭氧层,其破坏臭氧的循环示意图如下:
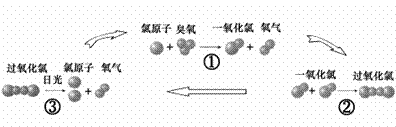
⑴请写出臭氧的化学式_______;
⑵上述反应属于化合反应的是(填序号)__________;
⑶经过上述①②③的反应过程后,反应物氯原子的个数是否发生变化?______(答:是或否)。
⑷诺贝尔奖金获得者莫里纳博士指出:“少量的氟里昂就能对臭氧层产生巨大的影响”,请你根据循环示意图论证他的观点
。
⑸在科学家的建议下,许多国家签署了停止使用和消费氟里昂的协议,使得大气中氟里昂的含量得到了控制。请你根据本题提供的信息就怎样有效保护我们的环境谈一点建议或认识:_____________________________________________________。
22.(4分)右表是小华对自己吸入的气体和呼出的气体进行探究的结果(体积分数)
⑴请你判断:X是_____,Y是____。(填化学式)
⑵请你回答:因参与新陈代谢而被人体消耗的是_____。
⑶请你分析:X气体在呼吸过程中没有参与化学反应,但呼出气体中体积分数却减少了,原因是:___________________________________________ ____________________________________________。
21.(4分)完成下列化学反应方程式并标出带“·”元素的化合价。
+1 +2 -2 +2 -2
H2O2 + BaSO3 = BaSO4↓+
|
气体 |
吸入气体 |
呼出气体 |
|
X |
78.25% |
74.88% |
|
Y |
21.05% |
15.26% |
|
CO2 |
0. 04% |
3.68% |
|
H2O |
0. 66 % |
6.18% |
20.2005年3月,国家质检局查出一些辣椒酱、番茄酱等食品中含有工业染色剂“苏丹红一号”,人食用后可能致癌。“苏丹红一号”的化学式为C16H12N2O 。下列有关“苏丹红一号”的说法中正确的是
A.“苏丹红一号”属于氧化物
B.“苏丹红一号”由30个原子构成
C.“苏丹红一号”的相对分子质量为248
D.“苏丹红一号”由四种元素组成
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com