
14ЃЎ(4Зж)ЪЕбщЬНОПЃКЧтбѕЛЏФЦШмвКжаФФвЛжжСЃзг(H2OЁЂNa+ЁЂOH-)ФмЪЙжИЪОМСБфЩЋЁЃ
ЁЁЁЁ ЪЕбщВНжшЃК
ЁЁЁЁ (1)дкЕквЛжЇЪдЙмжаМгШыдМ2 mLеєСѓЫЎЃЌЕЮШЫМИЕЮЮоЩЋЗгЬЊЪдвКЃЌЙлВьЯжЯѓЃЛ
ЁЁЁЁ (2)дкЕкЖўжЇЪдЙмжаМгШыдМ2 mL NaCl(pH=7)ШмвКЃЌЕЮШыМИЕЮЗгЬЊЪдвКЃЌЙлВьЯжЯѓЃЛ
ЁЁЁЁ (3)дкЕкШ§жЇЪдЙмжаМгШыдМ2 mL NaOHШмвКЃЌЕЮШыМИЕЮЮоЩЋЗгЬЊЪдвКЃЌЙлВьЯжЯѓЃЛ
ЁЁЁЁ ЭЈЙ§ЩЯЪіЪЕбщЕФЬНОПЃЌЛиД№ЯТСаЮЪЬт(ЯТЪіЁАЯжЯѓЁБЪЧжИЃКЮоЩЋЗгЬЊЪдвКЪЧЗёБфКь)ЃК
ЁЁЁЁ ЪЕбщ(1)ФуЕУГіЕФНсТлЪЧЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛ
ЁЁЁЁ ЪЕбщ(2)ЫЕУїNa+РызгЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЛ
ЪЕбщ(3)ПДЕНЕФЯжЯѓЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЃЛФуЕУГіЕФНсТлЪЧЃКЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
13ЃЎ(4Зж)аПгыбЮЫсЗДгІПЩжЦЕУЧтЦјЃЌСэвЛВњЮяЮЊТШЛЏаПЃЌЪдаДГіЗДгІЕФЛЏбЇЗНГЬЪН
ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
(1)вЛБфЃКШєгУA+BЁњABБэЪОЛЏКЯЗДгІЁЃABЁњA+BЃЌБэЪОЗжНтЗДгІЃЌдђЩЯЪіЗДгІПЩБэЪОЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁ (2) ЖўБфЃКШєгУ6.5 gаПКЭзуСПбЮЫсШмвКЗДгІПЩжЦЕУH2ЁЁЁЁЁЁЁЁЁЁ gЁЃ
ЁЁ (3)Ш§БфЃКШєгУ100 gбЮЫсШмвККЭвЛЖЈСПZnГфЗжЗДгІКѓЃЌШмвКжЪСПБфЮЊ106.3 gЃЌЮЪЭЌЪБжЦЕУH2ЁЁЁЁЁЁЁЁ gЁЃ
12ЃЎ(2Зж)жаПМЧАЃЌдцзЏЪаЖдГѕжаБЯвЕЩњНјааЛЏбЇЪЕбщВйзїПМКЫЃЌаЁЯшГщЕНЕФЬтЧЉЪЧЃКМьбщШмвКЕФЫсМюадЁЃЫћбЁдёзЯЩЋЪЏШяЪдвКЭъГЩСЫетИіЪЕбщЁЃвЛжБЯВЛЖПЦбЇЬНОПЕФЫћдкЕУжЊГЩМЈКЯИёКѓЃЌСЂМДЯђРЯЪІбЏЮЪЃЌжЊЕРСЫбљЦЗ1ЪЧЯЁNaClШмвКЃЌбљЦЗ2ЪЧЯЁHClШмвКЃЌбљЦЗ3ЪЧЯЁNa2CO3ШмвКЁЃЯИаФЕФаЁЯшЛЙЗЂЯжздМКЕФЗЯвКИзРяЕФЗЯвКЯдКьЩЋЃЛЧыФуАяжњаЁЯшЗжЮіЃК
(1)ЗЯвКРявЛЖЈКЌгаЕФЮяжЪЪЧЁЁЁЁЁЁЁЁЁЁ ЁЁ(ЪЏШяЪдвККЭЫЎВЛЬю)ЁЃ
(2)ЗЯвКГЪКьЩЋЕФдвђПЩФмЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
11ЃЎ(3Зж)вЛЖЈжЪСПЕФЬМдкбѕЦјжаЧЁКУЭъШЋЗДгІЩњГЩЦјЬхЃЌгУЁАДПОЛЮяЁЂЛьКЯЮяЁБЬюЯТСаПеАзЃК
ЁЁЁЁ (1)ШєЩњГЩЕФЦјЬхжаЬМдЊЫигыбѕдЊЫиЕФжЪСПБШЮЊ3ЃК8ЃЌдђЩњГЩЮяЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁЁЁ (2)ШєЩњГЩЕФЦјЬхжаЬМдЊЫигыбѕдЊЫиЕФжЪСПБШЮЊ3ЃК4ЃЌдђЩњГЩЮяЮЊЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЁЁЁЁ (3)ШєЩњГЩЕФЦјЬхжаЬМдЊЫигыбѕдЊЫиЕФжЪСПБШНщгк3ЃК8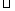 3ЃК4жЎМфЃЌдђЩњГЩЮяЮЊЁЁЁЁЁЁ ЁЃ
3ЃК4жЎМфЃЌдђЩњГЩЮяЮЊЁЁЁЁЁЁ ЁЃ
10ЃЎ(4Зж)гаWЁЂXЁЂYЁЂZЫФжжЮяжЪЃЌЫќУЧдквЛЖЈЬѕМўЯТгаШчЯТзЊЛЏЙиЯЕЃК
ЁЁЁЁ ЂйW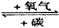 CO2ЁЁ ЂкY
CO2ЁЁ ЂкY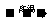 CaOЪЎX
CaOЪЎX ЁЁ ЂлZ(ШмНт)+XЁњYЁ§(АзЩЋ)+ H2OЁЁЁЁ ЧыаДГіИїЮяжЪЮЪЯрЛЅзЊЛЏЕФЛЏбЇЗНГЬЪНЃК
ЁЁ ЂлZ(ШмНт)+XЁњYЁ§(АзЩЋ)+ H2OЁЁЁЁ ЧыаДГіИїЮяжЪЮЪЯрЛЅзЊЛЏЕФЛЏбЇЗНГЬЪНЃК
ЂйЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЌЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂкЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
ЂлЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ ЁЃ
9ЃЎ(5Зж)дкHЁЂOЁЂCЁЂClЁЂCaЮхжждЊЫижаЃЌбЁдёЪЪЕБдЊЫиЃЌзщГЩЗћКЯЯТСавЊЧѓЕФЮяжЪЃЌНЋЦфЛЏбЇЪНЬюШыПеИёжаЃК
ЁЁЁЁ ПЩгУгкШЫЙЄНЕгъЕФбѕЛЏЮяЁЁЁЁЁЁЁЁЁЁ ЁЁЃЛПЩгУгкН№ЪєБэУцГ§атЕФЫсЁЁЁЁ ЁЁЁЁЁЁЁЁЃЛПЩИФСМЫсадЭСШРЕФМюЁЁЁЁЁЁЁЁЁЁ ЁЁЃЛПЩзїИЩдяМСЕФН№ЪєбѕЛЏЮяЁЁЁЁЁЁЁЁЁЁ ЁЁЃЛЯрЖдЗжзгжЪСПзюаЁЕФбѕЛЏЮяЪЧЁЁЁЁЁЁЁЁЁЁ ЁЁЁЃ
8ЃЎаПЗлЁЂТСЗлЁЂЬњЗлЁЂУОЗлЕФЛьКЯЮя3.8 gгывЛЖЈжЪСПЕФШмжЪжЪСПЗжЪ§ЮЊ25%ЕФЯЁСђЫсЧЁКУЭъШЋЗДгІЃЌНЋЗДгІКѓЕФЛьКЯЮяеєЗЂЫЎЗнЕУЙЬЬх(ВЛКЌНсОЇЫЎ)11 gЃЌдђЗДгІжаЩњГЩЧтЦјЕФжЪСПЮЊ
ЁЁ AЃЎ0.15 gЁЁЁЁ ЁЁЁЁЁЁBЃЎ0.20 gЁЁ ЁЁЁЁЁЁCЃЎ0.30 g ЁЁЁЁЁЁЁЁDЃЎ0.45 g
7ЃЎCaCO3ЁњCa(OH) 2ЁњNaoHЕФИїВНзЊЛЏжаЃЌУЛгаЩцМАЕНЕФЛљБОЗДгІРраЭЪЧ
ЁЁ AЃЎИДЗжНтЗДгІ ЁЁЁЁBЃЎЛЏКЯЗДгІЁЁЁЁ CЃЎжУЛЛЗДгІЁЁЁЁ ЁЁЁЁDЃЎЗжНтЗДгІ
6ЃЎНЋCOЁЂN2ЁЂO2ЁЂHCl ЫФжжЦјЬхЕФЛьКЯЮявРДЮЭЈЙ§Na2CO3ШмвКЁЂзЦШШЕФЭЭјЁЂЪЏЛвЫЎЁЂзЦШШЕФбѕЛЏЭЃЌзюКѓЪЃЯТЕФЦјЬхЪЧ(ЁЁЁЁ )
AЃЎN2КЭCOЁЁ ЁЁЁЁЁЁBЃЎN2 ЁЁЁЁЁЁЁЁCЃЎN2КЭCO2 ЁЁЁЁЁЁЁЁDЃЎN2КЭO2ЁЁЁЁ
5ЃЎКЃЫЎЕЛЏПЩгУФЄЗжРыММЪѕЁЃШчгвЭМЫљЪОЃЌЖдЕЛЏФЄгвВрЕФКЃЫЎМгбЙЃЌЫЎЗжзгПЩвдЭИЙ§ЕЛЏФЄНјШызѓВрЕЫЎГиЃЌЖјКЃЫЎжаЕФИїжжРызгВЛФмЭЈЙ§ЕЛЏФЄЃЌДгЖјЕУЕНЕЫЎЁЃЖдМгбЙКѓгвВрКЃЫЎГЩЗжБфЛЏНјааЗжЮіЃЌе§ШЗЕФЪЧЁЁЁЁ
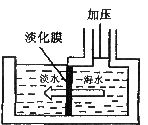
ЁЁ AЃЎШмжЪжЪСПдіМг ЁЁЁЁBЃЎШмМСжЪСПМѕЩй
ЁЁ CЃЎШмвКжЪСПВЛБфЁЁЁЁ DЃЎШмжЪжЪСПЗжЪ§МѕЩй
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com