
25.(9分)钢铁工业是国家工业的基础。2007年我国粗钢产量接近5亿吨,居世界前列。某校兴趣小组取某种钢样进行试验,请计算:
(1)取钢样(假设只含铁单质和碳单质)粉末100g,在氧气中充分燃烧,得到CO2气体4.4g,此钢样粉末中碳的质量分数为__________(保留到0.1%)。
(2)分别向四份不同质量的钢样粉末中加入100g稀硫酸溶液,充分反应后,测得的实验数据如下表所示:
|
序数 质量 |
实验1 |
实验2 |
实验3 |
实验4 |
|
钢样粉末的质量 |
2.84g |
4.25g |
6.23g |
7.51g |
|
生成H2的质量 |
0.10g |
0.15g |
0.20g |
0.20g |
①硫酸溶液中溶质的质量是__________g。
②求在实验3中反应后溶液的溶质质量分数。
24.(5分)农作物的无土栽培可以显著提高产品的产量和质量。某茄子的无土栽培营养液中含有7.08%的KNO3。
(1)KNO3属于__________(填“复合肥料”、“氮肥”、“钾肥”或“磷肥”)。其中氮、氧元素的质量比为__________。
(2)要配制150kg该营养液,需要KNO3的质量是__________kg。
23.(10分)某研究性学习小组对“SO2能否与H2O反应生成酸”进行探究。请你参与他们的探究活动,并回答有关问题。
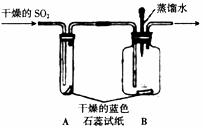
(1)查阅资料:①SO2常温下是一种无色气体,易溶于水;②酸能使蓝色石蕊试纸变成红色;③SO2有毒。
(2)提出假设:SO2能与H2O反应生成酸。
(3)实验探究:设计如上图所示装置进行实验。
①实验过程中,A装置内蓝色石蕊试纸的颜色始终没有变化。A装置的作用是___________。
②在通入SO2之前将B装置中胶头滴管内的蒸馏水滴到蓝色石蕊试纸上,未见试纸颜色发生变化,此步操作的目的是______________。当有SO2通过时发现湿润的蓝色石蕊试纸变红,此现象说明_____________,此过程中反应的化学方程式为________________________。
(4)结论:原假设成立。
(5)反思与评价:该实验方案中,有一个明显的疏漏,请你帮他们指出不足之处:________________________________________。
(6)拓展探究:该研究性学习小组取刚降到硫酸厂(生产过程中产生SO2)附近的雨水进行测定,每隔几分钟测一次pH,其数据如下表所示:
|
测定时刻 |
5:05 |
5:10 |
5:15 |
5:20 |
5:25 |
5:30 |
5:35 |
|
pH |
4.95 |
4.94 |
4.94 |
4.88 |
4.86 |
4.85 |
4.85 |
分析上述数据的变化,你可得出的结论是______________________________;
针对此结论,你猜测其中的原因为____________________________________。
结合大理石雕像受到酸雨腐蚀的事实,你认为碳酸、硫酸、亚硫酸(H2SO3)酸性由强到弱的顺序是____________________。
22.(13分)现有以下实验仪器,请按要求填空:
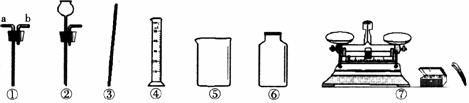
(1)仪器⑤的名称是__________;配制一定质量分数的氯化钠溶液,需用到的仪器有__________(填序号),还缺少的仪器是__________(填名称);如果用石灰石与盐酸反应制取CO2,可选上述仪器中的__________(填序号)组合成制气装置。
(2)某同学利用仪器①与⑥组合成一个贮气装置。当装满水用排水法收集甲烷(甲烷难溶于水、比空气轻)时,气体应从仪器①的__________(填“a”或“b”)通入;集满甲烷后将其导出使用时,水应该从仪器①的__________(填“a”或“b”)导入。该装置还有其他用途,请你任举一例:___________。
(3)下列对实验现象或实验操作的叙述正确的是__________(填序号,选错一个扣1分,本小题不出现负分)。
①铁丝在空气中燃烧产生黄色火焰;
②镁条在空气中燃烧发出耀眼的白光;
③将CO还原Fe2O3的尾气直接排入空气;
④不慎将氢氧化钠溶液沾在皮肤上,要用较多的水冲洗,再涂上稀硼酸溶液;
⑤加热高锰酸钾制备氧气、并用排水法收集满氧气后,先移出导管,后撤酒精灯。
21.(9分)某化工厂排出的废水透明、澄清、略显蓝色。一同学取少量废水,加入过量的盐酸,有不溶于稀硝酸的白色沉淀生成。过滤,所得的滤液分成两份,一份滤液中加入稀硫酸,也有不溶于稀硝酸的白色沉淀生成;另一份滤液中加入氢氧化钠溶液,产生蓝色溶液。试回答:
(1)用化学式回答:加入过量的盐酸,生成的白色沉淀是__________;生成的蓝色溶液是__________。
(2)废水中一定含有的物质是__________(填编号)。
A.氯化物 B.硫酸盐 C.硝酸盐 D.碳酸盐
(3)该同学设计了一个从废水中除去重金属离子的实验方案如下[已知白色的Fe(OH)2固体在潮湿的空气中可生成红褐色的Fe(OH)3]:
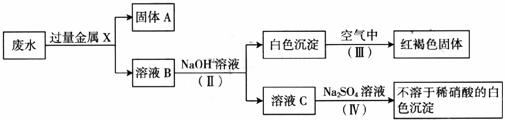
①金属X为__________,固体A中一定含有的物质为(写化学式)__________。
②B溶液中的溶质一定含有__________和__________(填序号字母)。
A.K2CO3 B.Fe(NO3)2 C.MgCl2 D.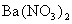
③第Ⅳ步反应的化学方程式为______________________________。
20.(6分)A-H都是初中化学中的常见物质,它们之间的转化关系如下图所示。A是天然气的主要成分,E是一种常见的食品干燥剂。请回答:
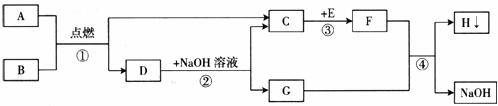
(1)A的化学式为__________。
(2)反应③的基本反应类型是__________。
(3)反应②的化学方程式为___________________,反应④的化学方程式为__________ ____________________。
19.(4分)2008年北京奥运火炬“祥云”的设计体现了“科技奥运”、“绿色奥运”的主题。
|
|
丙烷 |
丁烷 |
|
熔点(℃) |
-189.7 |
-138.4 |
|
沸点(℃) |
-42.1 |
-0.5 |
(1)丁烷曾被有些国家选为火炬燃料。由上表可知,在低温地区,丁烷会处于________(填“固态”、“液态”或“气态”),不利于点火燃烧,因此“祥云”采用丙烷为燃料。丙烷在空气中完全燃烧后的产物是CO2和H2O,对环境没有污染,则丙烷必定含有的两种元素是____________________。
(2)普通塑料制品难以自然降解,遗弃后容易造成“白色污染”,因此,“祥云”采用可回收重复利用的铝合金作为外壳材料。铝具有较强抗腐蚀性的原因___________________。
(3)“祥云”火炬上的“云纹”,具有浓郁的中国特色,主要是用酸等物质腐蚀雕刻形成的。若用稀盐酸来雕刻,则铝与稀盐酸反应的化学方程式为__________________________。
18.(3分)下图是甲、乙两物质的溶解度曲线:
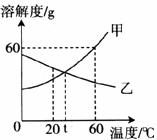
(1)甲、乙两物质溶解度相等时的温度为__________℃。
(2)60℃时,160g甲的饱和溶液中溶剂的质量为__________g。
(3)60℃时,将乙的饱和溶液降温至20℃时,以下描述正确的是_________(填字母)。
A.有乙物质的晶体析出 B.乙的溶解度不变
C.乙的溶质质量分数增大 D.乙溶液为不饱和溶液
17.(4分)下表是部分元素的原子结构示意图、主要化合价等信息,请完成以下填空:
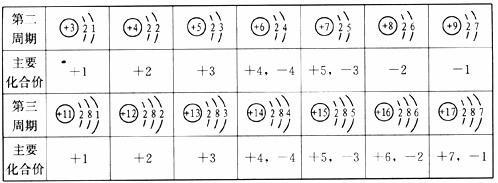
(1)铝原子的最外层电子数是__________。
(2)核电荷数为12的元素符号是__________。
(3)原子序数为8和14的元素组成化合物的化学式是__________。
(4)请你总结出此表中的原子结构与元素化合价或周期数的关系________(任写一条)。
16.(5分)某化肥包装袋上的部分说明如下图所示。
|
硝酸铵 化学式 NH4NO3 净重 50kg 含氮量 ≥30% 注意事项 密封贮存、防潮防晒、隔绝热源…… |
(1)硝酸铵属化学肥料中的__________(填序号)。
A.钾肥 B.氮肥 C.磷肥
(2)硝酸铵应具有的性质是__________(填序号)。
A.易溶于水 B.有挥发性 C.受热易分解
(3)硝酸铵能与强碱反应,其中与烧碱反应的方程式为: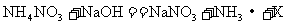 ,则X的化学式是:__________;施用该类肥料时,要避免与__________(填“酸”或“碱”)性物质混用,否则会降低肥效。
,则X的化学式是:__________;施用该类肥料时,要避免与__________(填“酸”或“碱”)性物质混用,否则会降低肥效。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com