
5.以下个物质间的每步转化不能通过一步反应就能实现的是 ( )
A.C→CO→CO2→Na2CO3 B.Fe→Fe3O4→Fe(OH)3→FeCl3
C.Na→Na2O2→Na2CO3→NaOH D.N2→NO→NO2→HNO3
|
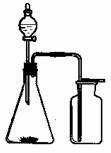 ①浓氨水和固体NaOH制NH3 ②大理石和稀盐酸制CO2
①浓氨水和固体NaOH制NH3 ②大理石和稀盐酸制CO2
③过氧化氢溶液和二氧化锰制O2 ④稀硝酸和铜片制NO
⑤浓盐酸和二氧化锰制Cl2 ⑥电石和水制C2H2
⑦锌粒和稀硫酸制H2 ⑧乙醇和浓硫酸制C2H4
A.②③ B.①⑥⑦
C.②⑤⑧ D.①④⑥
27、(11分)有X、Y、Z三种元素,已知:
①X2-、Y-均与Y的气态氢化物分子具有相同的电子数;
②Z与Y可组成化合物ZY3,ZY3溶液遇苯酚呈紫色。
请回答:
⑴Y的最高价氧化物对应水化物的化学式是 。
⑵将ZY3溶液滴入沸水可得红褐色液体,反应的离子方程式是
,
此液体具有的性质是 (填写序号字母)。
a.光束通过该液体时形成光亮的“通路”
b.插入电极通直流电后,有一极附近液体颜色加深
c.向该液体中加入硝酸银溶液,无沉淀产生
d.将该液体加热、蒸干、灼烧后,有氧化物生成
⑶X单质在空气中燃烧生成一种无色有刺激性气味的气体。
①已知一定条件下,每1mol该气体被O2氧化放热98.0kJ。若2mol 该气体与1mol O2在此条件下发生反应,达到平衡时放出的热量是176.4kJ,则该气体的转化率为 。
②原无色有刺激性气味的气体与含1.5molY的一种含氧酸(该酸的某盐常用于实验室制取氧气)的溶液在一定条件下反应,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式是
。
26、(7分)合成氨工业生产中所用的α-Fe催化剂的主要成分是FeO、Fe2O3
(1)某FeO、Fe2O3混合物中,铁、氧的物质的量之比为4:5,其中Fe2+与Fe3+物质的量之比为___________。
(2)当催化剂中Fe2+与Fe3+的物质的量之比为1:2时,其催化活性最高,此时铁的氧化物混合物中铁的质量分数为____________
|
2 Fe2O3十C → 4FeO十CO2↑。为制得这种活性最高的催化剂,应向480g Fe2O3粉末中加入炭粉的质量为_________g。
25、(10 分)某芳香烃A有如下转化关系:
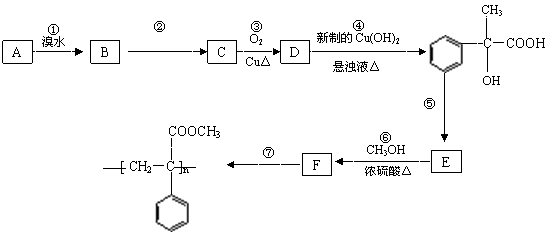
按要求填空:
⑴写出反应②和⑤的反应条件:② ;⑤ 。
⑵写出A和F结构简式:A ;F 。
⑶写出反应③对应的化学方程式:
③ 。
24、(10分)(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示______________,K值大小与温度的关系是:温度升高,K值______________。(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)+H2O(g)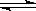 CO2(g)+H2(g) △H<0
CO2(g)+H2(g) △H<0
CO和H2O浓度变化如左图,则0-4min的平均反应速率v(CO)=______mol/(L·min)
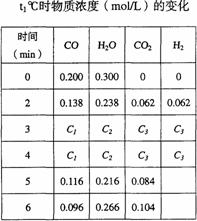
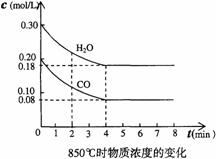
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如右表。
①表中3min-4min之间反应处于_________状态;C1数值________0.08mol/L(填大于、小于或等于)。
②反应在4min-5min问,平衡向逆反应方向移动,可能的原因是________(单选),
表中5min-6min之间数值发生变化,可能的原因是________(单选)。
a. 增加水蒸气 b. 降低温度
c. 使用催化剂 d. 增加氢气浓度
23、(12分)有常见A、B、C三种短周期元素,它们的原子序数逐渐增大,B元素原子最外层电子数是C元素原子最外层电子数的一半,A元素最外层电子数比B多一个。甲、乙、丙是3种含氧酸的钠盐,甲中含B元素,乙中含C元素,丙中含A元素,甲、丙溶液pH>7,乙溶液pH<7;丁为气体,戊为淡黄色固体。甲、乙、丙、丁、戊、己六种物质之间的相互反应关系如下图:
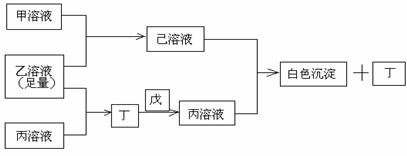
请回答:
(1)写出C元素的原子结构示意图_______________,写出丁和戊的电子式____________、_________________;
(2)用有关化学用语解释:
乙溶液呈酸性的原因____________________________;
丙溶液呈碱性的原因____________________________;
(3)写出有关反应的离子方程式:
①乙溶液+丙溶液→丁______________________________;
②己溶液+丙溶液→丁______________________________。
22、(12分)化合物 YX2 、ZX2 中, X、Y、Z 都是短周期元素, X 与Y属同一周期,Y 是 Z 的同族元素, Y原子的最外层中 P能级电子数等于前一电子层电子总数。X 原子最外层的P能级中有一个轨道是充填了两个电子的。
(1)用轨道表示式表示X 的核外电子排布 ;Y的电子排布式为 ;Z的电子排布式为
(2)YX2 的化学式是 它是 分子(填极性分子或非极性分子),它的晶体类型是 晶体。ZX2 的化学式是
,它的晶体类型是 晶体。YX2 的熔点、沸点比ZX2 的 。
21、(11分)今天是化学实验室开放日,老师拿出两瓶无标签的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体。请对此气体展开一系列探究。并完成下列实验报告。
(1)①此气体是什么物质?验证它的实验方案如下:
|
猜想 |
实验步骤 |
现象及结论 |
|
此气体可能是____ |
_________________________ ________________________ |
_____________ _____________ __ |
产生此气体的化学方程式可能是___________________________.
②想制取该气体,采用的发生装置可选用如图1中的__________ (对应填序号,下同),收集装置是_____.
③如用图2装置收集该气体,气体由_____端(填“a”“b”)导入.
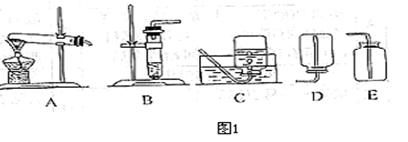
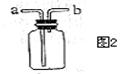
(2)猜想此无色气体还有没有可能是另一种气体,如果有,请写出产生它的化学方程式______ ________________ ___(只须写一种)。
20、(10分)某化学兴趣小组按照下列方案进行“由含铁废铝制备硫酸铝晶体”的实验:
步骤1:取一定量含铁废铝,加足量的NaOH溶液,反应完全后过滤。
步骤2:边搅拌边向滤液中滴加稀硫酸至溶液的pH=8-9,静置、过滤、洗涤。
步骤3:将步骤2中得到的固体溶于足量的稀硫酸。
步骤4:将得到的溶液蒸发浓缩、冷却、结晶、过滤、干燥。
请回答以下问题:
⑴上述实验中的过滤操作需要玻璃棒、______________、______________等玻璃仪器。
⑵步骤1过滤的目的是__________________________________________。
⑶当步骤2中的溶液pH=8-9时,检验沉淀是否完全的方法是______________。
⑷步骤2中溶液的pH控制较难操作,可改用____________________。
19.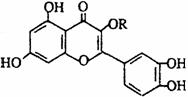 天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂。关于维生素P的叙述错误的是
天然维生素P(结构如图)存在于槐树花蕾中,它是一种营养增补剂。关于维生素P的叙述错误的是
A. 可以和溴水反应
B. 可用有机溶剂萃取
C. 分子中有三个苯环
D. 1mol维生素P可以和5molNaOH反应
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com