
9.2006年6月5日是第35个世界环境日,国家环保总局确定的主题是:“生态安全与环境友好型社会”。下列说法不符合这一主题的是
A.用“绿色化学”工艺,使原料尽可能转化为所需要的物质
B.回收废电池,减少对环境的污染
C.为使农作物高产,大量施用化肥和农药
D.研制开发燃料电池汽车,消除机动车尾气污染
29.(14分)将5.1g镁铝合金溶于60mL 5.0 mol·L-1H2SO4溶液中,完全溶解后再加入65mL 10.0mol·L-1的NaOH溶液,得到沉淀的质量为9.7g,继续滴加NaOH溶液时沉淀会减少。
(1)当加入 mL NaOH溶液时,可使溶解在硫酸的Mg2+和Al3+恰好完全沉淀。
(2)合金中镁的质量为 g;铝的质量为 g。
(3)计算合金溶于硫酸时所产生的氢气在标准状况下的体积为 L
28.(18分)
已知:①醛在一定条件可以两分子加成生成羟醛化合物:
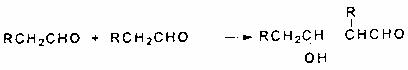
而该产物不稳定,受热即脱水而成为不饱和醛。
B是一种芳香族化合物。根据如图所示转化关系填空(所有无机物均已略去)
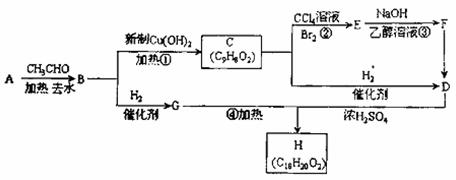
(1)写出B、F的结构简式:
B ;
F 。
(2)写出②和③反应的反应类型:
② ;③ 。
(3)写出G、D反应生成H的化学方程式
。
(4)F若与H2发生加成反应,每摩F最多消耗的H2的物质的量为 mol。
27.(16分)实验室用燃烧法测定某氨基酸CxHyOzNp的分子组成。取mg该种氨基酸放在纯氧中充分燃烧,生成CO2、H2O和N2,实验装置如下图:
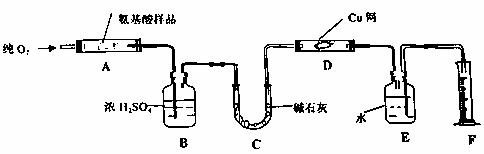
请回答下列有关问题:
(1)实验开始时,首先要通入一段时间的氧气,其理由是:
,
(2)以上装置中需要加热的仪器有 (填字母,下同)操作时应先点燃
处的酒精灯。
(3)A装置中发生反应的化学方程式是:
(4)装置D的作用是:
(5)读取N2体积时,应注意:① ;
② 。
(6)实验中测得N2的体积VmL(已折算为标准状况),为确定此氨基酸的分子式,还需要的有关数据有 (用字母填空)。
A.生成二氧化碳气体的质量
B.氨基酸的相对分子质量
C.通入氧气的体积
D.生成水的质量
26.(18分)物质的转化关系如下图所示,其中甲可由两种单质直接化合得到,乙为金属单质,F的溶液中只含有一种溶质,G为酸,乙在G的浓溶液中发生钝化。有的反应可能在水溶液中进行,有的反应中反应物和生成物未全部给出,反应条件也未注明。
|
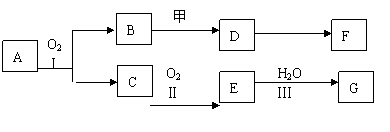
(1)若用两根玻璃棒分别蘸取A、G的浓溶液并使它们接近,有大量白烟生成;甲为一种淡黄色固体,D、F的溶液均呈碱性。则
①1.7gA与O2与反应生成气态的B和C时放出22.67kJ热量,写出该反应的热化学方程式: 。
②B与甲反应的离子方程式是 。
③D的水溶液和F的水溶液中由水电离出的c(OH‑-) (填字母序号)。
a.前者大 b.后者大 c.一样大 d.不知浓度,无法比较
(2)若B为红棕色固体,C能使品红褪色,D的水溶液中加入HNO3酸化的AgNO3溶液有白色沉淀生成。则
①在C转变为E的过程中,工业上常通入过量的O2,理由是
。
通入过量的O2,C能否全部转变成E ,
理由是 。
②由两种单质直接化合得到甲的反应条件是 或 。
③D和乙反应的离子方程式是 。
13. 某温度下,在一容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是 ( )
某温度下,在一容积可变的容器中,反应2A(g)+B(g) 2C(g)达到平衡时,A、B和C的物质的量分别为4mol、2mol和4mol。保持温度和压强不变,对平衡混合物中三者的物质的量做如下调整,可使平衡右移的是 ( )
A.均减半 B.均加倍
C.均增加1mol D.均减小1mol
第Ⅱ卷(非选择题 共174分)
12.有一种白色粉末由等质量的两种物质混合而成,分别取适量该白色粉末置于三支试管中进行实验。
(1)逐滴加入6mol·L-盐酸,同时不断振荡试管,有气泡产生,反映结束后得到无色透明溶液
(2)加热试管中的白色粉末,试管口有水滴凝结。
(3)逐滴加入6mol·L-硫酸,同时不断振荡试管,有气泡产生,反应结束后试管中还有白色不溶物,下列混合物中符合以上实验现象的是 ( )
A.NaHCO3、AgNO3
B.BaCl2、MgCO3
C.NH4HCO3、MgCl2
D.CaCl2·6H2O、Na2CO3
11.某温度下,100g饱和氯化钠溶液中含有氯化钠26.5g。若向此溶液中添加3.5g氯化钠和6.5g水,则该溶液的质量分数是 ( )
A.26.5% B.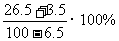
C.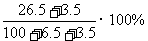 D.30%
D.30%
10.一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应为:2C2H6+7O2+8KOH=4K2CO3+10H2O,有关此电池的推断正确的是 ( )
A.负极反应为14H2O+7O2+28e-=28OH-
B.放电一段时间后,负极周围的pH升高
C.放电过程中KOH的物质的量浓度不变
D.每消耗1mol C2H6,则电路上转移的电子为14mol
9.已知乙烯和乙炔燃烧的热化学方程式分别为:
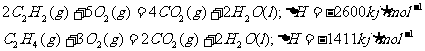
又知氧炔焰的温度比乙烯燃烧时火焰的温度高。据此,下列说法错误的是 ( )
A.物质的燃烧热越大,火焰温度越高
B.烃完全燃烧时,火焰温度的高低不仅仅取决于其燃烧热的高低
C.相同条件下等体积乙烯和乙炔气体完全燃烧时,乙炔放热较少
D.1mol乙烯完全燃烧生成气态产物时,放出的热量小于1411kJ
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com