
1.判断下列有关化学基本概念的依据正确的是
A.氧化还原反应:元素化合价是否变化 B.共价化合物:是否含有共价键
C.强弱电解质:溶液的导电能力大小 D.金属晶体:晶体是否能够导电
25.(10分)向100mLBaCl2、AlCl3和FeCl3的混合溶液A中,逐滴加入Na2SO4和NaOH
的混合溶液B,产生的沉淀总物质的量和加入溶液B的体积关系如右图所示:
(1)当加入B溶液110 mL时,溶液中的沉淀是__________________(填化学式)。
(2)溶液B中Na2SO4与NaOH的物质的量浓度之比____________;从90 mL至100 mL之间加入10 mL B溶液时所发生的离子反应方程式是_________ 。
(3)将A.B溶液中各溶质的物质的量浓度填入下表:
|
溶质 |
Na2SO4 |
NaOH |
BaCl2 |
AlCl3 |
FeCl3 |
浓度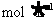 |
|
|
|
|
|
24.(5分)一定质量的氧化镁和氧化钙的混合物刚好与10倍质量的盐酸完全反应,试求盐酸中溶质的质量分数。
23.(10分)已知单质铁溶于-定浓度的硝酸溶液中反应的离子方程式为:aFe+bNO3-+cH+
=dFe2++fFe3++gNO↑+hN2O↑+kH2O(化学计量数a-k均为正整数)。回答下列问题:
(1)根据反应中氮、氢、氧三种元素的原子个数守恒,可得C.g、h的关系式是(用-个代数式表示。下同) 。
(2)根据反应中离子的电荷守恒,可得B.C.D.f的关系式是 。
(3)根据反应中电子转移的总数相等,可得D.f、g、h的关系式是 。
(4)若a=12,且铁和稀硝酸恰好完全反应,则b的取值范围是 ;
c的取值范围是 。
22.(12分)
(1)已知下列反应在一定条件下可以发生:
H2O2+4Fe2++2H+ 2Fe3++2H2O H2O2+2Fe3+ 2Fe2++O2↑+2H+
在以上反应中Fe2+实际上起着 作用,总反应为 。
(2)I2与Fe2+一样也能发生上述类似反应,类比(1)写出合适的化学反应方程式:
H2O2+I2 2HIO,
,总反应为
。
(3)在H2SO4和KI的混合溶液中加入足量的H2O2,放出大量的无色气体,溶液呈棕色,
并可以使淀粉溶液变蓝。有学生认为该反应的离子方程式为:H2O2+2I- I2+O2↑+2H+,这个方程式正确吗?
。若正确,理由是(若认为不正确,该步不必作答)
。若不正确,写出正确的化学反应方程式(若是离子反应,写出离子反应方程式,没有离子反应的,写出化学反应方程式):
。
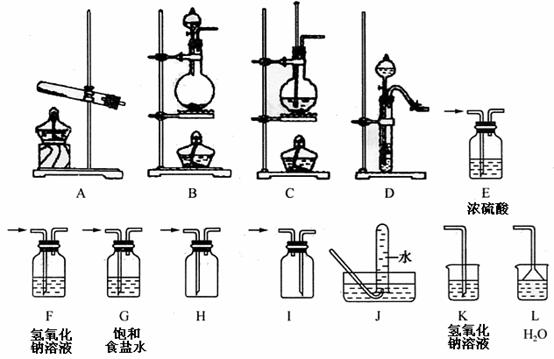
21.(8分)某校化学课外活动小组组装了下列仪器,如图所示。欲经过简单连接,制备中学化学中几种常见气体。
请填写下列表格中的空白:
|
序号 |
气体 |
装置的连接顺序(用编号表示) |
按要求填试剂名称 |
实验室制备该气体的化学反应方程式(是离子反应的要写出离子反应方程式) |
|
(1) |
CO2 |
制备→收集 ( )→( ) |
|
|
|
(2) |
NH3 |
制备→收集→尾气处理 ( )→( )→( ) |
若干燥NH3可选用的试剂 |
|
|
(3) |
Cl2 |
制备→净化→干燥→收集 →尾气处理 ( )→( )→( ) →( )→( ) |
处理尾气的试剂 |
|
20.(7分)位于短周期的四种主族元素A.B.C.D原子序数依次增大,已知A.C位于同一主族,A在周期表中原子半径最小。B.D的最外层电子数相等,且B.D的原子序数之和为A.C原子序数之和的两倍。根据你的推断回答下列问题:
(1)写出由上述元素形成的具有漂白作用的四种物质的化学式 , ,
, 。
(2)C与D形成D的最低价化合物的电子式:______
(3)仅由B.C.D三种元素形成的一种盐,溶于水后呈碱性,请用一个离子方程式表示其呈碱性的原因:______ 。
19.(6分)可用于分离或提纯物质的方法有:
A.分馏 B.盐析 C.过滤 D.重结晶 E、升华 F、渗析 G、电解
H、加热分解 I、蒸馏 J、灼热氧化。如欲分离或提纯下列各组混合物,请选择上
述方法中最合适者,并将相应字母填入题后空格内:
(1)从石油中分离出汽油和煤油等成分
(2)除去淀粉溶液中的少量碘化钠
(3)从油脂皂化反应后的混合液中分离出高级脂肪酸钠
(4)除去粗铜中锌、银等金属
(5)除去水中的Na+、SO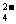 、Cl-等杂质
、Cl-等杂质
(6)除去KNO3晶体中混有的少量NaCl
18.有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),其中Cl-、Br-、I-的个数比为2∶3∶4,向该溶液中通入氯气,使溶液中Cl-和Br-的个数比为3∶1,则通入氯气的物质的量与溶液中剩余的Fe2+的物质的量之比为(还原性I->Fe2+>Br->Cl-) ( )
A.7∶1 B.7∶2 C.7∶3 D.7∶4
|
17.下列各组溶液,不用其他试剂就不能鉴别的是
A.FeCl3、NaNO3、Na2CO3、NaCl B.NaOH、MgSO4、Na2CO3、NaHSO4
C.AgNO3、KNO3、KCl、NaI D.HCl、BaCl2、NaOH、CuSO4
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com