
3.从下列事实所得出的相应结论正确的是
|
|
实验事实 |
结论 |
|
① |
SO2的水溶液可以导电 |
SO2是电解质 |
|
② |
将燃烧的镁条放入CO2中能继续燃烧 |
还原性:Mg>C |
|
③ |
常温下白磷可自燃而氮气须在放电时才与氧气反应 |
非金属性:P>N |
|
④ |
某无色溶液中加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝 |
该溶液中一定有NH4+ |
A.③④ B.②④ C.①② D.全部
2.物质发生化学变化时:①电子总数 ②原子总数 ③分子总数 ④物质的种类 ⑤物质的总质量 ⑥物质的总能量,反应前后肯定不发生变化的是 ( )
A.①②③⑤ B.①②⑤ C.②⑤⑥ D.①④⑤⑥
1.下列各项表达式正确的是 ( )
A.O2-的结构示意图: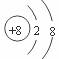 B.Na2S的电子式:
B.Na2S的电子式: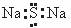
C.乙烯的结构简式:C2H4
D.氮分子的结构式: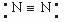
29.(14分)有机物G的分子结构模型如下图所示(图中球与球之间连线表示单键或双键)。
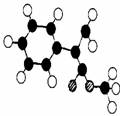
已知: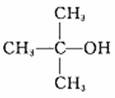 结构相似的醇不能被氧化为醛。由芳香烃A为原料合成G的路线如下:
结构相似的醇不能被氧化为醛。由芳香烃A为原料合成G的路线如下:

(1)写出有机物G的结构简式_________。
(2)A→B的反应类型是___________;E→F的反应类型是____________。
(3)化合物E中的官能团有____________(填名称)。
(4)写出A的加聚反应产物的结构简式_______________;C→D的化学方程式_______________________________;
(5)E的同分异构体有多种,写出符合下列条件的所有同分异构体:
①可用通式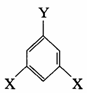 表示(其中X、Y均不是氢原子);
表示(其中X、Y均不是氢原子);
②能发生银镜反应; ③能和金属钠反应产生氢气。
28.(15分)下图所示为常见气体的制备、除杂、性质验证和尾气处理等实验的仪器装置(加热设备及夹持固定装置均略去)。请根据要求完成下列各题(实验装置可从图中选用)。
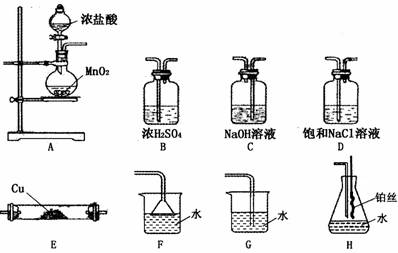
(1)实验室预制取纯净、干燥的Cl2,并验证其和铜的反应,所选装置的顺序依次为(从左向右)__________;需要加热的仪器有_____________,硬质玻璃管E内的现象为______________。
(2)制取无水MgCl2必须在氯化氢气流中进行。若选择装置A、E和尾气处理装置,实现由MgCl2·6H2O晶体制取无水MgCl2,应将烧瓶中的MnO2试剂改为___________,将E管中的试剂改为MgCl2·6H2O晶体,加热E玻璃管。制取无水MgCl2必须在氯化氢气流中进行的原因是__________;尾气处理装置可选用________________。
(3)若选择装置A和H在实验室模拟氨气的催化氧化实验,应将分液漏斗中的浓盐酸
改为浓氨水,圆底烧瓶中的试剂改为_____________,用H装置吸收一段时间氨气后再通入空气,同时将红热的铂丝(催化剂)插入H装置的锥形瓶内,锥形瓶中可观察到的现象是________;可能发生的反应用化学方程式表示为____________。
27.(16分)由若干种可溶性物质组成的固体混合物X,可能含有的阳离子和阴离子分别是:
|
阳离子 |
Na+ Mg2+ Al3+ Ag+ Ba2+ |
|
阴离子 |
OH- Cl- Cl- SO2-4 CO2-3 |
为了鉴定其中的离子,现进行如下实验,试根据实验现象和要求填空。
(1)取少许该白色固体加水溶解,最后得到无色溶液;用pH试纸检测,溶液的pH为13。则X中一定不存在的离子是_____________。
(2)向溶液中滴加盐酸溶液,刚开始无沉淀,后有沉淀生成,继续滴加沉淀消失,并有无色无味气体逸出。则X中一定存在的离子是____________;又可确定X中一定不存在的离子有________________.
(3)若组成X的物质有三种,则可能是(用化学式表示,写出一组即可)____________。
(4)尚待检验的离子及检验方法是:
|
尚待检验的离子 |
检验方法 |
|
|
|
13.将一定量的钠铝合金置于水中,合金全部溶解,得到20 mL pH=14的溶液,然后用1mol·L-1的盐酸溶液滴定,至沉淀质量最大时消耗盐酸40 mL。原合金中钠的质量为 ( )
A.0.92 g B.0.69 g C.0.46 g D.0.23 g
第Ⅱ卷(非选择题 共174分)
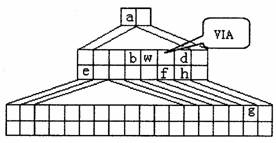
(1)请写出g元素在周期表中的位置_________,并将铁的元素符号填在上图中合适的位置。
(2)下列叙述正确的是_________。
A.氢化物Hd比Hh稳定,H2f的沸点高于H2O
B.离子半径r(e)>r(f)>r(h)
C.化合物bh4与bf2均为非极性分子
D.由图中标出的8种元素形成的10e-结构的阳离子只有Na+和NH+4
(3)已知由元素a、b、w组成的化合物abw可称为“氢某酸”,分子中各原子均达到稳定状态,试写出其电子式(请用其真实化学式填空)_____________;又知此酸对应的钾盐有剧毒,常温下其钾盐溶液的pH=9,则其溶液中由水电离出的c(OH-)=_________mol/L,该溶液中所有离子的浓度由大到小的顺序是(请用其真实化学式填空)_____________。
(4)元素e的某化合物固体呈淡黄色,该物质与e2f的溶液反应生成淡黄色沉淀(没有放出气体)。则反应的离子方程式为(请用其真实化学式填空)____________。
12.下图是工业电解饱和食盐水的装置示意图,下列有关说法不正确的是 ( )
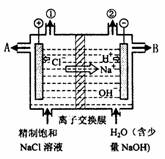
A.装置中的离子交换膜只能让阳离子通过,不能让阴离子通过
B.装置中出口①处的物质是氢气,出口②处的物质是氯气
C.除去杂质后的氢氧化钠溶液从出口B处导出
D.转移电子0.8 mol时产生氢气8.96 L(标准状态)
11.一定条件下,将一定量的A、B、C、D四种物质置于密闭容器中发生如下反应:
m A(s)+n B(g)  p C(g)+q D(g),达到平衡后测得B的浓度为0.5 mol/L。保持温度不变,将密闭容器的容积扩大到原来的两倍,再次达到平衡后测得B的浓度为0.2 mol/L。当其他条件不变时,C在反应混合物中的体积分数(C%)与温度(T)、时间(t)的关系如图所示。下列叙述正确的是 ( )
p C(g)+q D(g),达到平衡后测得B的浓度为0.5 mol/L。保持温度不变,将密闭容器的容积扩大到原来的两倍,再次达到平衡后测得B的浓度为0.2 mol/L。当其他条件不变时,C在反应混合物中的体积分数(C%)与温度(T)、时间(t)的关系如图所示。下列叙述正确的是 ( )
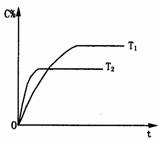
A.容积扩大到原来的两倍,平衡向逆反应方向移动
B.化学方程式中m+n<p+q
C.达到平衡后,若升高温度,平衡向逆反应方向移动
D.达到平衡后,增加A的量,有利于提高B的转化率
10.下列各组离子在指定的溶液中一定能大量共存的是 ( )
①加入Al能放出H2的溶液中:Fe2+、Al3+、NO-3、Cl-
②在pH=11的溶液中:Na+、AlO-2、NO-3、SO2-3
③使甲基橙变红的溶液中:K+、NH+4、Cl-、CO2-3
④加入Mg能放出H2的溶液中:K+、NH+4、Cl-、SO2-4
⑤室温下由水电离的c(H+)和c(OH-)的乘积为1×10-24的溶液中:Ba2+、NO-3 、K+、Cl-
A.①③ B.②③⑤ C.②④⑤ D.①②③
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com