
29.(15分)
有机物A、B、C、D、E、F、G、H、I之间有如下图所示的关系。B的主链上有3个碳原子,G可使溴水褪色。
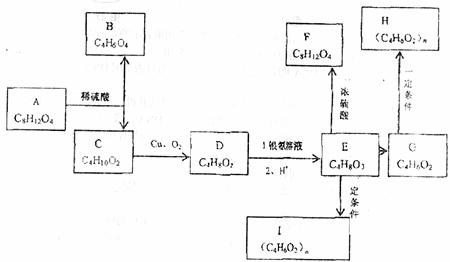
回答下列问题:
(1)E中官能团的名称 。
反应类型:D→E ,E→G 。
(2)A、F的结构简式: , 。
(3)反应的化学方程式:
C→D ,
G→H 。
28.(18分)I、目前,我国采用“接触法”制硫酸,生产设备如图所示:
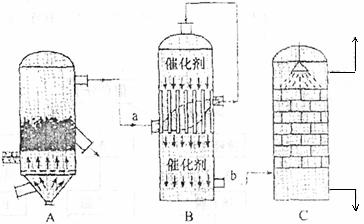
(1)图中设备A的名称是 ,a、b两处所含气体的化学式分别为 、 。
(2)有关接触法制硫酸的下列说法中,不正确的是 。
A.二氧化硫的接触氧化在合成塔中发生
B.吸收塔得到的硫酸浓度为98%
C.煅烧含硫48%的黄铁矿时,若FeS2损失了2%,则S损失4%
D.B装置中反应的条件之一为较高温度是为了提高SO2的转化率
|
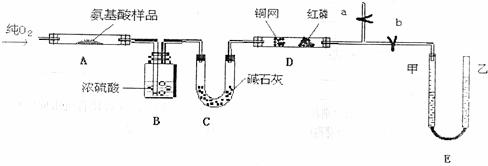
(1)实验开始时,首先打开止水夹a,关闭止水夹b,通入一段时间的氧气,这样做的目的是 ,之后关闭止水夹a。
(2)E装置的作用是测量 的体积,在读反应前后甲管中液面的读数求其差值的过程中,应注意 (填代号)。
a.视线与凹液面最低处相平
b.等待片刻,待乙管中液面不再上升时,立刻读数
c.读数时应上下移动乙管,使甲、乙两管液面相平
d.读数时不一定使甲、乙两管液面相平
(3)严格地说,按上述方案只能确定氨基酸的 。
若要确定此氨基酸的分子式,来要测定该氨基酸的 。
27.(14分)
有一化合物X,其水溶液为浅绿色,可发生如下的转化关系(部分反应物、生成物已略)。其中,X与过量NaOH溶液反应,生成的A、B物质的量之比为1:2。B、D、E、F均为无色气体,M、L为常见的金属单质,在混合液中加入BaCl2溶液可生成不溶于稀盐酸的白色沉淀,H和M反应可放出大量的热。
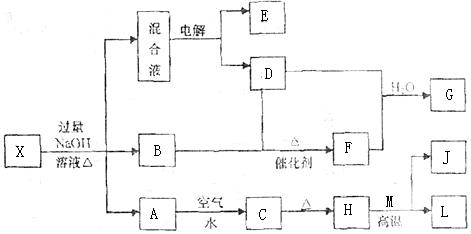
请回答下列问题:
(1)B的空间构型为 ,B气体的检验方法为 。
(2)物质X的化学式为 。
(3)电解混合液时阳极反应式为 。
(4)按要求写出下列反应的化学方程式:
①X与过量Ba(OH)2溶液在无氧条件下加热反应的离子方程式为 。
②L与过量G的稀溶液反应的离子方程式为 。
26.(13分)有原子序数依次增大的六种短周期主族元素A、B、C、D、E、F。其中A与D、B与E分别同主族,B原子最外层电子数为内层电子数的2倍;F元素的原子半径在所在周期的主族元素中最小;C与A、D都可形成两种化合物,且所形成的化合物中各有一种具有漂白性。B、E分别与C形成的化合物晶体类型不同。试回答下列问题:
(1)C、D以原子个数比为1:1形成的化合物的电子式为
(2)E单质的晶体类型是 。
(3)试写出工业用电解溶液法得到单质F的离子方程式:
(4)写出以上六种元素形成的含18个电子的分子式 (任写三种)。
(5)已知几种元素之间形成的化学键的键能如下:
|
化学键 |
A-A |
A-F |
B-E |
C-E |
E-E |
E-F |
|
键能(kJ/mol) |
436 |
431 |
347 |
460 |
176 |
360 |
工业上用含有E、F两种元素(原子个数比为1:4)的化合物在高温下与A单质反应来得到高纯度的单质E。则该反应的热化学方程式为 。
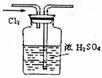
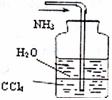
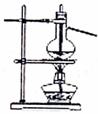
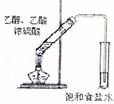
13.用下列实验装置完成对应的实验(部分仪器已省略),能达到实验目的的是 ( )
|
|
A |
B |
C |
D |
|
装置 |
 |
 |
 |
 |
|
实验 |
干燥氯气 |
吸收NH3 |
石油的分馏 |
制取乙酸乙酯 |
第Ⅱ卷
12.将a LSO3气体通过灼热的装有催化剂(V2O5)的硬质玻璃管,反应后测得气体体积增大了bL(气体体积均在同温同压下测定),则下列叙述正确的是 ( )
A.SO3的转化率为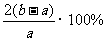
B.混合气体的平均相对分子质量为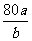
C.反应前与反应后气体的密度之比为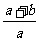
D.混合气体中SO2的体积分数为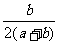
11.常温下,0.2mol/LCH3COOH溶液与0.1mol/L NaOH溶液等体积混合后(忽略混合前后溶液体积的变化),溶液的pH<7,则下列有关此溶液的叙述正确的是 ( )
A.溶液中由水电离产生的H+浓度为1×10-7mol/L
B.c(CH3COO-)+c(CH3COOH)-c(Na+)=0.05mol/L
C.溶液中CH3COOH的电离程度小于CH3COONa的水解程度
D.溶液中离子浓度的大小关系为:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
10.下列装置中,a5是铁电极,其余为石墨电极,烧杯中液体体积均为100mL,放置一段时间后,有关叙述不正确的是(不考虑溶液体积变化) ( )
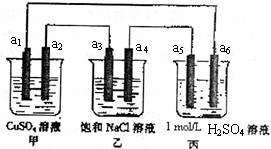
A.丙中的SO42-向a6电极移动
B.a1、a3电极上产生的物质,物质的量比是1:2
C.a2电极上有亮红色固体
D.当装置电路中有6.02×1021个电子通过时,乙中溶液的pH是13
9.下表中的实验,“操作和现象”与“结论”对应关系正确的是 ( )
|
|
操作和现象 |
结论 |
|
A |
向纯碱中滴加足量浓盐酸,将所得气体通入苯酚溶液中,溶液变浑浊 |
酸性:盐酸>碳酸>苯酚 |
|
B |
取某溶液少量,加入盐酸酸化的BaCl2溶液,出现白色沉淀 |
该溶液中一定含有大量的SO42- |
|
C |
取少量Fe(NO3)2试样加水溶液后加稀H2SO4酸化,滴加KSCN溶液,溶液变为红色 |
该Fe(NO3)2试样已经变质 |
|
D |
取皂化反应后的混合液滴入盛水的烧杯中,在液体表面出现油滴 |
皂化反应不完全 |
8.下列说法正确的是 ( )
A.可逆反应达平衡状态后,化学反应速率发生变化,平衡不一定移动
B.11.2LO2和CO2的混合气体中含有6.02×1023个氧原子
C.SO2溶于水能导电,它是电解质
D.由于H2O分子间存在氢键,所以H2O比H2S稳定
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com