
21.(8分)下表列出了①-⑩十种元素在周期表中的位置:
 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
|
2 |
|
|
|
① |
|
② |
|
|
|
3 |
|
|
③ |
④ |
|
⑤ |
⑥ |
⑦ |
|
4 |
⑧ |
⑨ |
|
|
|
|
⑩ |
|
(1)分别写出①、⑦、⑩的元素名称:① 、⑦ 、⑩ ;
(2)元素⑥最高价氧化物的水化物化学式为 ;元素④最高价氧化物水化物钠盐溶液俗称水玻璃,其溶质化学式是 。
(3)③、④、⑤、⑥四种元素中,原子半径由大到小的排列顺序是 >
> > (填写元素符号)。
(4)②和④可形成 (填“离子”或“共价”)化合物。
20.将SO2通入CuSO4和NaCl的浓溶液中,溶液颜色变浅,析出白色沉淀,取该沉淀分析,得知其中含Cl:35.7%、Cu:64.3%,在上述反应中SO2的作用是 ( )
A.作为酸 B.作为漂白剂 C.作为还原剂 D.作为氧化剂
第Ⅱ卷(非选择题,共50分)
19.两种元素A和B的原子序数都小于18。已知A元素原子最外层电子数为a,次外层电子数为b;B元素原子的M层电子数为(a一b),L层电子数为(a+b),则下列关于A、B两元素所形成稳定化合物的叙述不正确的是 ( )
A.玛瑙中含有该化合物 B.该化合物能与水反应
C.该化合物可用于制光导纤维 D.该化合物中B元素化合价为+4价
18.随着科技的飞速发展,出现了许多新型无机材料,如植入生物体内的生物陶瓷材料HAP[化学式为Cam(PO4)nOH]已被医疗上用于修补人的骨骼和牙组织。HAP的化学式中m等于 ( )
A.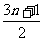 B.
B.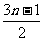 C.
C.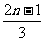 D.n+l
D.n+l
17.在①氯水;②漂白粉;③Na2O2;④H2O2;⑤活性炭;⑥SO2等六种物质中,能使品红溶液褪色的是 ( )
A.⑤⑥ B.⑥ C.①②③④ D.①②③④⑤⑥
16.下列离子能在溶液中大量共存的是 ( )
A.K+、H+、NO3-、SO42- B.Na+、H+、HCO3-、SO42-
C.K+、Ba2+、Cl-、CO32- D.Fe3+、Na+、OH-、Cl-
15.为了除去CO2中含有的少量SO2气体,可以使气体通过 ( )
A.NaOH溶液 B.饱和Na2CO3溶液
C.饱和NaHCO3溶液 D.Ca(OH)2溶液
14.下列说法正确的是 ( )
A.得电子难的原子,失电子一定容易
B.非金属单质一定不与任何酸反应
c.碱性氧化物一定为金属氧化物
D.酸性氧化物一定不与任何酸反应
13.用NA表示阿伏加德罗常数的数值,下列说法正确的是 ( )
A.常温常压下,NA个SO2的质量约为64 g
B.1 mol Fe与足量盐酸反应转移电子数为3NA个
C.0.1 mol/L的100 mLCH3COOH(醋酸)溶液中,含有的H+约为0.01 NA个
D.标准状况下,11.2 L SO3所含的原子数目为2NA
12.下列说法中,正确的是 ( )
A.在元素周期表里,主族元素所在的族序数等于原子的最外层电子数
B.卤族元素的最高正价均为+7
C.最外层电子数为8的粒子一定是稀有气体的原子
D.元素的原子序数越大,其原子半径也越大
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com